La miastenia gravis (MG) es una enfermedad autoinmune que afecta a la unión neuromuscular de músculos estriados. Provoca una debilidad fluctuante de la musculatura voluntaria, debida principalmente al ataque directo por medio de autoanticuerpos frente al receptor de acetilcolina1.
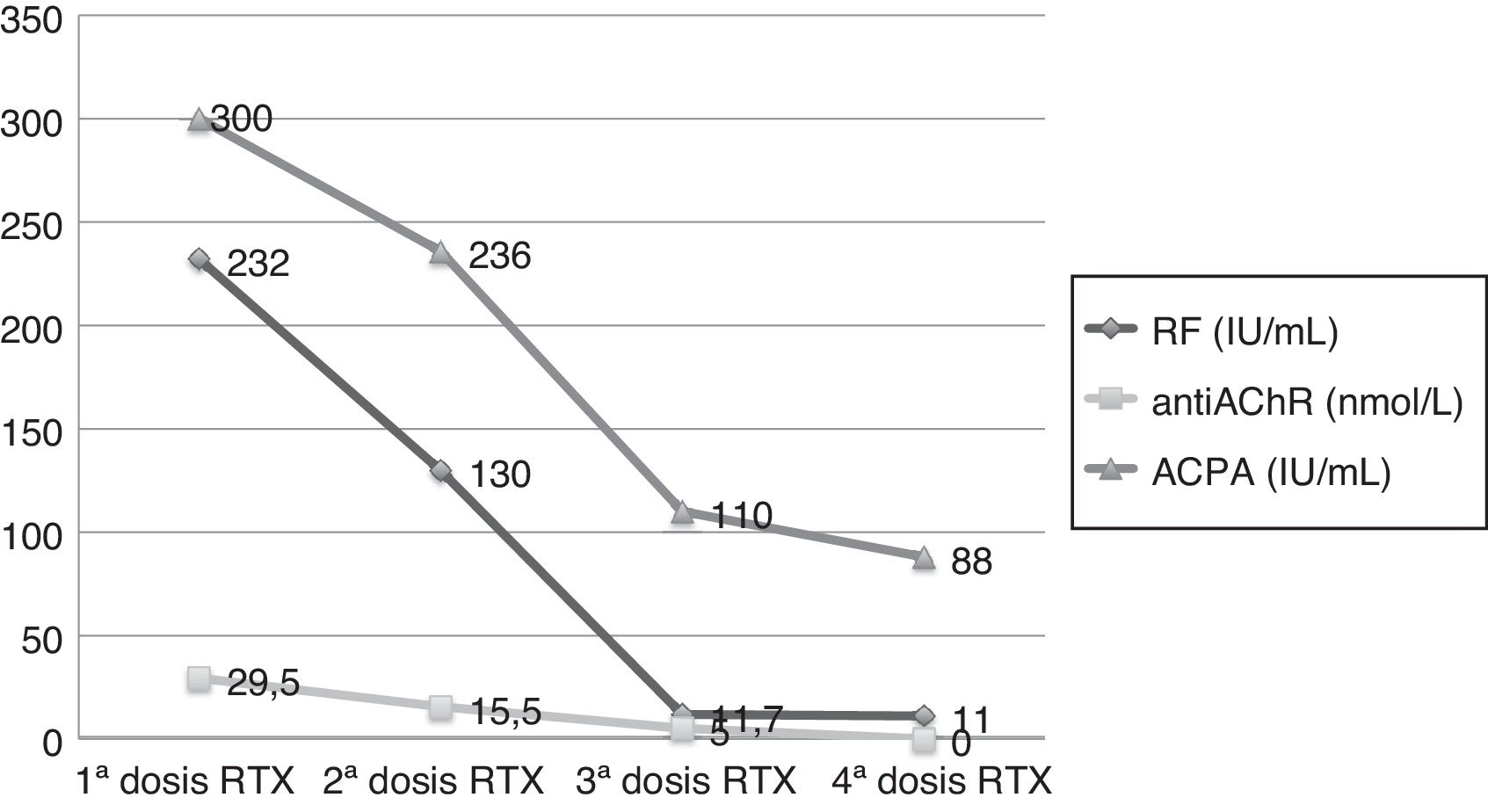
Mujer de 66 años, diagnosticada de artritis reumatoide (AR) en 2012, tratada con metotrexato 20mg/semanales. Después de 23 meses de buen control clínico, comenzó con actividad, por lo que se inició tratamiento con etanercept 50mg/semanales. Tras 6 dosis de etanercept, acudió a urgencias por ptosis completa de ojo derecho de curso fluctuante de 3 días de evolución y limitación de la supraversión ocular, consecuentemente, ingresó en neurología con la sospecha de MG-ocular. Durante el ingreso se realizaron RMN cerebral y TAC torácico, ambos normales. Analíticamente: VSG y PCR normales, ANA/ENA negativos, FR 232UI/ml (0-14), ACPA>300UI/ml (0-20) y anticuerpos anti-AChR 29,52nmol/l (0-0,25). El electromiograma reveló un aumento del jitter medio, presencia de bloqueos en músculo frontalis derecho y decremento de la amplitud de reposo del nervio facial a músculo nasalis, compatible con alteración de la transmisión neuromuscular post-sináptica. Confirmándose el diagnóstico de MG ocular se decidió suspender etanercept. Tras 3 semanas de interrupción del tratamiento con etanercept y con 30mg/día de prednisona, la paciente mejoró neurológicamente, pero en el transcurso de 12 semanas en progresiva reducción de prednisona, presentó un brote poliarticular y reaparición de sintomatología ocular. Se decidió administrar un ciclo de rituximab (2 dosis de 500mg separados 15 días) con dosis de retratamiento (500mg cada 6 meses), controlándose así, la sintomatología articular y neurológica (fig. 1).
Aproximadamente el 5% de la población padece una o más enfermedades autoinmunes, siendo la prevalencia más elevada en mujeres de mediana edad2. Aquellos pacientes que padecen una enfermedad autoinmune son más susceptibles a desarrollar una segunda. En el caso de la MG se asocia hasta en un 4% a la AR3.
Esta asociación puede deberse a factores inmunológicos que favorecen la activación de células B y células T autorreactivas, factores epigenéticos y susceptibilidad genética de determinados grupos de genes, particularmente aquellos pertenecientes al complejo mayor de histocompatibilidad (CMH)3. Por ello, si consideramos que la superposición de enfermedades autoinmunes es un reflejo de la existencia de mecanismos patógenos comunes, el abordaje terapéutico debería de ser común.
Los fármacos anti-TNFα han favorecido el tratamiento y pronóstico de las enfermedades reumáticas como la AR, además de utilizarse en otras enfermedades autoinmunes. De hecho, el etanercept, ha mostrado resultados satisfactorios en el tratamiento de MG refractaria4, sin efecto sobre los niveles plasmáticos de anti-AChR, ni modificación del TNFα circulante. Paradójicamente, existe un caso descrito en la literatura de MG en un paciente con AR en tratamiento con etanercept5, en el que la retirada del fármaco mejoró la clínica miasténica.
Aunque, no existe una asociación causal clara, el desarrollo de enfermedades neurológicas, sobre todo desmielinizantes (síndrome de Guillain-Barré, esclerosis múltiple, mononeuritis o polineuropatía crónica desmielinizante6,7) se han relacionado ocasionalmente con los anti-TNFα, en cuyo caso, la retirada del fármaco es la principal recomendación.
En este caso, ante la posibilidad de tratarse de una asociación entre 2 enfermedades autoinmunes o bien, de un probable efecto adverso de etanercept; se optó por retirar el fármaco e iniciar tratamiento con rituximab, ya que su utilidad está documentada en el tratamiento de la MG refractaria8. Gracias a su mecanismo de acción que provoca una depleción de células B y la consecuente disminución de anticuerpos, permitió el control clínico de ambas enfermedades. Generalmente se administran dosis de 375mg/m2 con dosis de retratamiento cada 6 meses dada la vida media del fármaco9, aunque aún no existe consenso en cuanto a la pauta de administración en MG.