Observar las características clínicas y de laboratorio de pacientes con diagnóstico inicial de polimialgia reumática (PMR), que luego desarrollaron otra enfermedad.
Material y métodoSe revisaron las historias clínicas de pacientes con diagnóstico de PMR de 3 hospitales de Argentina. Los pacientes tenían diagnóstico de PMR si cumplían con los siguientes criterios: edad ≥ 50 años, velocidad de sedimentación globular (VSG) > 40mm/h, dolor y rigidez persistente de al menos 1 mes de evolución en dos de las siguientes áreas: cuello o torso, hombros o región proximal de los brazos, caderas o región proximal de los miembros inferiores. Se prestó especial atención a los síntomas o signos de “alarma” que hicieran sospechar la presencia de otra enfermedad no PMR en un período ≤ 12 meses.
ResultadosSe incluyó a 200 pacientes, de los cuales 16 (8%), presentaron otra enfermedad durante el seguimiento. Las enfermedades diagnosticadas fueron neoplasias (n=4) y enfermedades reumáticas (n=4), además de endocarditis infecciosa (n=1), canal estrecho cervical (n=1), enfermedad de Parkinson (n=1), mialgias relacionada con estatinas (n=1), hipotiroidismo (n=1), hipovitaminosis D (n=1) y artropatía por depósito de cristales de pirofosfato cálcico dihidratado (PFCD) (n=2). El tiempo medio±desviación estándar al cambio de diagnóstico fue 4,5±3 meses. Diez pacientes no tuvieron respuesta a esteroides y 2 sujetos presentaron VSG persistentemente elevada.
ConclusionesEn este trabajo resaltamos la importancia de reconocer signos y síntomas clínicos, junto con datos de laboratorio y falta de respuesta al tratamiento como sospecha para diagnóstico de otra enfermedad en pacientes con manifestaciones que simulan PMR.
To examine the main clinical and laboratory data of patients initially diagnosed with polymyalgia rheumatica (PMR), which then developed another conditions.
Material and methodsWe reviewed the clinical records of patients diagnosed with PMR in three hospitals in Argentina. Patients had a diagnosis of PMR if they met the following criteria: age ≥ 50 years, erythrocyte sedimentation rate (ESR) at the time of diagnosis > 40mm, persistent pain and stiffness of at least one month of evolution in two of the following areas: neck, shoulders or proximal arms, hips or proximal lower limbs. Special attention was paid to symptoms or signs of “alarm” (beginning or during disease progression) for suspecting the presence of other non PMR disease within a period of ≤ 12 months.
ResultsSixteen of the 200 patients (8%) had other diseases during follow up. Malignancies (n=4) and rheumatic diseases (n=4) were the most common entities, in addition to infective endocarditis (n=1), narrow cervical canal (n=1), Parkinson's disease (n=1), statin-related myalgia (n=1), hypothyroidism (n=1), vitamin D deficiency (n=1) and Calcium Pyrophosphate Deposition Disease (CPDD) (n=2). The average length change of diagnosis was 4.5±3 months. Ten patients had no response to steroids and two had persistently elevated ESR.
ConclusionIn this study we highlight the importance of recognizing signs and symptoms along with laboratory data and lack of response to treatment as suspects for the diagnosis of other disease manifestations in patients with PMR symptoms.
La polimialgia reumática (PMR) es la enfermedad inflamatoria reumática más frecuente en la población anciana1. Si bien sus características clínicas son bien conocidas, no existe una prueba específica para su diagnóstico. Varios trabajos han descrito una amplia variedad de enfermedades que se presentan con síntomas polimiálgicos2-4.
El objetivo de este estudio fue observar las características clínicas y de laboratorio de pacientes con diagnóstico inicial PMR, que luego desarrollaron otra enfermedad.
Material y métodoSe revisaron las historias clínicas de pacientes con diagnóstico de PMR, entre enero 2004 y diciembre 2009, de 3 hospitales de Argentina: el Hospital J.M. Cullen de la ciudad de Santa Fe, el Hospital E. Tornú de la Ciudad Autónoma de Buenos Aires y el Hospital Privado de la Comunidad de Mar del Plata.
Los pacientes tenían diagnóstico de PMR si cumplían con los siguientes criterios5:
- –
Edad ≥ 50 años.
- –
Velocidad de sedimentación globular (VSG) > 40mm/h.
- –
Dolor y rigidez persistente de al menos un mes de evolución en dos de las siguientes áreas: cuello o torso, hombros o región proximal de los brazos, caderas o región proximal de los miembros inferiores.
Se podía incluir a pacientes menores de 50 años, si tenían síntomas típicos de PMR, VSG elevada y respuesta franca a esteroides.
Se registraron las características demográficas (sexo, edad de comienzo de la PMR), la duración de los síntomas (meses) antes del diagnóstico PMR, la rigidez matinal (duración) y la dosis inicial de esteroides (prednisona u otro).
Siguiendo a Gonzalez Gay et al2-4, se prestó especial atención a ciertos síntomas o signos de “alarma” (al inicio o durante la evolución) que hagan sospechar la presencia de otra enfermedad no PMR:
- –
Anamnesis: no empeoramiento de los síntomas con el movimiento, dolor difuso y rigidez matinal mínima.
- –
Examen físico: fiebre con o sin soplo, artritis de muñecas, metacarpofalángicas, interfalángicas proximales, metatarsofalángicas, dactilitis, talalgia, agrandamiento visceral y presencia de adenopatías.
- –
Laboratorio: citopenias, gammapatías monoclonales, aumento de transaminasas hepáticas, enzimas musculares, altos títulos de anticuerpos antinucleares (ANA), hematuria inexplicable y tirotropina (TSH).
Falta de respuesta se definió como la ausencia de resolución de los síntomas luego de 7 días de tratamiento con dosis bajas de esteroides (10-20mg/día).
Se consideró que los pacientes tenían PMR pura si cumplían los 3 criterios de inclusión, además de una respuesta completa a dosis bajas de esteroides (10-20mg/día). Los pacientes fueron clasificados de tener otras condiciones diferentes de PMR, si además de las características clínicas de PMR presentaban características clínicas y/o de laboratorio de otras enfermedades específicas al momento del diagnóstico o en un período ≤ 12 meses.
Se excluyó a pacientes que durante la evolución desarrollaron arteritis células gigantes (ACG) y artritis reumatoide (AR) de comienzo en el anciano.
El protocolo fue presentado y aprobado en el comité de ética de cada hospital participante del estudio.
ResultadosSe incluyó a 200 pacientes, de los cuales 16 (8%), que reunían criterios de clasificación para PMR, presentaron otra enfermedad durante el seguimiento. Las características principales se observan en la tabla 1. La mediana de duración de los síntomas, antes del diagnostico de PMR fue 1,5 meses (mínimo 1-máximo 6). Todos los pacientes presentaron síntomas proximales, junto con VSG elevada al momento de la consulta, y sólo 1 paciente tenía < 50 años. No se encontraron datos en cuanto a la duración de la rigidez matinal de 10 pacientes; 2 presentaron rigidez de 1h o más y 4 pacientes < 1h. Diez pacientes no tuvieron respuesta a una dosis media±desviación estándar de 15±6mg de prednisona. El tiempo medio al cambio de diagnostico fue 4,5 meses.
Principales características de los pacientes “no PMR”.
| Varones | 6 |
| Mujeres | 10 |
| Edad media al diagnóstico de PMR, años (media±DE) | 67±10 |
| VSG inicial (mm/h) (media±DE) | 78±17 |
| Dosis inicial media prednisona (mg/día) (media±DE) | 15±6 |
| Tiempo al cambio de diagnóstico, meses (media±DE) | 4,5±3 |
DE: desviación estándar; PMR: polimialgia reumática; VSG: velocidad de sedimentación globular.
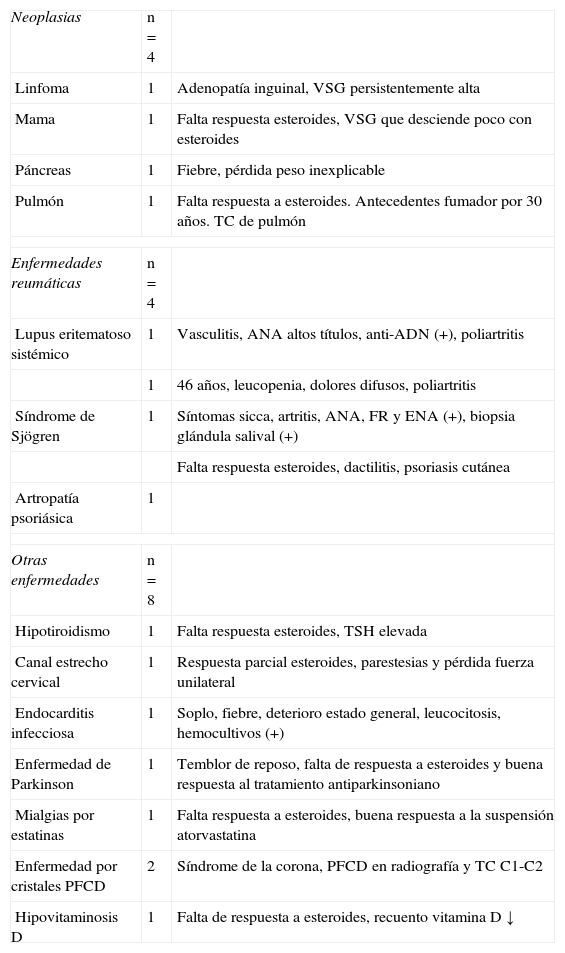
Las enfermedades más frecuentemente diagnosticadas fueron neoplasias y enfermedades reumáticas; además de endocarditis infecciosa, canal estrecho cervical, enfermedad de Parkinson y mialgias relacionada con drogas, hipotiroidismo, hipovitaminosis D y enfermedad por depósito de pirofosfato cálcico dihidratado (PFCD). Los principales signos y síntomas de alarma se observan en la tabla 2.
Datos clínicos o de laboratorio que indicaban la presencia de otra enfermedad (n=16).
| Neoplasias | n=4 | |
| Linfoma | 1 | Adenopatía inguinal, VSG persistentemente alta |
| Mama | 1 | Falta respuesta esteroides, VSG que desciende poco con esteroides |
| Páncreas | 1 | Fiebre, pérdida peso inexplicable |
| Pulmón | 1 | Falta respuesta a esteroides. Antecedentes fumador por 30 años. TC de pulmón |
| Enfermedades reumáticas | n=4 | |
| Lupus eritematoso sistémico | 1 | Vasculitis, ANA altos títulos, anti-ADN (+), poliartritis |
| 1 | 46 años, leucopenia, dolores difusos, poliartritis | |
| Síndrome de Sjögren | 1 | Síntomas sicca, artritis, ANA, FR y ENA (+), biopsia glándula salival (+) |
| Falta respuesta esteroides, dactilitis, psoriasis cutánea | ||
| Artropatía psoriásica | 1 | |
| Otras enfermedades | n=8 | |
| Hipotiroidismo | 1 | Falta respuesta esteroides, TSH elevada |
| Canal estrecho cervical | 1 | Respuesta parcial esteroides, parestesias y pérdida fuerza unilateral |
| Endocarditis infecciosa | 1 | Soplo, fiebre, deterioro estado general, leucocitosis, hemocultivos (+) |
| Enfermedad de Parkinson | 1 | Temblor de reposo, falta de respuesta a esteroides y buena respuesta al tratamiento antiparkinsoniano |
| Mialgias por estatinas | 1 | Falta respuesta a esteroides, buena respuesta a la suspensión atorvastatina |
| Enfermedad por cristales PFCD | 2 | Síndrome de la corona, PFCD en radiografía y TC C1-C2 |
| Hipovitaminosis D | 1 | Falta de respuesta a esteroides, recuento vitamina D ↓ |
ANA: anticuerpos antinucleares; ENA: antígenos nucleares extraíbles; FR: factor reumatoide; PFCD: pirofosfato cálcico dihidratado; TC: tomografía computarizada; TSH: tirotropina.
Cuatro pacientes desarrollaron neoplasias, 3 sólidas y 1 hematológica. En el primer paciente, las características que indicaron la presencia de otra condición no PMR fueron la falta de respuesta al tratamiento con esteroides, fiebre y pérdida de peso inexplicable, estudios de imagen posteriores mostraron adenocarcinoma de páncreas. Otra paciente persistía con síntomas polimiálgicos junto con VSG elevada a pesar del tratamiento, que motivó la realización de un centellograma óseo total revelando hipercaptaciones del radiofármaco sospechosas de metástasis, que finalmente correspondieron a un carcinoma de mama. El tercer paciente, con antecedentes de fumador, la tomografía mostró un nódulo pulmonar, que la biopsia informó como carcinoma. El cuarto paciente, varón con PMR típica y buena respuesta a 15mg prednisona, persistió durante el seguimiento con VSG elevada. A los 7 meses de tratamiento se presentó en la consulta de control con adenopatía inguinal izquierda; se realizó biopsia que mostró linfoma no Hodking.
Cuatro pacientes desarrollaron enfermedades reumáticas, 2 pacientes lupus eritematoso sistémico (LES), 1 paciente síndrome de Sjögren y el último, artropatía psoriásica. Los pacientes que desarrollaron LES tuvieron síntomas polimiálgicos con buena respuesta a esteroides, pero títulos altos de ANA. Uno de los pacientes tenía 46 años; los dolores eran más difusos y tuvo además leucopenia; ambos durante el seguimiento, presentaron artritis en las manos.
El tercer paciente, luego de 6 meses de tratamiento como PMR, presentó síntomas sicca que condujeron a la determinación de autoanticuerpos específicos y biopsia de glándula salival con diagnóstico final de síndrome de Sjögren.
Otras enfermedades fueron: hipotiroidismo, canal estrecho cervical, endocarditis infecciosa, enfermedad de Parkinson, mialgias por estatinas, artropatía por depósito de PFCD e hipovitaminosis D.
Una mujer de 68 años consultó por dolor y rigidez en el cuello y la cintura escapular, de 5 semanas de evolución, sin síntomas sistémicos y artritis bilateral de rodillas y carpo derecho. Los estudios radiológicos mostraron calcificaciones (tipo PFCD) del ligamento triangular de carpos, hombros, rodillas, caderas y sínfisis pubis; una tomografía computarizada (TC) de C1 y C2 mostró calcificación ligamento transverso. El otro paciente presento síndrome de la corona, que se confirmó con TC. Ambos fueron diagnosticados de enfermedad por depósito de cristales de PFCD y tuvieron buena respuesta a fármacos antiinflamatorios no esteroideos.
La falta de respuesta a los esteroides, además de la intensa fatiga y una TSH elevada, hicieron sospechar la presencia de hipotiroidismo. Esta falta de respuesta también se observó en: mialgias por estatinas (junto con resolución del cuadro con la suspensión de atorvastatina); hipovitaminosis D (aparte del recuento de valores reducidos de vitamina D y excelente respuesta a dosis altas de ésta) y endocarditis infecciosa por Enterococcus spp. (junto con deterioro progresivo del estado general, fiebre y soplo que motivó a la toma de cultivos y ecocardiograma).
Otro paciente que presentó dolor con rigidez cervical y cintura escapular de predominio izquierdo, mejoró parcialmente con esteroides; en la evolución agregó parestesias y pérdida de fuerza en la mano izquierda y fue diagnosticado de canal estrecho cervical.
DiscusiónCuando los pacientes se presentan con síntomas típicos de PMR, el diagnóstico es claro. Sin embargo, la PMR sigue siendo un desafío diagnóstico. Por un lado, por los múltiples diagnósticos diferenciales, ninguno de los hallazgos clínicos ni de laboratorio son específicos de la afección (manifestaciones de PMR pueden ocurrir en pacientes con infecciones, neoplasias y otras enfermedades reumáticas). Por otro lado, existe una relativa frecuencia de hallazgos “atípicos” (sinovitis periférica, dolor en extremidades distales, eritrosedimentación normal y debilidad muscular). Una anamnesis y un examen físico cuidadoso son las herramientas diagnósticas más importantes6.
Existen enfermedades que pueden causar dolor y confundirse con PMR, como la AR de comienzo en ancianos, miositis inflamatoria, espondiloartropatías de inicio tardío, vasculitis, polimiositis y fibromialgia. Los síndromes virales pueden ocasionar síntomas similares, pero generalmente tienen una duración más corta. Las infecciones crónicas, como la hepatitis C, la tuberculosis, la brucelosis, el virus de la inmunodeficiencia humana y la endocarditis bacteriana subaguda, además de los síndromes paraneoplásicos y las enfermedades endocrinas, como el hipotiroidismo e hipoparatiroidismo, pueden producir cansancio y mialgias7.
Gonzalez-Gay et al3 fueron los primeros en describir las características clínicas y de laboratorio de pacientes con manifestaciones que simulan PMR, que fueron diagnosticados de otra enfermedad, en una población bien definida de pacientes PMR, con o sin ACG. En su trabajo, encontraron 23/208 (11%) pacientes que presentaron síntomas polimiálgicos sin evidencia de otra enfermedad, que desarrollaron neoplasias dentro de los 3 meses del comienzo de los síntomas (10/23 pacientes, 5 sólidas y 5 hematológicas) y enfermedades reumáticas, con una media de demora para el diagnóstico de 13 meses (10/23 pacientes, 5 artritis seronegativa, 2 LES, 2 miopatías inflamatorias y 1 espondilitis anquilosante, además de endocarditis, hipotiroidismo y enfermedad de Parkinson).
En esta serie, 16/200 (8%) pacientes desarrollaron otras afecciones, en un tiempo medio de 4,5 meses de seguimiento y de manera similar al estudio de Gonzalez-Gay et al, las neoplasias y las enfermedades reumáticas fueron las enfermedades más frecuentemente encontradas. Excluimos de manera intencional a los pacientes con ACG y AR de comienzo de ancianos, por la relación ya conocida que existe entre estas entidades y la PMR7-12. En consecuencia, centraremos la discusión alrededor de otras entidades que no se consideran tanto.
La artropatía por depósito cristales de PFCD puede presentarse con una amplia variedad de síndromes clínicos, incluidos síntomas que simulan PMR/ACG (el compromiso de articulaciones proximales puede ser la presentación clínica de artropatía por PFCD), con elevación de reactantes de fase aguda y respuesta a esteroides. Recientemente, Pego-Reigosa et al13 analizaron a pacientes con PMR pura y enfermedad por PFCD tipo PMR buscando factores predictores que diferencien estas entidades. La presencia de artrosis tibio-femoral, calcificaciones tendinosas y artritis de tobillo deben hacer sospechar enfermedad por PFCD en pacientes con síntomas que simulan PMR. Por lo tanto, esta enfermedad por cristales debería incluirse en el espectro de afecciones que imitan a la PMR.
Dieppe et al14 comunicaron 8 pacientes con PMR supuesta, de una serie de 105 pacientes con artropatía por pirofosfato, y sugirieron que la enfermedad por PFCD puede presentarse con síntomas polimiálgicos o que el tratamiento con esteroides prescripto a estos pacientes con características de PMR puede predisponer al desarrollo de condrocalcinosis.
Se halló calcificación del ligamento transverso en el 44-71% de los pacientes con condrocalcinosis, mientras que el síndrome de la corona fue observó en el 9-45% en dos de estos estudios15-18.
En 2004, Aouba et al19 describieron a 3 pacientes con síndrome de la corona (asociación de calcificación radiológica del ligamento cruciforme alrededor del proceso odontoide y dolor agudo cervicoccipital, con fiebre, rigidez de cuello y síndrome inflamatorio biológico) y condrocalcinosis de la muñeca y rodilla, que fueron mal diagnosticados como PMR. La presencia de dolores cervicoccipitales agudos, fiebre y rigidez de cuello hacen imprescindible descartar otros diagnósticos, como meningitis, espondilitis y PMR/ACG. La identificación de este síndrome puede evitar investigaciones innecesarias, invasivas y caras, al igual que un tratamiento inadecuado, largo y potencialmente peligroso con esteroides, además de una internación prolongada en estos pacientes.
El síndrome que simula PMR y/o ACG puede ser la forma de presentación de una neoplasia. Haga et al20 comunican que el intervalo entre el diagnóstico de PMR y/o ACG y el registro de neoplasia (media 6,5 años) no es consistente con un mecanismo paraneoplásico.
Las neoplasias hematológicas, tales como mielodisplasia, leucemia, linfoma, mieloma o amiloidosis, pueden simular PMR. Por lo tanto, es importante detectar la presencia de citopenias, adenopatías, proteinuria o picos monoclonales en la corrida electroforética. De igual manera, las neoplasias sólidas (riñón, estómago, colon, páncreas, pulmón, próstata, ovario, útero) pueden presentarse como PMR y deben sospecharse por los antecedentes, síntomas atípicos (dolores difusos, pérdida de peso inexplicable, hematuria) y la falta de respuesta a esteroides.
En general, las mialgias asociadas a tumores sólidos no responden a la terapia esteroidea, en cambio las asociadas a neoplasias hematológicas pueden responder a dosis bajas de aquélla. Cuando se utilizan dosis altas se pueden enmascarar otras enfermedades, como problemas del manguito rotador, AR, infección, migraña o tumores.
Los pacientes ancianos con dolores musculoesqueléticos inespecíficos refractarios a fármacos antiinflamatorios no esteroideos tienen una prevalencia alta (30-90%) de presentar deficiencia de vitamina D. Esta se define habitualmente como valores de 25 hidroxivitamina D<20 ng/ml (50 nmol/l); el cuadro clínico puede ser sutil y no tenerse en cuenta. Los signos y síntomas pueden ser alteraciones esqueléticas y/o musculares, dependiendo de la gravedad del déficit, y se deben a osteomalacia o hiperparatiroidismo secundario. Éstos incluyen dolores difusos en la cintura escapular y pelviana, la caja torácica, la región lumbar y las piernas; fatiga general, dolor o debilidad muscular, y trastornos en la marcha. Estos pacientes a menudo son diagnosticados erróneamente como polimialgia reumática, fibromialgia o enfermedades malignas21.
La fiebre puede verse en PMR en el 35% de los pacientes; ésta (aún baja), junto a la poca respuesta a los esteroides, obliga a excluir una infección sistémica subyacente, sobre todo endocarditis bacteriana, que puede causar síntomas musculoesqueléticos en el 17%-44% de los casos22g. En regiones endémicas, otras enfermedades infecciosas crónicas (brucelosis, tuberculosis) deben tenerse en cuenta.
El hipotiroidismo en su forma idiopática es frecuentemente causado por una tiroiditis de Hashimoto, una enfermedad autoinmunitaria que puede asociarse con enfermedades del tejido conectivo. La prevalencia de manifestaciones musculoesqueléticas en pacientes con hipotiroidismo varía entre el 30 y el 80%. El hipotiroidismo grave puede presentar una artropatía mixedematosa que afecta a pequeñas y grandes articulaciones. La miopatía tiroidea es más común; se caracteriza por dolor y endurecimiento generalizados, pero afecta más a los músculos deltoides y cuádriceps, de forma similar que la PMR. Esta miopatía también puede causar debilidad muscular, con elevación de enzimas musculares, pero con TSH muy elevada23.
Los síntomas iniciales de la enfermedad de Parkinson son muy variados. El dolor en el cuello, la espalda o las extremidades, junto con rigidez en las regiones proximales que dificulta la marcha, puede preceder a los trastornos de motilidad y disfunción vegetativa durante meses. El diagnóstico se basa, fundamentalmente, en los datos clínicos y una buena respuesta a la levodopa24.
Se han comunicado varios fármacos que pueden ser causa de manifestaciones clínicas que sugieren PMR (enalapril, metoprolol, dipiridamol y estatinas)25. Las “estatinas” o inhibidores de la hidroximetilglutaril-coenzima A reductasa (HMG-CoA) se utilizan para disminuir la producción de colesterol y su uso está muy difundido en la actualidad. Si bien han demostrado ser, en general, seguras y bien toleradas, entre sus efectos adversos hay que tener en cuenta los síndromes miopáticos. Se han definido cuatro síndromes miopáticos relacionados con las estatinas: la miopatía por estatinas, mialgias, miositis y rabdomiólisis. De éstos, las mialgias relacionadas con las estatinas son las más frecuentemente observadas (1,5-10%)26.
El diagnóstico de LES de comienzo tardío puede confundirse con PMR. La presencia de síntomas vagos, como pérdida de peso y dolor muscular, en forma intermitente, demora el diagnóstico. Otra complicación es que los anticuerpos antinucleares no son una prueba de cribado útil, ya que hasta 36% de los ancianos sanos pueden tener ANA positivos a títulos bajos. Si bien las artralgias y la artritis son características comunes de presentación en el LES de inicio en el joven y el anciano, varios trabajos mostraron una frecuencia mayor de serositis y hemocitopenias en el LES del anciano27.
En los pacientes con síndrome de Sjögren, la presencia de síntomas extraglandulares, como fibromialgia, astenia y fatiga, pueden confundir el diagnóstico. Existen escasas comunicaciones en la literatura científica de PMR/ACG y síndrome de Sjögren primario28,29.
La mejoría con corticoides no es específica para el diagnóstico de PMR, pero su ausencia siempre requiere otra evaluación diagnóstica. En nuestra serie, la falta de respuesta a los esteroides se presentó en 10/16 (60%) pacientes y fue una de las principales características que alertó de la presencia de otra afección.
La VSG se utiliza no sólo para el diagnóstico, sino también para monitorear la actividad de la enfermedad. Debe prestarse una atención especial en los pacientes en que la VSG empieza a aumentar o se mantiene persistentemente elevada durante el tratamiento; esto podría significar que estamos en presencia de otra afección. En nuestra serie, 2/16 (12%) pacientes tuvieron VSG elevada persistente a pesar del tratamiento.
En este trabajo remarcamos la importancia de reconocer los signos y síntomas clínicos, los datos de laboratorio y la falta de respuesta al tratamiento como sospecha diagnóstica de otra enfermedad en pacientes con manifestaciones que simulan PMR.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.