El carácter crónico de las enfermedades del aparato locomotor requieren una atención integrada de atención primaria y las especialidades de reumatología, traumatología y rehabilitación. El objetivo del trabajo fue evaluar la implementación de un modelo organizativo integrado de gestión de la osteoporosis, lumbalgia, enfermedades del hombro y enfermedades de la rodilla mediante el proceso de mejora continua de Deming, teniendo en cuenta las derivaciones y el consumo de recursos.
Material y métodosEn la fase de planificación se utilizó un modelo de simulación para predecir la evolución del consumo de recursos en cada enfermedad del aparato locomotor y realizar un análisis del impacto presupuestario desde 2012 hasta 2020 en la comarca Goierri-Alto Urola. En la etapa de revisión se evaluó el estado del proceso en 2014 utilizando el análisis estadístico para comprobar el grado de consecución de los objetivos para cada enfermedad.
ResultadosSegún el modelo de simulación la población de pacientes con enfermedad osteomuscular aumentará en un 4,4% en 2020, con un incremento en costes para un sistema convencional de un 5,9%. Si la intervención integrada alcanzase sus objetivos este presupuesto se reduciría en un 8,5%. El análisis estadístico evidenció un descenso de derivaciones a traumatología y una reducción de consultas sucesivas en todas las especialidades.
DiscusiónLa implementación del modelo integrado en las enfermedades de osteoporosis, lumbalgia, hombro y rodilla está todavía en un estadio inicial. Sin embargo, el empoderamiento de la atención primaria mejoró la derivación de pacientes y redujo ligeramente los costes.
The chronic nature of musculoskeletal diseases requires an integrated care which involves the Primary Care and the specialities of Rheumatology, Traumatology and Rehabilitation. The aim of this study was to assess the implementation of an integrated organizational model in osteoporosis, low back pain, shoulder disease and knee disease using Deming's continuous improvement process and considering referrals and resource consumption.
Material and methodsA simulation model was used in the planning to predict the evolution of musculoskeletal diseases resource consumption and to carry out a Budget Impact Analysis from 2012 to 2020 in the Goierri-Alto Urola region. In the checking stage the status of the process in 2014 was evaluated using statistical analysis to check the degree of achievement of the objectives for each speciality.
ResultsSimulation models showed that population with musculoskeletal disease in Goierri-Alto Urola will increase a 4.4% by 2020. Because of that, the expenses for a conventional healthcare system will have increased a 5.9%. However, if the intervention reaches its objectives the budget would decrease an 8.5%. The statistical analysis evidenced a decline in referrals to Traumatology service and a reduction of successive consultations in all specialities.
DiscussionThe implementation of the integrated organizational model in osteoporosis, low back pain, shoulder disease and knee disease is still at an early stage. However, the empowerment of Primary Care improved patient referrals and reduced the costs.
El incremento de la prevalencia de enfermedades crónicas debido al envejecimiento está determinando un cambio en la organización de los servicios sanitarios1–3. La integración asistencial es un nuevo enfoque dirigido a corregir la fragmentación de los sistemas sanitarios tradicionales4–6. Estos nuevos modelos organizativos se han aplicado con asiduidad en los programas de atención a pacientes crónicos frágiles7,8. Por el contrario, en el campo del aparato locomotor existe poca literatura acerca de la integración de atención primaria (AP) y atención hospitalaria (AH), a pesar de que la enfermedad osteomuscular es el primer motivo de derivación desde AP y genera con frecuencia listas de espera9. Además, el carácter crónico de gran parte de esta enfermedad hace que los pacientes tengan una relación recurrente con AP y las especialidades de reumatología, traumatología y rehabilitación4,10.
La creación de las Organizaciones Sanitarias Integradas (OSI) en el Sistema Vasco de Salud impulsó la integración de la AP y la AH mediante una gestión orientada al paciente que también se aplicó al aparato locomotor11. En esta línea, en la OSI Goierri-Alto Urola se implantó un nuevo modelo de atención clínica integrada mediante el desarrollo de rutas asistenciales comunes elaboradas por un grupo multidisciplinar compuesto por reumatólogos, traumatólogos, rehabilitadores y médicos de familia, por entender que las enfermedades del aparato locomotor requieren un planteamiento común de todos los profesionales implicados12. Las rutas recogieron los aspectos principales en el manejo del paciente con enfermedad osteomuscular, así como las indicaciones para su derivación a las especialidades de reumatología, traumatología y rehabilitación5,13. El nuevo modelo se basó en el empoderamiento de la AP, dando acceso a los médicos de familia a pruebas diagnósticas complejas como resonancia magnética nuclear o densitometrías14,15. También se implantó la interconsulta no presencial para facilitar la comunicación entre diferentes niveles de atención y evitar a los pacientes desplazamientos innecesarios16,17. Sus características de intervención compleja hacen de su implantación un reto en el que hay que separar la eficacia de la intervención de su despliegue organizativo18–20.
El objetivo de este estudio se dirigió a evaluar la implementación del modelo organizativo integrado de gestión de las enfermedades del aparato locomotor en la OSI, incorporando el uso de modelos de simulación y el análisis estadístico en el proceso de mejora continua Plan-Do-Check-Act (PDCA) de Deming21,22.
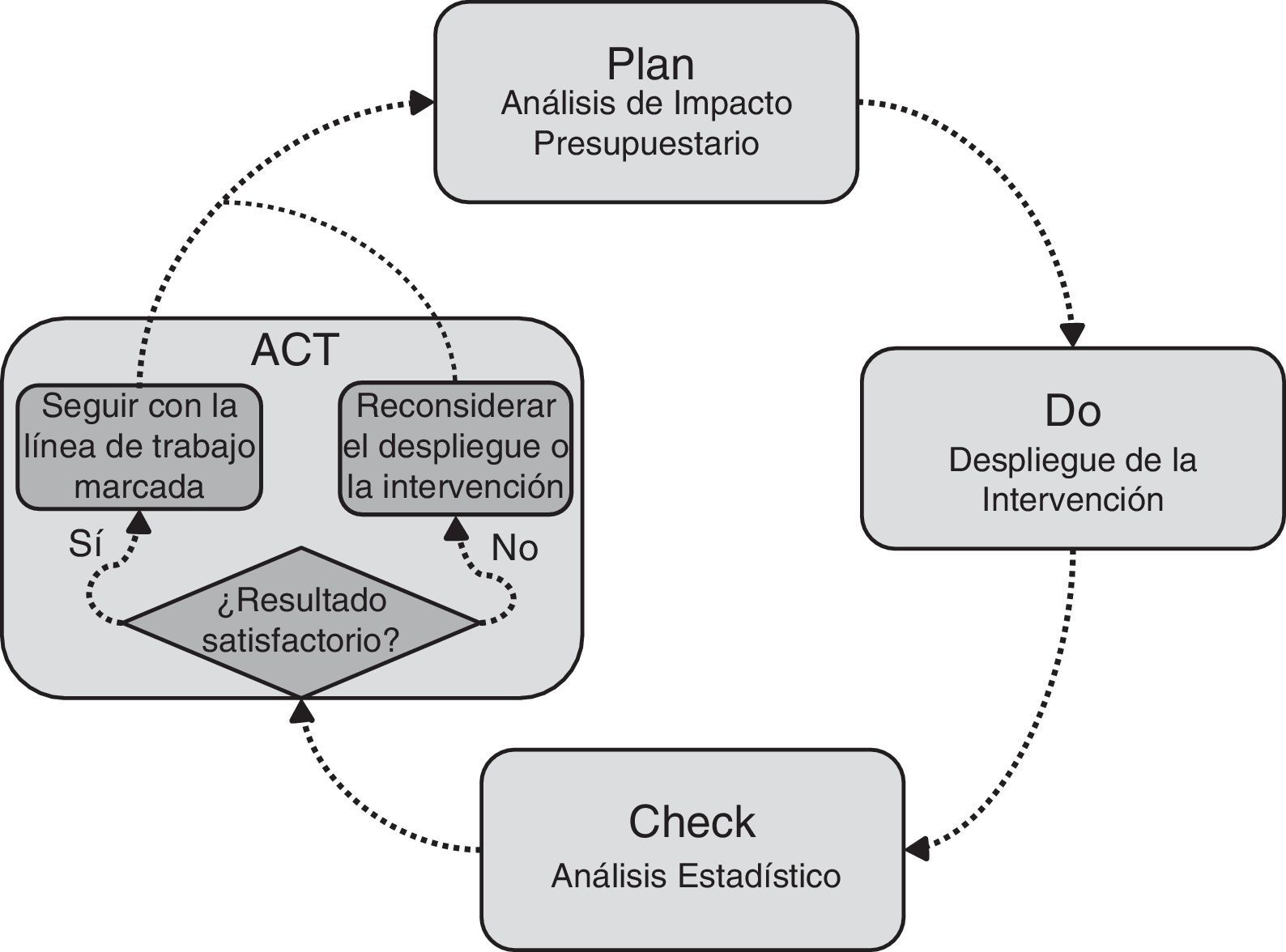
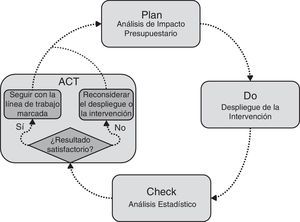
Material y métodosEl estudio fue de tipo evaluativo y se llevó a cabo utilizando grandes bases de datos (Big Data) a partir de los registros administrativos y clínicos de Osakidetza. Debido a la dificultad de evaluación de las intervenciones complejas18–20, se planteó un nuevo diseño de evaluación comparando la nueva intervención con el modelo convencional. Para ello, el estudio se basó en el enfoque PDCA, una herramienta clásica en gestión que consiste en repetir un proceso de mejora continua de 4 fases: Plan, Do, Check y Act21,22. El enfoque planteado se centró en dar contenido al Plan con un análisis de impacto presupuestario (AIP) mediante un modelo de simulación, y al Check con un análisis estadístico23,24. El primero permitió representar la intervención delimitando el impacto en función de los objetivos25. El segundo sirvió para testar el grado de consecución de dichos objetivos y observar la tendencia de la intervención, comprobando así si se estaba generando el impacto deseado. La figura 1 muestra cómo se integraron el AIP y el análisis estadístico dentro del marco de gestión PDCA. En función de esto se partió de la situación anterior al despliegue del modelo integrado en el año 2012. Se utilizó la simulación para predecir la evolución del consumo de recursos de la OSI y realizar un AIP desde 2012 hasta 2020 en 2 escenarios: caso base y escenario con objetivos cumplidos (Plan). De acuerdo con lo planificado, una vez iniciado el despliegue los costes reales deberían converger paulatinamente hacia el objetivo del modelo integrado (Do). Con los datos de 2014 se evaluó el estado del proceso, utilizando el análisis estadístico para compararlo con los datos de 2012 y comprobar el grado de consecución de los objetivos y la tendencia de la intervención (Check). Así, en función del resultado del análisis, se podría actuar en consecuencia para mantener el planteamiento del proyecto o ajustar el despliegue de la intervención (Act).
La OSI Goierri-Alto Urola cubre una población total de 95.000 habitantes y la muestra analizada incluyó todos los episodios con enfermedades del aparato locomotor atendidos en AP (27.060 en 2012 y 27.462 en 2014) y AH (9.358 en 2012 y 10.552 en 2014). Mediante el sistema Adjusted Clinical Groups (ACG) se clasificaron las enfermedades del aparato locomotor en 17 grupos que se muestran en la tabla 1 del anexo on-line, de los cuales 2 fueron creados para poder agrupar las enfermedades del hombro y la rodilla26. Pese a que la implementación del programa integrado tiene como objetivo intervenir en todos los grupos ACG, inicialmente solo actuó en 4 de ellos: osteoporosis, lumbalgia, enfermedades del hombro y enfermedades de la rodilla. Los grupos intervenidos fueron seleccionados debido a que son las enfermedades que mayor carga de trabajo y consumo de recursos generan. En cambio, a la hora de realizar el estudio se analizaron todos los grupos patológicos para poder mostrar el impacto de la intervención en el conjunto total del aparato locomotor. La intervención se limitó a las consultas externas y no influyó en la hospitalización quirúrgica asociada.
Al comparar los 2 modelos organizativos se observa que en el modelo tradicional el paciente iniciaba un episodio de atención nuevo cada vez que cambiaba de nivel asistencial27. Esto implicaba una repetición de pasos clínicos, un aumento de las listas de espera y, por tanto, problemas de acceso, continuidad, fragmentación, ineficiencia y calidad28,29. El despliegue de la intervención integrada comenzó en 2013 y consistió en el uso de rutas asistenciales conjuntas para AP y AH, el acceso a pruebas diagnósticas por parte de AP (resonancia magnética nuclear y densitometrías) y las interconsultas no presenciales con especialistas. Las rutas asistenciales se consensuaron entre los médicos de AP y AH para actuar con criterios homogéneos y coordinados5,13. Se definió la ruta óptima a seguir por los pacientes según su enfermedad y se facilitó el acceso a pruebas diagnósticas para aumentar la capacidad de resolución de problemas en AP y evitar la derivación no justificada a especialistas hospitalarios14,15. También se implantó la interconsulta no presencial para facilitar la comunicación entre diferentes niveles de atención y evitar desplazamientos innecesarios de los pacientes16,17. El objetivo pretendido en términos de uso de recursos fue una reducción de las derivaciones y de la relación sucesivas/primeras en consultas especializadas. El uso de las rutas también pretendió disminuir la carga de trabajo derivada a traumatología, dirigiendo directamente los pacientes a reumatología y rehabilitación, sin tener que pasar por el traumatólogo13. El análisis de los resultados se basó en el consumo de recursos y los costes.
Los objetivos se definieron utilizando el método Delphi30. Mediante la consulta a un grupo de clínicos y gestores de la OSI, a los que se les facilitó las tasas de derivación por enfermedad entre los años 2010 y 2012, se fijaron las tasas a conseguir en 2020 (osteoporosis 7,5%, lumbalgia 6%, enfermedades del hombro 13,7% y enfermedades de la rodilla 11,6%). Además, se estimó que la relación sucesivas/primeras podría reducirse un tercio. Los indicadores planteados para la evaluación del programa integrado fueron el número de derivaciones desde AP, el reparto de las derivaciones por especialidad, el número de consultas por episodio para cada especialidad y los costes.
La información necesaria para realizar el estudio referente a los años 2012 y 2014 se extrajo de las bases de datos administrativas y clínicas de la OSI, obteniendo los costes unitarios de las consultas (AP y AH) en el año 2012 del sistema de contabilidad analítica. Para las proyecciones de población entre 2012 y 2020, en cambio, se utilizaron las bases de datos del Instituto Vasco de Estadística (EUSTAT). Todos los parámetros utilizados y su fuente se encuentran disponibles en la tabla 2 del anexo on-line.
Análisis del impacto presupuestarioPara calcular el impacto presupuestario se representó mediante simulación de eventos discretos el flujo de pacientes con enfermedad osteomuscular y se predijo la evolución del consumo de recursos y la carga económica desde 2012 hasta 202025. Según Mauskopf, el AIP mide el impacto de un nuevo tratamiento en el coste anual, el beneficio en salud anual y en otros resultados de interés en los años posteriores a su introducción en un sistema nacional de salud o en un plan de salud privado23. Por su parte, la simulación de eventos discretos es un método de modelado flexible que permite representar comportamientos complejos e interacciones entre diferentes individuos, niveles y entornos31,32. El modelo se construyó mediante el software Arena® de Rockwell Automation. Primero, se obtuvieron las funciones matemáticas para construir el modelo convencional utilizando la información referente al año 2012. Para representar el escenario del modelo integrado se agregaron los objetivos que se esperaban alcanzar estimados por el estudio Delphi30.
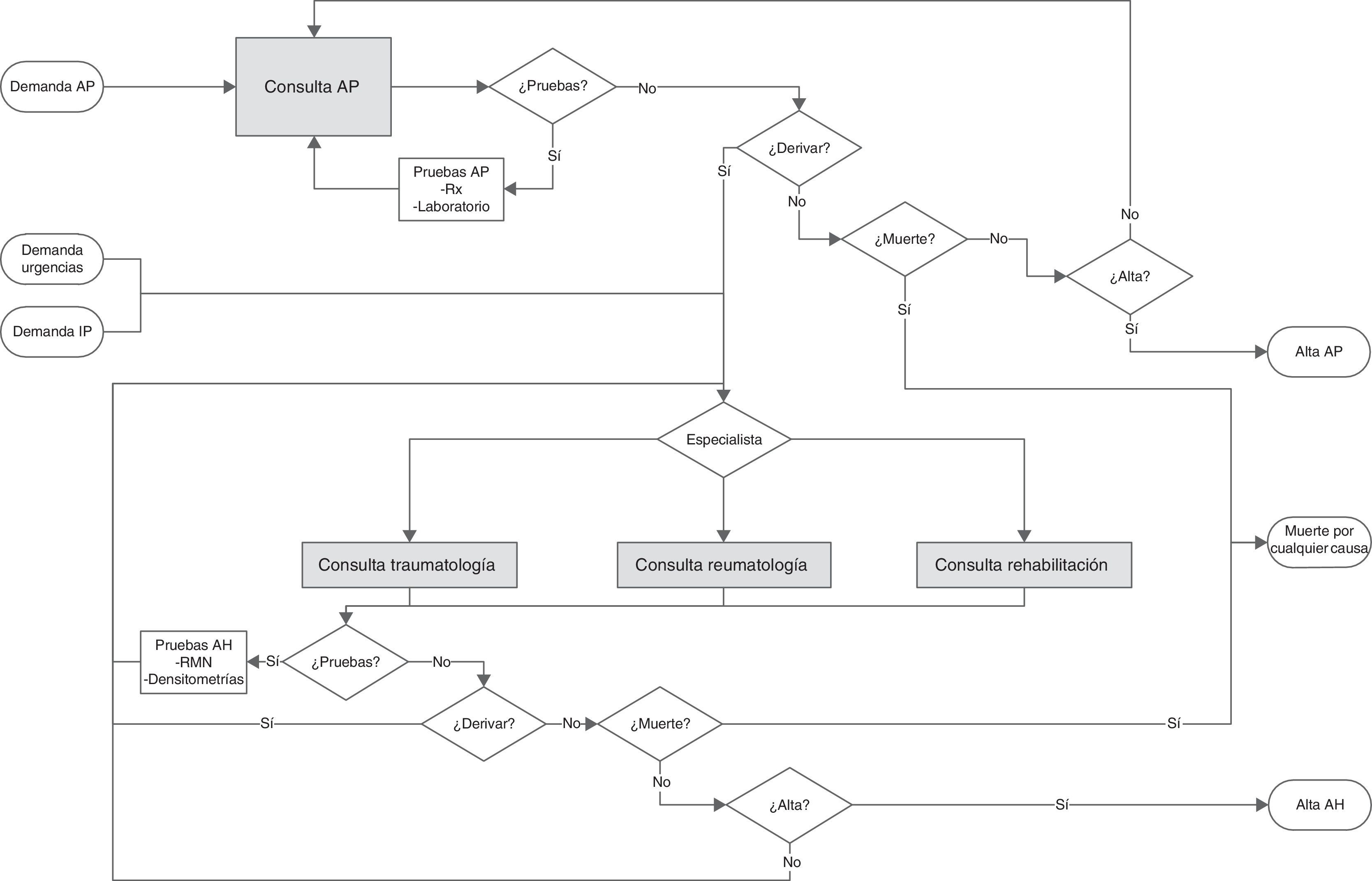
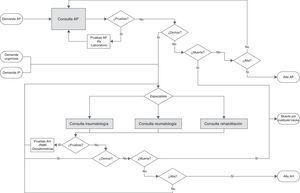
Para representar la historia natural del paciente a cada individuo que entra al sistema se le asignan los atributos personales que determinarán su camino a seguir dentro del modelo. Mientras no fallezcan (muerte por cualquier causa) permanecen en el sistema hasta ser derivados o ser dados de alta. La figura 2 muestra el modelo conceptual con las posibles rutas y contactos que pueden mantener los pacientes. La entrada a AH puede darse por 3 orígenes diferentes: AP, urgencias o iniciativa propia. Los pacientes que entran a través de AP lo hacen pasando por la consulta del médico de cabecera. En cambio, los individuos que entran por urgencias o por iniciativa propia pasan directamente a AH. En ambos niveles asistenciales los pacientes podrán necesitar diversas consultas antes de ser derivados o hasta ser dados de alta. El modelo de simulación se validó haciendo una prueba de bondad de ajuste (Goodness of Fit). En el anexo on-line se describe con detalle el modelo de simulación y entre las tablas 3-8 se encuentran los resultados de validación empleados.
Una vez validado el modelo se calculó el consumo de recursos en cada escenario. Multiplicando las tasas de consumo por los costes unitarios se obtuvo el coste de la enfermedad para el sistema tradicional y el sistema integrado. El consumo de recursos y los costes en cada escenario se proyectaron en el tiempo desde el año 2012 hasta 2020, teniendo en cuenta el efecto del envejecimiento poblacional.
Análisis estadísticoEl análisis estadístico comparó los datos observados en 2012 y 2014 para ver si había cambiado el consumo de recursos. También se midió la distancia real que existía en 2014 entre los resultados observados y el objetivo. Para el análisis se utilizaron todas las consultas realizadas en AP y AH en un año natural. Aunque algunas consultas perteneciesen a episodios abiertos en años anteriores, y otros episodios quedasen sin cerrar a final de año, se estimó que al incluir todas las consultas esta diferencia quedaba compensada. Primero, un análisis descriptivo univariante permitió ver si había diferencias sociodemográficas y clínicas. En el segundo paso se analizaron las tasas de derivación y consumo de recursos por grupo. Para hacer este análisis univariante, primero se llevó a cabo una categorización de las tasas para así aplicar el test Chi-cuadrado y poder ver si existían diferencias estadísticamente significativas entre los grupos. Las tasas de derivación se categorizaron en 2 grupos (no derivado, derivado). Además, para los episodios derivados se diferenció a qué especialidad fueron remitidos. Por su parte, para analizar las tasas de consumo de recursos se categorizaron los episodios en 3 grupos (una consulta, 2-5 consultas, >5 consultas). Sin embargo, en los resultados se muestran las medias para facilitar la interpretación. El último punto del análisis estadístico consistió en una evaluación univariante de los costes de AP y AH por grupo. El procedimiento aplicado fue el test Mann-Whitney U.
ResultadosEl análisis descriptivo se ha remitido a la tabla 9 del anexo on-line. Sus resultados no mostraron diferencias significativas entre las características sociodemográficas y clínicas de ambos grupos.
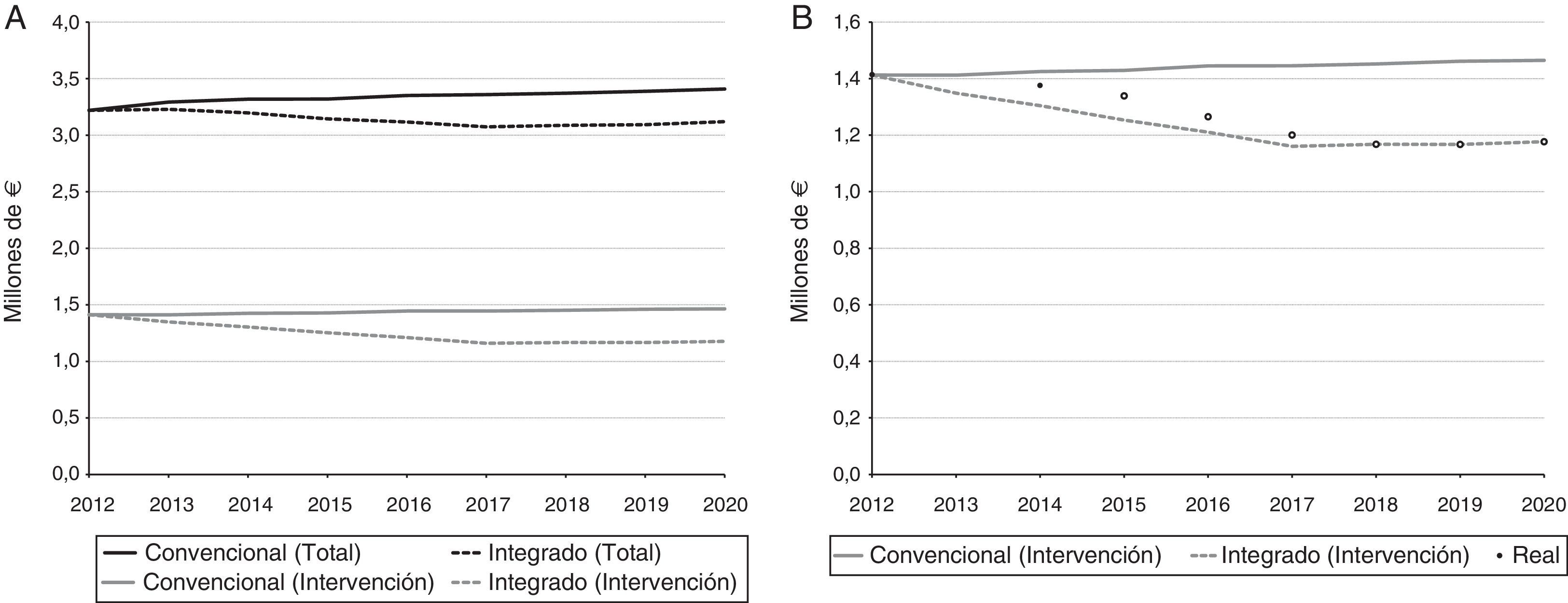
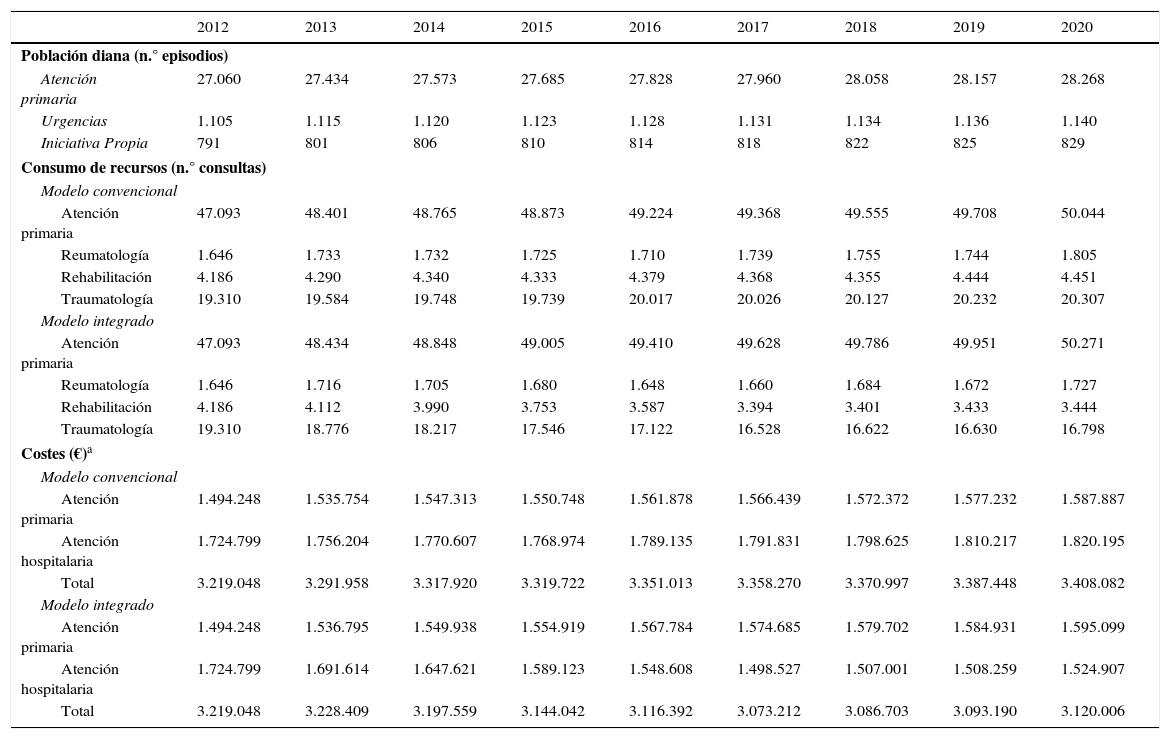
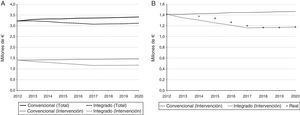
Por su parte, los resultados del AIP se muestran en la tabla 1. En la primera fila se observa cómo cambia la población diana en la comarca de Goierri-Alto Urola de acuerdo al envejecimiento poblacional. Para 2020 se previó un incremento de la incidencia del 4,4%. También se muestra la posible evolución en el tiempo del número de consultas realizadas en AP y AH junto con sus gastos asociados. Los costes para un sistema de salud convencional aumentan en un 5,9%. En cambio, considerando una situación hipotética en la que la intervención resultase satisfactoria en 5 años, se observó que el presupuesto en 2020 podría reducirse un 8,5%. La evolución del coste por año para cada escenario se representa gráficamente en la figura 3A.
Extrapolación del 2012 al 2020 de la población diana, el número de consultas según el modelo organizativo y el análisis de impacto presupuestario
| 2012 | 2013 | 2014 | 2015 | 2016 | 2017 | 2018 | 2019 | 2020 | |
|---|---|---|---|---|---|---|---|---|---|
| Población diana (n.° episodios) | |||||||||
| Atención primaria | 27.060 | 27.434 | 27.573 | 27.685 | 27.828 | 27.960 | 28.058 | 28.157 | 28.268 |
| Urgencias | 1.105 | 1.115 | 1.120 | 1.123 | 1.128 | 1.131 | 1.134 | 1.136 | 1.140 |
| Iniciativa Propia | 791 | 801 | 806 | 810 | 814 | 818 | 822 | 825 | 829 |
| Consumo de recursos (n.° consultas) | |||||||||
| Modelo convencional | |||||||||
| Atención primaria | 47.093 | 48.401 | 48.765 | 48.873 | 49.224 | 49.368 | 49.555 | 49.708 | 50.044 |
| Reumatología | 1.646 | 1.733 | 1.732 | 1.725 | 1.710 | 1.739 | 1.755 | 1.744 | 1.805 |
| Rehabilitación | 4.186 | 4.290 | 4.340 | 4.333 | 4.379 | 4.368 | 4.355 | 4.444 | 4.451 |
| Traumatología | 19.310 | 19.584 | 19.748 | 19.739 | 20.017 | 20.026 | 20.127 | 20.232 | 20.307 |
| Modelo integrado | |||||||||
| Atención primaria | 47.093 | 48.434 | 48.848 | 49.005 | 49.410 | 49.628 | 49.786 | 49.951 | 50.271 |
| Reumatología | 1.646 | 1.716 | 1.705 | 1.680 | 1.648 | 1.660 | 1.684 | 1.672 | 1.727 |
| Rehabilitación | 4.186 | 4.112 | 3.990 | 3.753 | 3.587 | 3.394 | 3.401 | 3.433 | 3.444 |
| Traumatología | 19.310 | 18.776 | 18.217 | 17.546 | 17.122 | 16.528 | 16.622 | 16.630 | 16.798 |
| Costes (€)a | |||||||||
| Modelo convencional | |||||||||
| Atención primaria | 1.494.248 | 1.535.754 | 1.547.313 | 1.550.748 | 1.561.878 | 1.566.439 | 1.572.372 | 1.577.232 | 1.587.887 |
| Atención hospitalaria | 1.724.799 | 1.756.204 | 1.770.607 | 1.768.974 | 1.789.135 | 1.791.831 | 1.798.625 | 1.810.217 | 1.820.195 |
| Total | 3.219.048 | 3.291.958 | 3.317.920 | 3.319.722 | 3.351.013 | 3.358.270 | 3.370.997 | 3.387.448 | 3.408.082 |
| Modelo integrado | |||||||||
| Atención primaria | 1.494.248 | 1.536.795 | 1.549.938 | 1.554.919 | 1.567.784 | 1.574.685 | 1.579.702 | 1.584.931 | 1.595.099 |
| Atención hospitalaria | 1.724.799 | 1.691.614 | 1.647.621 | 1.589.123 | 1.548.608 | 1.498.527 | 1.507.001 | 1.508.259 | 1.524.907 |
| Total | 3.219.048 | 3.228.409 | 3.197.559 | 3.144.042 | 3.116.392 | 3.073.212 | 3.086.703 | 3.093.190 | 3.120.006 |
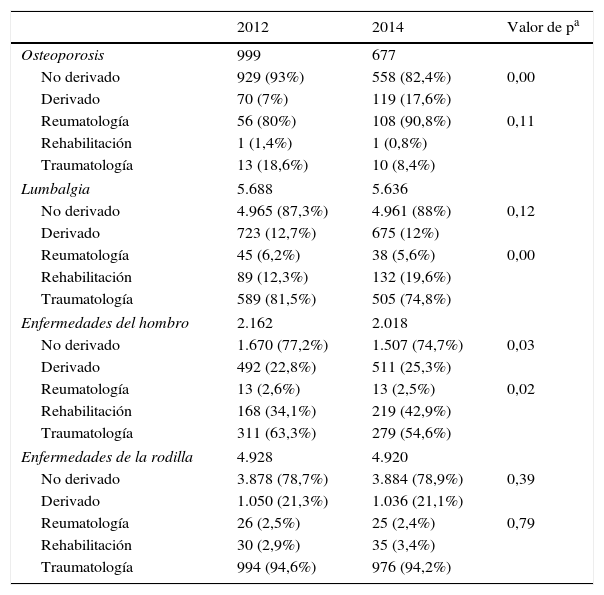
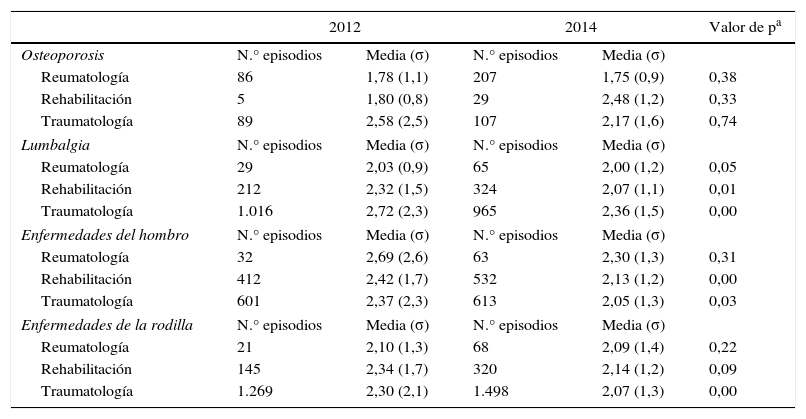
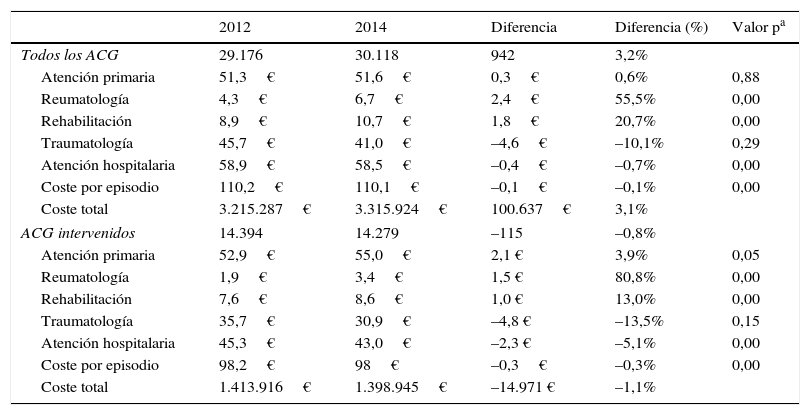
Por otro lado, al hacer el análisis estadístico y analizar los 2 periodos no se observó ninguna mejoría estadísticamente significativa en cuanto a la reducción de la derivación se refiere (tabla 2). No obstante, sí descendieron las derivaciones al servicio de traumatología. En el nivel especializado se observó una reducción del número de consultas por episodio en la mayoría de los casos (tabla 3). Los valores p de esta tabla surgen del análisis que se realizó con los episodios categorizados por número de consultas, resultados que se amplían en la tabla 10 del anexo on-line. El impacto de la intervención también se hizo visible en los costes (tabla 4).
Análisis estadístico univariante de las derivaciones realizadas desde AP a AH en 2012 y 2014
| 2012 | 2014 | Valor de pa | |
|---|---|---|---|
| Osteoporosis | 999 | 677 | |
| No derivado | 929 (93%) | 558 (82,4%) | 0,00 |
| Derivado | 70 (7%) | 119 (17,6%) | |
| Reumatología | 56 (80%) | 108 (90,8%) | 0,11 |
| Rehabilitación | 1 (1,4%) | 1 (0,8%) | |
| Traumatología | 13 (18,6%) | 10 (8,4%) | |
| Lumbalgia | 5.688 | 5.636 | |
| No derivado | 4.965 (87,3%) | 4.961 (88%) | 0,12 |
| Derivado | 723 (12,7%) | 675 (12%) | |
| Reumatología | 45 (6,2%) | 38 (5,6%) | 0,00 |
| Rehabilitación | 89 (12,3%) | 132 (19,6%) | |
| Traumatología | 589 (81,5%) | 505 (74,8%) | |
| Enfermedades del hombro | 2.162 | 2.018 | |
| No derivado | 1.670 (77,2%) | 1.507 (74,7%) | 0,03 |
| Derivado | 492 (22,8%) | 511 (25,3%) | |
| Reumatología | 13 (2,6%) | 13 (2,5%) | 0,02 |
| Rehabilitación | 168 (34,1%) | 219 (42,9%) | |
| Traumatología | 311 (63,3%) | 279 (54,6%) | |
| Enfermedades de la rodilla | 4.928 | 4.920 | |
| No derivado | 3.878 (78,7%) | 3.884 (78,9%) | 0,39 |
| Derivado | 1.050 (21,3%) | 1.036 (21,1%) | |
| Reumatología | 26 (2,5%) | 25 (2,4%) | 0,79 |
| Rehabilitación | 30 (2,9%) | 35 (3,4%) | |
| Traumatología | 994 (94,6%) | 976 (94,2%) | |
Análisis estadístico univariante por patología y especialidad hospitalaria del número de consultas por episodio en 2012 y 2014
| 2012 | 2014 | Valor de pa | |||
|---|---|---|---|---|---|
| Osteoporosis | N.° episodios | Media (σ) | N.° episodios | Media (σ) | |
| Reumatología | 86 | 1,78 (1,1) | 207 | 1,75 (0,9) | 0,38 |
| Rehabilitación | 5 | 1,80 (0,8) | 29 | 2,48 (1,2) | 0,33 |
| Traumatología | 89 | 2,58 (2,5) | 107 | 2,17 (1,6) | 0,74 |
| Lumbalgia | N.° episodios | Media (σ) | N.° episodios | Media (σ) | |
| Reumatología | 29 | 2,03 (0,9) | 65 | 2,00 (1,2) | 0,05 |
| Rehabilitación | 212 | 2,32 (1,5) | 324 | 2,07 (1,1) | 0,01 |
| Traumatología | 1.016 | 2,72 (2,3) | 965 | 2,36 (1,5) | 0,00 |
| Enfermedades del hombro | N.° episodios | Media (σ) | N.° episodios | Media (σ) | |
| Reumatología | 32 | 2,69 (2,6) | 63 | 2,30 (1,3) | 0,31 |
| Rehabilitación | 412 | 2,42 (1,7) | 532 | 2,13 (1,2) | 0,00 |
| Traumatología | 601 | 2,37 (2,3) | 613 | 2,05 (1,3) | 0,03 |
| Enfermedades de la rodilla | N.° episodios | Media (σ) | N.° episodios | Media (σ) | |
| Reumatología | 21 | 2,10 (1,3) | 68 | 2,09 (1,4) | 0,22 |
| Rehabilitación | 145 | 2,34 (1,7) | 320 | 2,14 (1,2) | 0,09 |
| Traumatología | 1.269 | 2,30 (2,1) | 1.498 | 2,07 (1,3) | 0,00 |
Análisis estadístico univariante de los costes utilizando los costes unitarios referentes al año 2012
| 2012 | 2014 | Diferencia | Diferencia (%) | Valor pa | |
|---|---|---|---|---|---|
| Todos los ACG | 29.176 | 30.118 | 942 | 3,2% | |
| Atención primaria | 51,3€ | 51,6€ | 0,3€ | 0,6% | 0,88 |
| Reumatología | 4,3€ | 6,7€ | 2,4€ | 55,5% | 0,00 |
| Rehabilitación | 8,9€ | 10,7€ | 1,8€ | 20,7% | 0,00 |
| Traumatología | 45,7€ | 41,0€ | –4,6€ | –10,1% | 0,29 |
| Atención hospitalaria | 58,9€ | 58,5€ | –0,4€ | –0,7% | 0,00 |
| Coste por episodio | 110,2€ | 110,1€ | –0,1€ | –0,1% | 0,00 |
| Coste total | 3.215.287€ | 3.315.924€ | 100.637€ | 3,1% | |
| ACG intervenidos | 14.394 | 14.279 | –115 | –0,8% | |
| Atención primaria | 52,9€ | 55,0€ | 2,1 € | 3,9% | 0,05 |
| Reumatología | 1,9€ | 3,4€ | 1,5 € | 80,8% | 0,00 |
| Rehabilitación | 7,6€ | 8,6€ | 1,0 € | 13,0% | 0,00 |
| Traumatología | 35,7€ | 30,9€ | –4,8 € | –13,5% | 0,15 |
| Atención hospitalaria | 45,3€ | 43,0€ | –2,3 € | –5,1% | 0,00 |
| Coste por episodio | 98,2€ | 98€ | –0,3€ | –0,3% | 0,00 |
| Coste total | 1.413.916€ | 1.398.945€ | –14.971 € | –1,1% | |
Como último punto se comparó la situación de 2014 con el objetivo. La figura 3B incluye el coste total de 2014 al AIP, así como su posible evolución en los años venideros. Se puede ver cómo el coste de 2014 se separa ligeramente de la línea que sigue el modelo convencional. La predicción fue que a medida que el modelo integrado fuese desarrollándose, los costes se separarían cada vez más de la línea convencional para ir acercándose al objetivo.
DiscusiónDebido al corto periodo de tiempo que lleva implantado el programa integrado resulta precipitado sacar conclusiones definitivas. A pesar de ello, los resultados de este trabajo permitieron analizar la tendencia que lleva la intervención, mostrando que la integración empezó a generar cambios en el perfil de uso de recursos de la OSI. Además, al haber realizado el análisis para cada categoría ACG se pudo empezar a evaluar el despliegue por enfermedad y especialidad. De este modo, el hallazgo del limitado cambio en la tasa de derivaciones a reumatología, traumatología y rehabilitación identificó un punto a mejorar. No obstante, hay que tener en cuenta la posibilidad de que la tasa de derivaciones fuese baja antes de la intervención, con lo que el margen de mejora sería menor. Como aspecto positivo, sí se apreció un cambio significativo en la calidad de la derivación. Descendieron las derivaciones al servicio de traumatología y parte de la carga se derivó directamente a reumatología y rehabilitación, lo que disminuyó consultas innecesarias y el tiempo que el paciente pasaba en el sistema. A nivel hospitalario la osteoporosis pasó a ser atendida casi totalmente por reumatología. Por el contrario, aunque la derivación directa de la lumbalgia a rehabilitación aumentó significativamente, su atención junto con la de las enfermedades del hombro y la rodilla siguió siendo mayoritariamente del servicio de traumatología. Se apreció también una disminución del número de consultas por episodio en la mayoría de los casos, observándose cambios significativos en la atención a los grupos patológicos de lumbalgia, hombro y rodilla. Esto se debe a que son las enfermedades en donde se trabajó más intensamente. Sobre el tema económico hay que destacar que el coste de traumatología descendió. Aunque no fue una reducción estadísticamente significativa, este es un dato a tener en cuenta, ya que es la especialidad que más carga de trabajo recibe. Por lo tanto, la valoración de los resultados obtenidos fue que el uso de rutas asistenciales ayudó a derivar mejor los pacientes a reumatología y rehabilitación a la vez que redujo las consultas sucesivas y el coste total.
En cuanto al método utilizado, la principal aportación de este trabajo fue integrar el AIP dentro del ciclo PDCA para ayudar a la planificación de la implantación del modelo integrado de atención en osteoporosis, lumbalgia, enfermedades del hombro y enfermedades de la rodilla. Como apoyo a la gestión, la simulación permitió predecir el impacto en el presupuesto de un modelo integrado que cumpliese con los objetivos planteados. Según nuestro conocimiento, este trabajo es el primer estudio en el que se utilizaron modelos predictivos para representar el proceso de atención a las enfermedades del aparato locomotor. En la literatura se pueden encontrar estudios acerca de rutas asistenciales implantadas dentro del área del aparato locomotor33,34, pero en ningún caso evaluadas mediante modelos de simulación. El uso de esta herramienta para la evaluación de servicios de salud ha sido avalado además por diferentes grupos de expertos internacionales, que a su vez han resaltado su escasa utilización31,35.
En la etapa de planificación, el AIP permitió extrapolar el consumo de recursos hasta 2020 teniendo en consideración el envejecimiento poblacional en la OSI Goierri-Alto Urola, tanto para el modelo convencional como para el modelo integrado. Aunque la integración solo intervino en 4 enfermedades, mostrar la evolución total del coste permitió visualizar que el impacto en el conjunto del aparato locomotor alcanzó el 43,9% del coste total. Puede discutirse el modo utilizado para definir los objetivos, no obstante, para que las mejoras se materialicen es necesario establecer las metas cuantitativamente. Ninguna organización puede mejorar sin una intención clara y firme para hacerlo. Por ello, el consenso alcanzado mediante el método Delphi para definir los objetivos en términos de derivaciones y consultas sucesivas ayudó en la evaluación del despliegue del modelo integrado30. Sin embargo, hay que tener en cuenta que los objetivos no se pueden conseguir de forma automática desde el primer momento, sino que su consecución será gradual36,37. De este modo, se observó que si el objetivo se consiguiera progresivamente en 5 años, generaría ahorros acumulados que superarían el millón y medio de euros para el periodo analizado.
La combinación de los resultados del AIP y del análisis estadístico permitió tener en cuenta la variable «tiempo», dando una perspectiva longitudinal al estudio18. Puede darse el caso de que en el momento en el que se realice el análisis estadístico los resultados no muestren diferencias estadísticamente significativas, pero que la tendencia de la intervención en el tiempo sea positiva. Es por ello que basar las decisiones únicamente en el análisis estadístico transversal conlleva el riesgo de abandonar una intervención que en el futuro puede ser capaz de generar mejoras relevantes, las cuales se hacen visibles al analizar la tendencia que lleva la intervención. Como se puede observar en la figura 3B, el punto referente al año 2014 se separa ligeramente de la línea que habrían seguido los costes del modelo convencional. Esto mostraba un cambio de tendencia y hacía suponer que poco a poco el modelo integrado iba generando el impacto deseado. En la misma imagen también se añade una muestra hipotética de cómo podrían evolucionar esos puntos en los próximos años. No obstante, para asegurar que las previsiones se cumplen hay que tener en cuenta las diferentes barreras que existen a la hora de implementar una intervención de atención a pacientes crónicos38,39. Estas barreras pueden generar una resistencia al cambio que dificulte la difusión y la correcta adopción del nuevo modelo36,37. Por lo tanto, el modelo integrado implica llevar a cabo un cambio cultural complejo en el que se deben adoptar nuevos roles. A este respecto, el Chronic Care Model identifica 6 áreas de mejora a la hora de promover una gestión de calidad para las enfermedades crónicas40. La intervención analizada en este trabajo incidió principalmente en 2 de ellas, la organización en la atención a la salud (Organization of Health Care) y dar soporte a la toma de decisiones (Decision Support). Como consecuencia, tanto la eficiencia del sistema de atención al aparato locomotor como la relación entre diferentes niveles asistenciales mejoró. Esta tendencia positiva tendrá que ser validada en los próximos años realizando análisis estadísticos consecutivos e integrando los resultados en el AIP. De esta forma, si los puntos se acercan cada vez más a la línea del objetivo se podrá decir que se trabaja en la línea correcta. En caso contrario, habrá que reconsiderar el despliegue y/o la intervención realizando un análisis para determinar qué está fallando. Posteriormente se podrán tomar las acciones correctoras pertinentes y empezar de nuevo el ciclo.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciaciónEste trabajo fue financiado por la Ayuda con expediente PI14/01664 de los Fondos de Investigación Sanitaria del Instituto de Salud Carlos III incluidos en el Plan Nacional de I+D+I 2008-2011 y los Fondos FEDER.
AutoríaTodos los autores cumplen los criterios de autoría y no se excluye a nadie que también los cumpla. IL, MSG y JaM diseñaron el estudio. JeM, RSV, MLJ y JA colaboraron en el diseño y aportaron el modelo conceptual y la obtención de los datos. IL, MSG y AA programaron el modelo y llevaron a cabo el análisis estadístico. IL, JaM y MSG escribieron el borrador de las secciones de introducción y discusión. AA e IL escribieron las secciones de métodos y resultados. Todos los autores revisaron los datos clínicos y epidemiológicos, aportaron comentarios en la introducción y conclusiones y aprobaron el texto final del artículo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.