El abatacept es un nuevo fármaco disponible para el tratamiento de los pacientes con artritis reumatoide (AR) refractaria. No obstante, al igual que sucede con otros tratamientos biológicos, este tratamiento no está exento de potenciales efectos adversos. A continuación se presenta el caso de una paciente de 73 años, con AR tratada con abatacept, en el que se desarrolló neumonía por Legionella pneumophila tipo 1.
Abatacept is a new drug available for refractory Rheumatoid Arthritis (RA), as other biologic therapies this drug is not free of potentially serious adverse events. We present a case of a 73 year-old patient treated with abatacept who suffered a Legionella pneumophila type 1 pneumoniae.
Los tratamientos habituales para la artritis reumatoide (AR) incluyen los tradicionales fármacos antirreumáticos modificadores de la enfermedad (FARME), como metotrexato, y agentes biológicos, como los inhibidores del TNF (tumor necrosis factor 'factor de necrosis tumoral'). A pesar de que estas opciones terapéuticas han ofrecido beneficios clínicos a muchos pacientes, una proporción significativa no responde al tratamiento anti-TNF1,2,3,4 y otros pierden la respuesta a éste con el tiempo5. Además, un grupo de pacientes presentan toxicidad medicamentosa que obliga a la suspensión del tratamiento1,2,4. Recientemente, se han introducido otros tratamientos para la población de pacientes que tiene una respuesta inadecuada al tratamiento anti-TNF6,7. Estos tratamientos tienen mecanismos de acción diferentes a los tradicionales FARME y a los agentes anti-TNF.
El abatacept es un modulador de la coestimulación soluble de origen humano, que se dirige selectivamente a la señal coestimuladora CD80/CD86:CD28, necesaria para la activación de la célula T. En el ensayo ATTAIN (Abatacept Trial in Treatment of Anti-TNF INadequate responders), se estudiaron la eficacia y la seguridad del abatacept en los pacientes con AR activa y respuesta inadecuada al tratamiento anti-TNF7. A los 6 meses, la fase doble ciego de este estudio proporcionó las primeras pruebas que apoyaban a una estrategia de tratamiento en los pacientes que no han respondido a la inhibición a TNF y que demuestran mejorías significativas tras el tratamiento con abatacept en los signos y síntomas, la función física y la calidad de vida7. Recientemente, se han presentado los hallazgos a los 2 años de tratamiento con este fármaco8 y se ha demostrado el mantenimiento de los efectos beneficiosos observados ya a los 6 meses.
Entre los efectos adversos descritos con este tratamiento, destaca la incidencia de infecciones graves (5 de cada 100 pacientes al año). Entre las infecciones más frecuentes (incidencia superior a 0,5% de los pacientes) se encuentra la neumonía lobular8.
Caso clínicoMujer de 73 años, sin hábitos tóxicos, con antecedentes de hipertensión arterial y enfermedad pulmonar obstructiva crónica de grado leve de 10 años de evolución, así como AR seronegativa desde 1980 (28 años de evolución), sin complicaciones extraarticulares. Se la había tratado desde el diagnóstico con sales de oro, antiinflamatorios no esteroideos, glucocorticoides y, secuencialmente, con leflunomida, etanercept, adalimumab e infliximab (durante 12 meses con cada uno), que se suspendieron consecutivamente por ineficacia en el control de los síntomas articulares. En el momento de la presentación del caso, la paciente recibía tratamiento con prednisolona (4mg por vía oral), metotrexato (15mg semanales) y, ante el empeoramiento de los síntomas articulares, con abatacept (hasta la fecha, había recibido 3 dosis de 750mg intravenosos, con un intervalo de 2 semanas entre éstas).
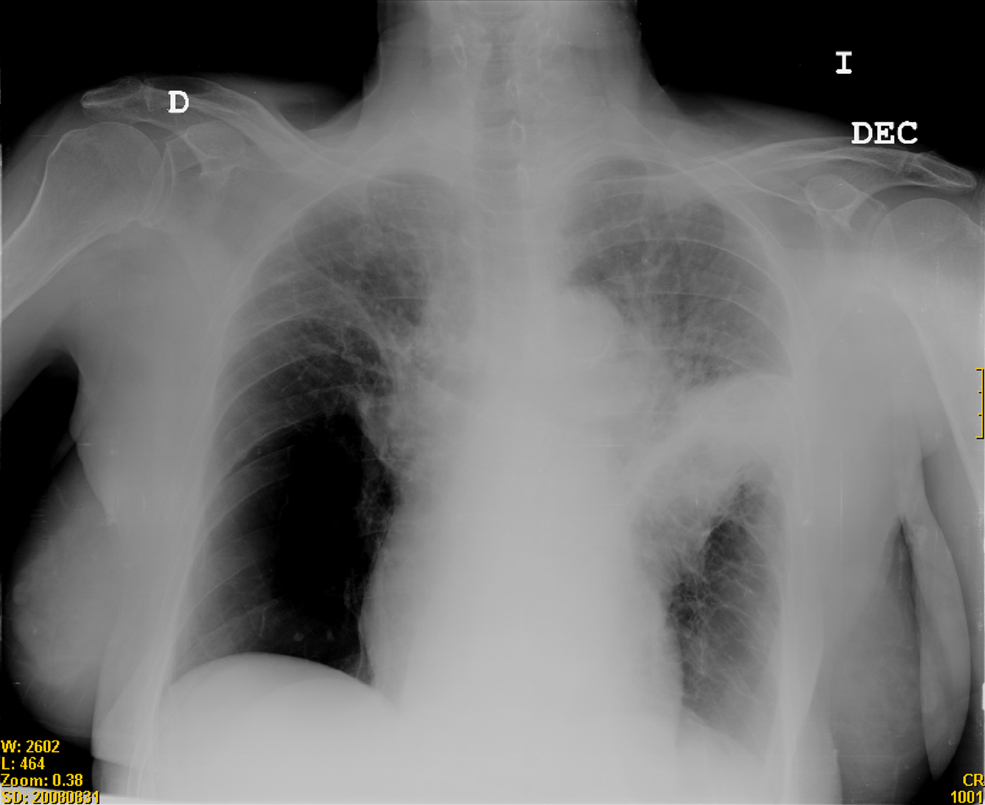
A la semana de la última dosis, la mujer comenzó con fiebre de 38°C junto con tos, expectoración purulenta y dolor pleurítico en el hemitórax izquierdo, que se fueron haciendo más intensos progresivamente, por lo que ingresó 5 días después en el hospital. En las pruebas complementarias, destacaba un recuento de 15,4×109 leucocitos (el 76% segmentados) y la radiografía de tórax (figura 1) con un extenso infiltrado alveolar en el lóbulo superior del pulmón izquierdo, que producía mínima atelectasia ipsilateral. También se apreciaba una bulla en la base del hemitórax derecho, ya presente en las radiografías previas. El antígeno de Legionella pneumophila tipo 1, recibido a los 2 días, resultó positivo, por lo que se continuó con el tratamiento iniciado empíricamente con cefotaxima y levofloxacino; a pesar de ésto, la paciente presentó un curso tórpido, con empeoramiento inicial (extensión al pulmón contralateral en las radiografías seriadas).
Figura 1. Radiografía de tórax posteroanterior de la paciente en el momento de su ingreso.
Sin embargo, tras 15 días de tratamiento con la pauta anterior, además de fisioterapia respiratoria intensiva, se le pudo dar de alta sin otras complicaciones.
DiscusiónEl tratamiento con antagonistas del TNF se asocia a un incremento del riesgo de infección, especialmente por microorganismos intracelulares9. Así, en estudios previos se han descrito infecciones por Mycobacterium tuberculosis10, Listeria monocytogenes11, Aspergillus fumigatus12, Pneumocystis jirovecii13, Histoplasma capsulatum14 o Coccidioides immitis15 tras el inicio del tratamiento con antagonistas del TNF, aunque han sido muchas menos las descripciones de casos producidos por Legionella. Así, en un registro nacional francés sobre infecciones oportunistas y graves, se recogieron durante el año 2004 sólo 10 casos de neumonía por L. pneumophila (6 pacientes tratados con adalimumab, 2 pacientes tratados con etanercept y 2 pacientes tratados con infliximab), por lo que el riesgo relativo de legionelosis entre los pacientes tratados con antagonistas del TNF se estimó entre 16,5 y 2116.
A pesar de que las complicaciones infecciosas son bien conocidas con los fármacos empleados en el tratamiento de la AR, no ocurre lo mismo con los nuevos fármacos (abatacept entre éstos). En este sentido, este caso de neumonía por Legionella asociado al tratamiento con abatacept es el primero publicado en España, lo que quizá se debe a la corta vida de este fármaco (aprobado por la Agencia Española del Medicamento en diciembre de 2007 y comercializado desde abril de 2008).
Los médicos que prescriben abatacept deben vigilar la potencial aparición de infecciones graves, como la neumonía por Legionella.