Determinar la incidencia acumulada de daño grave en órganos diana en la esclerosis sistémica con afección cutánea difusa (ESD), en una cohorte de pacientes mexicanos a los 3 años desde el inicio de los síntomas de la enfermedad, y compararla con lo observado en una cohorte de pacientes blancos.
Pacientes y métodoSe incluyó a los pacientes evaluados por primera vez en los primeros 2 años desde el inicio de los síntomas de la ESD. Se determinó la incidencia acumulada de daño grave en los siguientes órganos: piel, riñones, sistemas cardiovascular, pulmonar y gastrointestinal, y se comparó con lo observado en una cohorte donde el 94% de los pacientes son blancos, mediante la prueba de una muestra para una proporción binomial.
ResultadosSe encontró que 63 pacientes cumplían los criterios del estudio. La incidencia acumulada de daño grave en la piel fue del 3,17% (2/63) (intervalo de confianza [IC] del 95%, 0,04-11); daño renal del 4,17% (3/63) (IC del 95%, 0,99-13,29); daño cardiovascular del 1,6% (1/63) (IC del 95%, 0,04-8,5); daño pulmonar grave del 11,11% (7/63) (IC del 95%, 4,5-21,5), y daño gastrointestinal del 4,7% (3/63) (IC del 95%, 0,99-13,3). Al comparar los datos con los observados en pacientes blancos en el mismo período de evolución de la ESD, se encontró una menor incidencia de daño grave en la piel (p=0,0001), y daño renal (p=0,03) y cardiovascular (p=0,03).
ConclusionesSe determinó la incidencia de daño grave en órganos diana en pacientes mexicanos con ESD a los 3 años desde el inicio de los síntomas. La incidencia de daño de piel, y daño renal y cardiovascular es menor que lo observado en pacientes de raza blanca.
To determine the cumulative incidence of severe organ involvement in Mexican patients with systemic sclerosis (SS) and diffuse scleroderma at 3 years from the onset of SS symptoms, and to compare itwith the cumulative incidence observed in a cohort of white patients with SS.
Patients and methodPatients with SS and diffuse scleroderma were evaluated within the first 2 years from the onset of SS symptoms and were included. An estimation of the cumulative incidence of severe involvement to the skin, kidney, heart, lungs, and gastrointestinal track at 3 years from the onset of SS symptoms was carried out. This cumulative incidence was compared with that of white SS patients with diffuse scleroderma, using the one sample test for a binomial proportion.
ResultsSixty-three patients were included. The cumulative incidence of severe involvement to the skin was 3.17% (2/63) (95% CI, 0.04%-11); kidney involvement in 4.17% (3/63) (95% CI, 0.99%-13.29%); heart involvement in 1.6% (1/63) (95% CI, 0.04%-8.5%); lung involvement in 11.11% (7/63) (95% IC, 4.5%-21.5%); and gastrointestinal involvement in 4.7% (3/63) (95% IC, 0.99%-13.3%). Mexican patients had a lower Reumatol Clin. 2008;4(1):3-7 3 02 ORIG 2582 (3-7).qxp 23/1/08 11:09 Página 4 Rojas-Serrano J et al. Incidencia de daño grave en pacientes mexicanos con esclerosis sistémica incidence of severe skin involvement (P=.0001), kidney involvement (P=.03) and heart involvement (P=.03) compared to white SS patients with diffuse scleroderma.
ConclusionsThe cumulative incidence of severe organ involvement in SS Mexican patients with diffuse scleroderma was determined. The incidence of severe skin, kidney and heart involvement is lower than in white SS patients with diffuse scleroderma.
La esclerosis sistémica con afección cutánea difusa (ESD) se caracteriza por la esclerodermia proximal de codos y rodillas, así como la afección de órganos internos que puede llevar a la pérdida de su función1. Steen et al2 describieron la incidencia acumulada de daño grave a órganos diana en la ESD en la cohorte de Pittsburg, en la que el 94% de los pacientes son de raza blanca. Encontraron que la mayor incidencia acumulada de daño grave a órganos diana aparece en los primeros 3 años desde el inicio de los síntomas atribuibles a la ESD, y describieron una incidencia acumulada en ese período de daño renal del 13%, de piel del 18%, del sistema cardiovascular del 8%, del sistema gastrointestinal del 4% y un daño grave pulmonar del 8%.
Por otro lado, se han encontrado diferencias en la expresión clínica en los grupos étnicos estudiados: los pacientes afroamericanos tienen mayor frecuencia de manifestaciones inflamatorias, hipertensión arterial pulmonar, derrame pleural, miopatía, insuficiencia renal, así como fibrosis pulmonar al compararlos con pacientes de raza blanca3–5. Las diferencias en la expresión clínica entre los diferentes grupos étnicos se pueden observar incluso en los pacientes que tienen el mismo perfil de autoanticuerpos. Kuwana et al6 compararon a pacientes afroamericanos, japoneses e indígenas Choctaw, todos con antitopoisomerasa I, en sus características clínicas y serológicas. Nuevamente, los pacientes blancos tenían menor frecuencia de fibrosis pulmonar y mejores tasas de supervivencia que los demás grupos étnicos. En nuestro medio (Ciudad de México, DF), la impresión general de los médicos que atienden a pacientes con ESD es que tienen una menor incidencia de daño grave renal (crisis renales). Este estudio se llevó a cabo con el fin de determinar la incidencia acumulada de daño grave a órganos diana en pacientes mexicanos a los 3 años desde el inicio de los síntomas de la ESD, y comparar esta incidencia acumulada con lo informado en otra población2, en la que el 94% de la muestra son pacientes blancos.
Pacientes y métodoEl diseño del estudio fue de cohorte retrospectivo. La información se obtuvo de los expedientes clínicos de los pacientes evaluados en dos centros hospitalarios (Hospital General de México y Centro Médico Nacional La Raza). Se incluyó a pacientes que cumplieron con los criterios para esclerosis sistémica de la ARA7 y presentaron un patrón de afección cutánea difuso según lo propuesto por LeRoy et al8. Ambos centros hospitalarios están situados en la Ciudad de México. El primero brinda atención médica a población abierta, el segundo a población que cuenta con seguridad social. Los pacientes atendidos son mestizos mexicanos (descendientes de indígenas americanos y europeos). En ambos centros, se evalúa a los pacientes con ESD de manera estandarizada al menos cada 6 meses, y se les realiza una determinación de la escala de Rodnan modificada en cada consulta, en caso de que el paciente así lo requiera, se lo evalúa en menor tiempo de acuerdo con el criterio del médico tratante. La toma de exámenes de laboratorio y su periodicidad se decide de acuerdo con las necesidades de atención del paciente. En ambos centros, se realiza, a todos los pacientes, una espirometría y una telerradiografía de tórax cada año. Los médicos que atienden a los pacientes son reumatólogos o médicos internistas que evalúan a los pacientes en búsqueda de daño grave en órgano diana de acuerdo con las definiciones de Steen y Medsger que se describen más adelante8. Para evitar una cohorte de supervivientes, sólo se incluyó a los pacientes cuya consulta de primera vez ocurrió en los primeros 2 años desde el inicio de los síntomas de la ESD.
Recolección de la información: un médico cegado a los objetivos del estudio revisó los expedientes y recabó las variables clínicas y de laboratorio. En caso de muerte, se determinó su causa de acuerdo con el expediente y la entrevista con el médico tratante. En caso de que el paciente presentara daño grave de órgano blanco, se registró el tiempo en el que éste había ocurrido a partir del inicio de los síntomas atribuibles a la ESD.
Para definir daño grave a órgano diana, se utilizaron las mismas definiciones operacionales de Steen et al2:
- 1.
Daño grave renal (crisis renal). Se define como la presencia de hipertensión arterial maligna y/o insuficiencia renal aguda y/o anemia hemolítica microangiopática (AHM). A los pacientes con hipertensión arterial de inicio reciente, sin aumento de las concentraciones de creatinina sérica o AHM no se los clasifica como con daño renal grave, aun si fueron tratados exitosamente con inhibidores de la enzima de conversión de angiotensina.
- 2.
Daño grave cardiovascular. Se define como la presencia de cardiomiopatía con disminución de la fracción de eyección ventricular izquierda y síntomas de insuficiencia cardíaca congestiva o pericarditis sintomática con dolor pericárdico o insuficiencia cardíaca por el derrame o una arritmia atribuible al daño cardíaco por la ESD que ameritara tratamiento. Los pacientes con disminución no sintomática de la fracción de eyección ventricular, derrame pericárdico asintomático o arritmias asintomáticas no entran en la clasificación de daño cardíaco grave. Tampoco se consideró daño grave cardíaco los problemas no relacionados con la esclerodermia y los cambios no específicos en el ecocardiograma, el electrocardiograma o vigilancia con Holter.
- 3.
Daño grave pulmonar. Se define como la fibrosis pulmonar demostrada por telerradiografía de tórax y una capacidad vital forzada < 55% de lo predicho. No se incluye en esta definición la hipertensión arterial pulmonar.
- 4.
Daño grave gastrointestinal. Se define como la presencia de síndrome de absorción intestinal deficiente o episodios repetidos de obstrucción intestinal o problemas gastrointestinales graves que requieran apoyo nutricional. Los cuadros de diarrea que responden a antibióticos sin desnutrición, la plenitud abdominal posprandial y la estenosis del esófago no se clasifican como daño grave de órgano diana, a menos que se asociaran a una pérdida del 10% del peso corporal o a ingresos hospitalarios.
- 5.
Daño grave de la piel. Puntuación de la escala modificada de Rodnan > 40 de un máximo de 51.
Análisis estadístico. Las variables categóricas se describen como frecuencias y porcentajes, las numéricas como medias, desviación estándar (DE) y medianas. Se determinó la incidencia acumulada de daño grave de órgano diana a los 3 años desde el inicio de la ESD y sus intervalos de confianza (IC) del 95% con el método binomial exacto. Se comparó esta incidencia con lo informado por Steen et al2 en el mismo período desde el inicio de los síntomas de la ESD mediante la prueba de hipótesis de una muestra para una proporción binomial a una cola. Se determinó el valor de p < 0,05 como estadísticamente significativo. El análisis se efectuó con el paquete de software STATA (9.2).
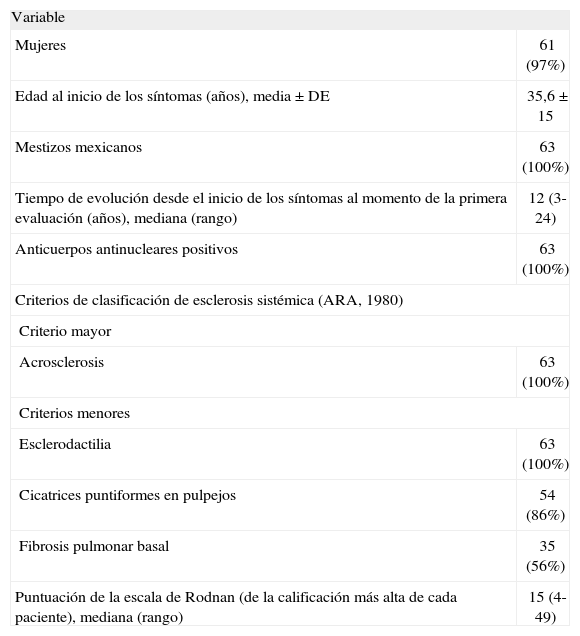
ResultadosDe 200 pacientes con diagnóstico de esclerodermia encontrados en ambos centros, 63 tenían ESD y se los había evaluado por primera vez en los primeros 2 años desde el inicio de los síntomas (tabla 1). De éstos, 61 (97%) eran mujeres, con una media de edad al inicio de los síntomas de 35,6 ± 15 (mediana, 32) años. Al momento de ser evaluados por primera vez, tenían una mediana desde el inicio de los síntomas de 12 (intervalo, 3-24) meses. La mediana de la puntuación de la escala de Rodnan modificado (de la calificación más alta de cada paciente durante todo el seguimiento) fue de 15 (intervalo, 4-49). Todos los pacientes incluidos cumplieron con los criterios propuestos por LeRoy et al8 para clasificarlos con ESD. Diez (16%) pacientes recibieron en algún momento ciclofosfamida a dosis variables, tanto por vía oral como en bolos mensuales.
Características de la cohorte del estudio (n = 63)
| Variable | |
| Mujeres | 61 (97%) |
| Edad al inicio de los síntomas (años), media ± DE | 35,6 ± 15 |
| Mestizos mexicanos | 63 (100%) |
| Tiempo de evolución desde el inicio de los síntomas al momento de la primera evaluación (años), mediana (rango) | 12 (3-24) |
| Anticuerpos antinucleares positivos | 63 (100%) |
| Criterios de clasificación de esclerosis sistémica (ARA, 1980) | |
| Criterio mayor | |
| Acrosclerosis | 63 (100%) |
| Criterios menores | |
| Esclerodactilia | 63 (100%) |
| Cicatrices puntiformes en pulpejos | 54 (86%) |
| Fibrosis pulmonar basal | 35 (56%) |
| Puntuación de la escala de Rodnan (de la calificación más alta de cada paciente), mediana (rango) | 15 (4-49) |
DE: desviación estándar.
La incidencia acumulada de daño grave de órganos diana a los 3 años desde el inicio de los síntomas de esclerodermia fue la siguiente: piel, el 3,17% (2/63) (IC del 95%, 0,04-11%); crisis renales, el 4,17% (3/63) (IC del 95%, 0,99-13,29%); daño del corazón, el 1,6% (1/63) (IC del 95%, 0,04-8,5%); daño pulmonar grave, el 11,11% (7/63) (IC del 95%, 4,5-21,5%); daño gastrointestinal, el 4,7% (3/63) (IC del 95%, 0,99-13,3%). Durante el período de evaluación, 3 (5%) pacientes fallecieron. Las causas de muerte fueron por daño grave intestinal en 2 pacientes y por crisis renal en una paciente.
Al comparar la frecuencia de daño acumulado en los primeros 3 años desde el inicio de los síntomas entre nuestros pacientes y lo informado por Steen y Medsger se encontraron diferencias estadísticamente significativas en la frecuencia de daño grave en piel, renal y cardiovascular, con menor frecuencia en los pacientes de la Ciudad de México y, por el contrario, el daño pulmonar y gastrointestinal fue más frecuente en este grupo de pacientes, esto sin alcanzar una diferencia estadísticamente significativa (tabla 2).
Comparación de las frecuencias acumuladas de daño grave de órgano diana en los primeros 3 años de la enfermedad entre pacientes mexicanos y pacientes de la cohorte de Pittsburg
| Daño de órgano diana (n = 63) | Mexicanos | Pittsburg (n = 953) | p* |
| Piel | 3,17% | 18% | 0,001 |
| Crisis renal | 4,17% | 13% | 0,03 |
| Cardiovascular | 1,6% | 8% | 0,03 |
| Gastrointestinal | 6% | 4% | 0,75 |
| Pulmonar | 12% | 8% | 0,87 |
Los resultados obtenidos en el estudio apuntan a que la frecuencia de daño grave en piel, renal y cardiovascular es menor en los pacientes mexicanos que en los pacientes de raza blanca, y a una mayor incidencia, sin ser estadísticamente significativa, de daño gastrointestinal y pulmonar.
Estos resultados hay que analizarlos en varios aspectos, el primero es en relación con el tiempo de seguimiento en ambas cohortes, si bien en el trabajo de Steen et al2 se siguió a los pacientes el tiempo suficiente para estimar la incidencia acumulada hasta los 9 años desde el inicio de los síntomas, en ese mismo trabajo se comprobó que la mayor incidencia acumulada de daño grave de órgano blanco ocurre en los primeros 3 años desde el inicio de los síntomas. De hecho, es una evidencia más que apoya el concepto por el cual se eliminó el calificativo de progresiva a la esclerosis sistémica7, ya que se sabe que la progresión de la enfermedad no es lineal y, en ocasiones, puede haber mejoría aun en pacientes no tratados9,10. De tal manera que comparar a las dos cohortes sólo durante los primeros 3 años desde el inicio de los síntomas es un concepto válido con lo que conocemos de la historia natural de la ESD.
Ambas cohortes tienen un sistema de evaluación clínica muy similar: los exámenes de laboratorio se solicitan de acuerdo con el criterio del médico tratante y los pacientes se visitan al menos dos veces por año. En ambas, si el paciente así lo requiere, tiene citas adicionales. Por otra parte, las definiciones de daño grave son clínicamente muy evidentes, todas tienen manifestaciones graves y obligan a los pacientes a buscar ayuda médica de forma inmediata, por lo que no consideramos que éste sea un factor que haya influido en los resultados obtenidos. Steen et al2 no mencionan el tratamiento de los pacientes. En nuestra cohorte el 15% de los pacientes recibieron ciclofosfamida, y se podría especular que ésta hubiera modificado la evolución y disminuido la incidencia acumulada de daño grave. El papel de la ciclofosfamida como modificador de la enfermedad es controvertido; en un ensayo clínico publicado recientemente11, en el que se comparó el uso de ciclofosfamida contra placebo para valorar el efecto en la función pulmonar en la ESD, si bien se encontró una diferencia estadísticamente significativa en la capacidad vital forzada a favor del grupo que recibió ciclofosfamida, desde el punto de vista funcional y clínico, esta diferencia fue insignificante.
Con el fin de evitar una cohorte de supervivientes y, por lo tanto, estimar de forma errónea la incidencia acumulada del daño grave de órganos diana, se incluyó sólo a pacientes que fueron evaluados por primera vez dentro de los 2 años desde el inicio de la ESD. Al utilizar este criterio de admisión, disminuyó el número total de pacientes incluidos en el estudio; sin embargo, consideramos que las cifras así obtenidas reflejan de mejor manera la incidencia acumulada del daño en la ESD en los pacientes mexicanos.
Existen importantes diferencias entre los grupos étnicos estudiados en la expresión clínica de la esclerodermia: los pacientes afroamericanos tienen mayor frecuencia de esclerodermia difusa y manifestaciones inflamatorias que los blancos3–5. Las diferencias también se han observado al comparar a blancos con otros grupos étnicos, como los “hispanos” (en su mayoría estadounidenses de origen mexicano), japoneses y tailandeses3,4,12, en este caso, los blancos también tienen menor frecuencia de enfermedad cutánea difusa y anticuerpos antitopoisomerasa I, y una mayor frecuencia de anticuerpos anticentrómero13. Las diferencias en la expresión clínica de la enfermedad se pueden observar incluso en los pacientes que tienen el mismo autoanticuerpo. Kuwana et al6 compararon a pacientes afroamericanos, japoneses e indígenas Choctaw, todos con antitopoisomerasa I, en sus características clínicas y serológicas. Nuevamente, los pacientes blancos tenían menor frecuencia de fibrosis pulmonar y mejores tasas de supervivencia. Lo anterior apoya la noción de que la ESD es una enfermedad en la que la etnia es un factor que influye de manera importante en su expresión clínica.
Hasta el momento no se han identificado factores ambientales o socioculturales que puedan explicar estas diferencias. Niert et al14 llevaron a cabo un estudio para determinar si el nivel de educación, el sexo, la duración de la enfermedad y su clasificación influían en las manifestaciones clínicas. Después de ajustar a los pacientes afroamericanos y los blancos con las variables anteriores, las diferencias entre las manifestaciones clínicas de ambos grupos étnicos persistían. Se ha postulado que los factores genéticos pueden tener un papel fundamental en la expresión clínica de la enfermedad, Arnett et al15 describieron que los indígenas de la tribu Choctaw de Oklahoma tienen una alta prevalencia de ESD, a diferencia de los indígenas Choctaw de otro estado de Estados Unidos en los que no encontraron un solo caso a pesar de compartir haplotipos HLA. La experiencia con los indígenas Choctaw apunta a que el escenario más probable es la interacción de factores ambientales y genéticos lo que determina la aparición de la ESD y su expresión clínica.
Nuestro estudio tiene las limitaciones propias de su diseño retrospectivo, además de un número pequeño de pacientes. Otra limitación del estudio es que sólo contamos con anticuerpos antinucleares en nuestros pacientes, pero carecíamos en un buen número (el 50% de los casos) de los patrones específicos de los anticuerpos, por ese motivo no incluimos este dato en el trabajo. A pesar de lo anterior, consideramos que refleja adecuadamente la incidencia acumulada del daño grave en órganos diana en esta población.
En conclusión, se determinó la incidencia acumulada a los 3 años desde el inicio de los síntomas de ESD en una población de mestizos mexicanos. La incidencia de daño grave de órganos diana es diferente de lo informado en pacientes blancos, que es menor en piel, renal y cardiovascular, y con una incidencia pulmonar y gastrointestinal semejante.