La terapia biológica ha cambiado el curso de las enfermedades reumáticas inflamatorias. La seguridad de la misma está más que documentada en diferentes estudios nacionales e internacionales. La baja frecuencia de las manifestaciones neurológicas dificulta en muchas ocasiones el establecer una relación causal clara entre el tratamiento biológico y la clínica neurológica propiamente dicha. Los síntomas y signos neurológicos que pueden aparecer son múltiples, y en ocasiones simulan enfermedades neurológicas desmielinizantes y/o neurodegenerativas. El conocimiento y el reporte de los mismos es fundamental para realizar un manejo exhaustivo de la terapia biológica en nuestros pacientes.
Biological therapy has changed the course of inflammatory rheumatic diseases. The safety is well documented in national and international studies. Neurological manifestations are uncommon and it is difficult to establish a clear causal relationship. The neurological signs and symptoms that may appear are multiple and sometimes mimic demyelinating neurological diseases and/or neurodegenerative diseases. Knowledge and disclosure of these cases is essential for a comprehensive management of biological therapy in our patients.
Desde la era de los tratamientos biológicos el pronóstico de la mayoría de las enfermedades reumáticas inflamatorias ha mejorado de forma significativa. Tanto los fármacos inhibidores de la citocina proinflamatoria factor de necrosis tumoral alfa (TNFα), como los que inhiben otras interleucinas (IL) y células que participan en el mecanismo de la inflamación, han cambiado definitivamente el curso de muchas enfermedades reumáticas crónicas.
Actualmente, la seguridad de estos fármacos a medio y largo plazo está más que documentada en diversos estudios nacionales e internacionales basados fundamentalmente en registros de pacientes que se siguen prospectivamente. Los resultados en algunos de estos son heterogéneos, ya que la muestra a estudio, la recogida de datos e incluso el análisis dista de ser similar. Sin embargo, en general todos coinciden en que las infecciones y las reacciones por hipersensibilidad son los efectos adversos más comunes.
En la actualidad, los fármacos biológicos comercializados en España son los siguientes1,2:
- 1.
Fármacos inhibidores del TNFα que pueden bloquear la molécula propiamente dicha (infliximab, adalimumab, golimumab, certolizumab) o su receptor (etanercept).
- 2.
Fármacos que inhiben otras IL: tocilizumab, inhibe la IL-6, que participa en el mecanismo de inflamación y destrucción articular; anakinra, bloquea la actividad de la IL-1 al inhibir de forma competitiva su unión al receptor IL1-R1; ustekinumab (anticuerpo monoclonal IgG1kappa que inhibe la IL-12/IL-23).
- 3.
Fármacos que interfieren en la actividad de líneas celulares: abatacept (inhibe la unión del CD28 con el CD80, bloqueando la señal de coestimulación de los linfocitos T); rituximab (depleción de los linfocitos B CD20 positivos).
En esta revisión nos centraremos fundamentalmente en los fármacos anti-TNFα debido a que del resto prácticamente no hay casos de afectación neurológica, probablemente, entre otras cosas, por el menor tiempo que llevan en el mercado. Estas manifestaciones neurológicas durante el tratamiento con fármacos biológicos son infrecuentes, pero no por ello son menos importantes. Pueden llegar, igualmente, a ser irreversibles.
Desde el inicio de su utilización hasta la actualidad se han publicado numerosos casos aislados y series de casos, aunque continúa siendo difícil establecer una causa-efecto definida3–5. El hallazgo neurológico más descrito en la literatura es la desmielinización del sistema nervioso central y/o periférico, pero hay otras también reportadas: neuritis óptica, polineuropatía aguda/crónica inflamatoria, mononeuritis múltiple y síndrome de Guillain-Barré, entre otras6–9. Todas las guías sobre el uso de terapia biológica contraindican su utilización en pacientes con esclerosis múltiple, y han de emplearse con precaución si existen antecedentes familiares.
Sin embargo, continúa el debate sobre si el tratamiento biológico puede enmascarar el desarrollo de una enfermedad desmielinizante preexistente, como la esclerosis múltiple o por otro lado, es el responsable de inducir una desmielinización de novo en el sistema nervioso central y/o periférico9.
EpidemiologíaEn estudios iniciales se reportó que el riesgo de desarrollar una enfermedad desmielinizante con el uso de terapia biológica se incrementaba un 30%10. Según el Registro español de acontecimientos adversos de terapias biológicas en enfermedades reumáticas (BIOBADASER) la incidencia es baja, entre 0,3 y 0,6 por cada 1.000 personas-año de exposición. En BIOBADASER, tras un seguimiento en 9.256 pacientes (21.425 personas-año) se han comunicado 9 casos, por lo que la tasa de enfermedad desmielinizante en pacientes tratados con anti-TNFα no fue superior a la esperada en la población general3. Los casos de enfermedad desmielinizante fueron más frecuentes en pacientes de mayor edad, varones y con diagnóstico de artritis psoriásica, aunque todos ellos sin diferencias estadísticamente significativas8.
PatogeniaEl mecanismo que conduce a que un paciente esté predispuesto a desarrollar una enfermedad desmielinizante o a una exacerbación de la misma una vez iniciado el tratamiento biológico es desconocido.
Se han propuestos varias hipótesis que apuntan a que el TNFα desempeña un papel fundamental en la patogenia de la esclerosis múltiple11. Es una citocina proinflamatoria que participa en la fase aguda de la enfermedad y en el proceso de desmielinización. Por otro lado, el TNFα también tiene unas propiedades inmunosupresoras en la segunda fase de la enfermedad. Estas propiedades están relacionadas con los receptores del TNFα (TNFR) 1 y 2, los cuales median diferentes respuestas biológicas del TNFα propiamente dicho.
En el sistema nervioso central el TNFα es producido por la microglía, astrocitos y otras células, como la proteína transmembrana precursora monomérica (tmTNF). La enzima convertidora del TNFα escinde la cola citoplasmática y libera formas solubles del TNFα (sTNF). Para llevar a cabo sus funciones biológicas las formas monoméricas de TmTNF y sTNF se deben agregar y formar homodímeros. Ambos TNF (tmTNF, sTNF) se pueden unir tanto a TNFR1 como a TNFR2; sTNF tiene mejor afinidad con el TNFR1, produciendo la respuesta inflamatoria y apoptosis. El tmTNF principalmente se une al TNFR2 y promueve la activación y supervivencia celular. En ratones transgénicos se ha investigado que la expresión aislada de tmTNF puede evitar y suprimir la progresión de encefalitis autoinmune experimental, al mismo tiempo que mantiene la autotolerancia y resistencia a la infección. Por tanto, la inhibición selectiva de la señal sTNF/TNFR1 se podría usar como una estrategia para prevenir recaídas en la esclerosis múltiple11.
Teniendo en cuenta esta teoría, se han postulado fundamentalmente 4 hipótesis para explicar una potencial relación biológica entre los antagonistas del TNF y la enfermedad desmielinizante:
- a)
Los anti-TNFα no traspasan la barrera hematoencefálica, pero mejoran la actividad mediante un aumento de las células T periféricas autorreactivas que pueden penetrar en el sistema nervioso central12.
- b)
Baja regulación de TNFR2 necesario para la proliferación de oligodendrocitos y reparación de daño12,13.
- c)
Baja regulación y producción de citocinas como la IL-10 y sobreproducción y regulación de IL-12 e IFN-γ asociado con el proceso desmielinizante14,15.
- d)
Los anti-TNFα podrían enmascarar una infección latente que a su vez podría ser crítica para iniciar un proceso autoinmune desmielinizante16.
Kaltsonoudis et al.9 realizaron un estudio prospectivo en 77 pacientes con enfermedad reumática inflamatoria (36 pacientes con artritis reumatoide, 24 pacientes con artritis psoriásica y 17 pacientes con espondilitis anquilosante) que iniciaron anti-TNFα (infliximab, adalimumab, etanercept). A todos se les realizó exploración neurológica completa, resonancia magnética nuclear craneal, de columna completa y estudio neurofisiológico antes y después de 18 meses del inicio de la terapia biológica. En el escrutinio inicial se detectó en 2 pacientes lesiones compatibles con enfermedad desmielinizante en la resonancia, por lo que se desestimó el tratamiento biológico. Al final del estudio un 4% de los pacientes (3/75) presentó afectación neurológica: neuropatía desmielinizante periférica (2 pacientes) y neuritis óptica. En todos los casos se suspendió el biológico y se trató la enfermedad neurológica. Los síntomas neurológicos remitieron en todos los pacientes9. Los autores recalcan la importancia de la resonancia y el estudio neurofisiológico para la detección precoz de afectación neurológica en este grupo de pacientes, sin embargo, solicitar estas pruebas complementarias a todos los pacientes que inician terapia biológica aumentaría de manera significativa el gasto sanitario y probablemente no sería coste-efectivo.
Formas de afectación neurológica y revisión de casosNanau et al.5 realizan una revisión sistemática de la seguridad de los inhibidores de TNFα en pacientes con enfermedades reumáticas inflamatorias5. Incluyen publicaciones de ensayos clínicos y series de casos comprendidas entre el año 2010 y 2014. La mayoría de los efectos adversos neurológicos se objetivan en pacientes con artritis reumatoide; un 50,9% en un periodo de 10 años según recogen los autores. Lo más frecuente fue la afectación del sistema nervioso central, el espectro de las enfermedades desmielinizantes, la neuritis óptica y la neuropatía periférica desmielinizante sensitiva y/o motora. El resto de eventos neurológicos, como la mielitis transversa o la leucoencefalopatía multifocal progresiva, fueron raros5,17.
En una cohorte francesa de 33 pacientes con enfermedad reumática inflamatoria y hallazgos de enfermedad desmielinizante en la resonancia, tratados con anti-TNFα durante un periodo de 3 años, 2/3 de los pacientes desarrollaron afectación del sistema nervioso central (encefalitis, mielitis transversa y neuritis óptica) y un tercio afectación periférica (polineuropatía crónica desmielinizante, síndrome de Guillain-Barré). En el examen del líquido cefalorraquídeo se objetivó: proteinorraquia (4 casos), bandas oligoclonales (11 casos), pleocitosis (4 casos). Fue normal en 6 pacientes a pesar de la afectación del sistema nervioso central. En el 90% de los casos con afectación del sistema nervioso periférico se objetivó proteinorraquia en el líquido cefalorraquídeo5,25.
Por otra parte, el diagnóstico de esclerosis múltiple propiamente dicha no es tan frecuente si tenemos en cuenta el número de veces que en la resonancia magnética nuclear se visualizan imágenes sugestivas de desmielinización26-28. En muchos casos el paciente no cumple criterios diagnósticos de esclerosis múltiple29. En una serie danesa de 550 pacientes con terapia biológica, 6 desarrollan síntomas sugestivos de enfermedad desmielinizante y 4 cumplieron criterios diagnósticos después de finalizar el estudio18. En definitiva, no toda la afectación desmielinizante será una esclerosis múltiple.
La leucoencefalopatía multifocal progresiva (LMP) es una infección subaguda del sistema nervioso central asociada a la destrucción de oligodendrocitos por el virus de John Cunningham (virus JC). La reactivación de virus JC ocurre bajo condiciones de inmunosupresión. Los síntomas incluyen confusión, alteración motora, de la coordinación, trastornos del habla y alteraciones visuales. Las convulsiones son infrecuentes. Los focos de desmielinización se pueden ver en la región occipital y parietal30,31. El diagnóstico de confirmación se obtiene cuando se identifica el virus en cultivo de líquido cefalorraquídeo o en biopsia cerebral. Así como la incidencia del virus JC en pacientes tratados con rituximab está ligeramente aumentada, en pacientes con anti-TNFα es baja, y es comparable con la de la población general31. Un total de 15 casos de virus JC se han reportado en la Food and Drug Administration Adverse Event Reporting System database32. Infliximab y adalimumab se han relacionado de manera más estrecha con la reactivación del virus JC, según la Agencia de Farmacovigilancia Canadiense y la base de datos de efectos adversos de la Organización Mundial de la Salud. Sin embargo, también hay casos con el resto de anti-TNFα32. Mejor conocida es la asociación entre rituximab y LMP, la mayoría de los casos descritos, en pacientes con artritis reumatoide23,24. No obstante, se debe tener en cuenta que el rituximab, a diferencia de otros fármacos biológicos, se utiliza para tratar otras enfermedades no reumáticas como enfermedades hematológicas y neurológicas, por tanto, este otro grupo de enfermedades también contribuiría a aumentar la prevalencia de LMP22,33-36. Otros efectos adversos relacionados con el rituximab son: la miofascitis por enterovirus, la polineuoropatía infecciosa (virus del Nilo Occidental) y la encefalitis34-36.
Por último, los síndromes bradi-acinéticos son raros. En la literatura solo hay un caso descrito de enfermedad de Parkinson de rápida instauración un año después del inicio de anti-TNFα37. No obstante, la consulta en la base de datos del Sistema Español de Farmacovigilancia sí localiza varios casos que relaciona los anti-TNFα con los síndromes parkinsonianos2. La base de datos de la OMS relaciona más de 70 casos con anti-TNFα y parkinsonismo, aunque dado que no se puede acceder a los datos, no se puede analizar si hay una relación causal clara38.
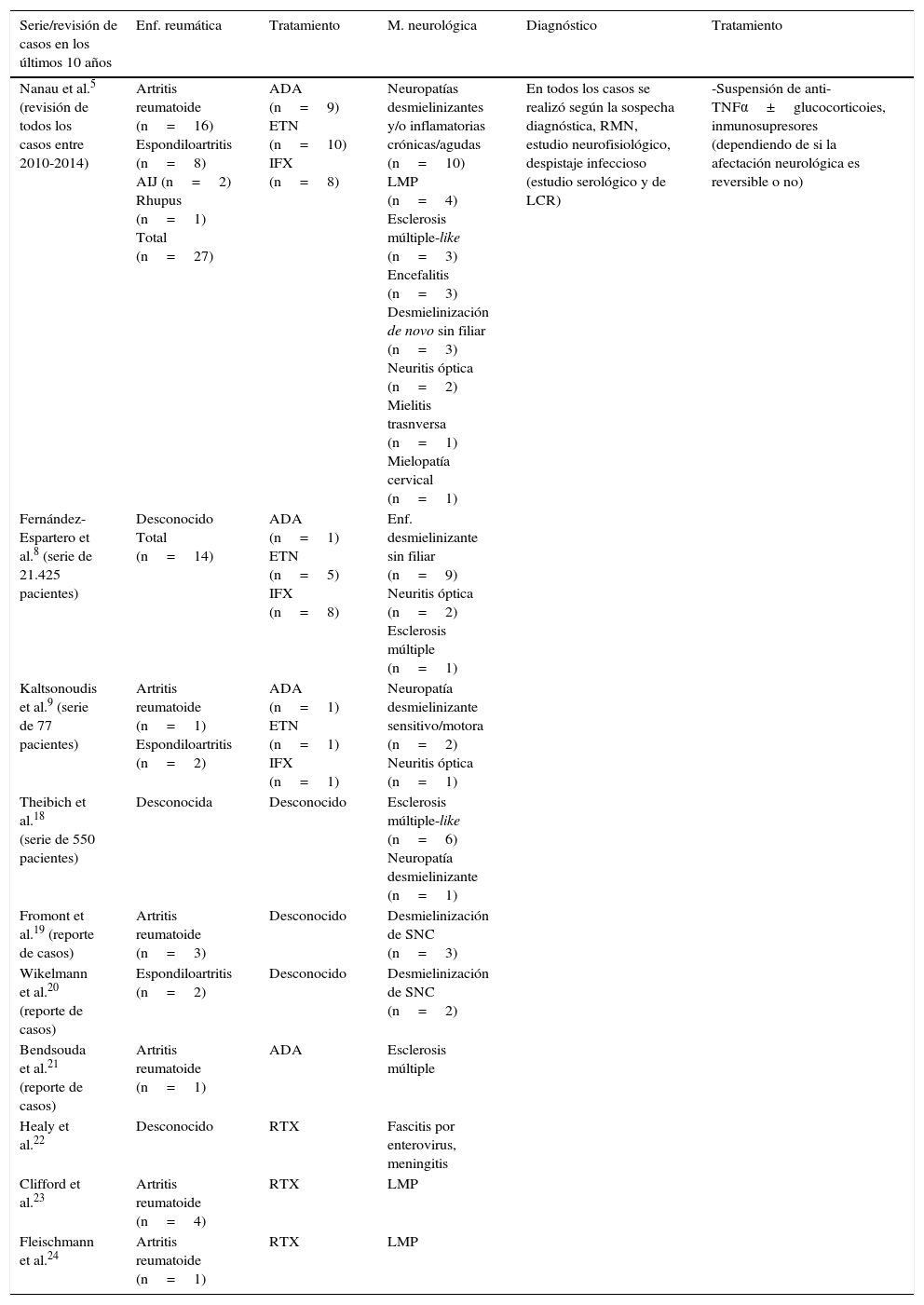
Paradójicamente, parece que puede existir una relación entre la familia de receptores del TNFα y las caspasas que participan en el desarrollo de la enfermedad de Parkinson. Está descrito que el TNFα podría ser tóxico para neuronas dopaminérgicas del mesencéfalo, que participan en el desarrollo de la enfermedad, y si esta hipótesis fuese cierta los inhibidores de TNFα serían beneficiosos y no perjudiciales. Belarbí et al.39 realizan un estudio experimental en ratas y demuestran que la inhibición de la síntesis de TNFα restablece la función neuronal y el déficit cognitivo inducido por la neuroinflamación crónica. Concluyen que la inhibición del TNFα puede ser una futura diana terapéutica en el espectro de enfermedades neurodegenerativas39. No obstante, los resultados son contradictorios, por lo que son necesarios más estudios para aclarar esta cuestión. En la tabla 1 se adjunta a modo de resumen los casos descritos en la literatura en los últimos 10 años.
Resumen de las series de pacientes con enfermedades reumáticas publicadas en los últimos 10 años
| Serie/revisión de casos en los últimos 10 años | Enf. reumática | Tratamiento | M. neurológica | Diagnóstico | Tratamiento |
|---|---|---|---|---|---|
| Nanau et al.5 (revisión de todos los casos entre 2010-2014) | Artritis reumatoide (n=16) Espondiloartritis (n=8) AIJ (n=2) Rhupus (n=1) Total (n=27) | ADA (n=9) ETN (n=10) IFX (n=8) | Neuropatías desmielinizantes y/o inflamatorias crónicas/agudas (n=10) LMP (n=4) Esclerosis múltiple-like (n=3) Encefalitis (n=3) Desmielinización de novo sin filiar (n=3) Neuritis óptica (n=2) Mielitis trasnversa (n=1) Mielopatía cervical (n=1) | En todos los casos se realizó según la sospecha diagnóstica, RMN, estudio neurofisiológico, despistaje infeccioso (estudio serológico y de LCR) | -Suspensión de anti-TNFα±glucocorticoies, inmunosupresores (dependiendo de si la afectación neurológica es reversible o no) |
| Fernández-Espartero et al.8 (serie de 21.425 pacientes) | Desconocido Total (n=14) | ADA (n=1) ETN (n=5) IFX (n=8) | Enf. desmielinizante sin filiar (n=9) Neuritis óptica (n=2) Esclerosis múltiple (n=1) | ||
| Kaltsonoudis et al.9 (serie de 77 pacientes) | Artritis reumatoide (n=1) Espondiloartritis (n=2) | ADA (n=1) ETN (n=1) IFX (n=1) | Neuropatía desmielinizante sensitivo/motora (n=2) Neuritis óptica (n=1) | ||
| Theibich et al.18 (serie de 550 pacientes) | Desconocida | Desconocido | Esclerosis múltiple-like (n=6) Neuropatía desmielinizante (n=1) | ||
| Fromont et al.19 (reporte de casos) | Artritis reumatoide (n=3) | Desconocido | Desmielinización de SNC (n=3) | ||
| Wikelmann et al.20 (reporte de casos) | Espondiloartritis (n=2) | Desconocido | Desmielinización de SNC (n=2) | ||
| Bendsouda et al.21 (reporte de casos) | Artritis reumatoide (n=1) | ADA | Esclerosis múltiple | ||
| Healy et al.22 | Desconocido | RTX | Fascitis por enterovirus, meningitis | ||
| Clifford et al.23 | Artritis reumatoide (n=4) | RTX | LMP | ||
| Fleischmann et al.24 | Artritis reumatoide (n=1) | RTX | LMP |
ADA: adalimumab; AIJ: artritis idiopática juvenil; ETN: etanercept; IFX: infliximab; LCR: líquido cefalorraquídeo; LMP: leucoencefalopatía multifocal progresiva; RMN: resonancia magnética nuclear; RTX: rituximab; SNC: sistema nervioso central. TNFα: factor de necrosis tumoral alfa.
No debemos olvidar las manifestaciones secundarias a la enfermedad reumatológica de base. Teniendo en cuenta que la mayoría de las enfermedades reumáticas tienen un componente sistémico de más o menos peso, el diagnóstico diferencial es fundamental e imprescindible. En ocasiones será difícil discernir si la afectación neurológica es de etiología farmacológica o por la propia enfermedad, incluso después de haber realizado las pruebas complementarias pertinentes. Además, la heterogeneidad de las series de casos y de los casos aislados publicados en la literatura dificulta establecer una relación causal entre el fármaco anti-TNFα y la afectación neurológica.
Recomendaciones y conclusionesSe debe valorar la interrupción del tratamiento biológico cuando el diagnóstico no es certero. Esta decisión la debe tomar el clínico, teniendo en cuenta el riesgo-beneficio de la suspensión de la terapia biológica de manera individualizada en cada paciente. En los casos de afectación neurológica grave el tratamiento estándar consiste en la administración de glucocorticoides. En pocos casos se ha requerido inmuglobulinas5,25. La remisión de la clínica neurológica no siempre es completa en todos los pacientes, incluso una vez suspendido el biológico. La decisión de reiniciarlo o no depende de la afectación neurológica en cuestión y de si se ha establecido con certeza una causa-efecto. Dicho de manera coloquial, «no todo lo que le ocurra al paciente tiene que ser por la terapia biológica». No obstante, ante cualquier duda, lo mejor es suspender el fármaco y si la enfermedad del paciente está activa, cambiar la diana terapéutica.
Para concluir, como reumatólogos debemos conocer y estar familiarizados con los efectos adversos de los tratamientos que utilizamos en nuestra práctica clínica habitual, a pesar de que sean infrecuentes. Es de suma importancia reportarlos aunque no estemos seguros de que exista una relación de causalidad. Los reumatólogos españoles tenemos la suerte de contar con el registro BIOBADASER, el cual nos aporta facilidades a la hora de revisar qué efectos debemos tener más en cuenta y la distribución de los mismos en la población española.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.