La infección por virus Chikungunya (CHIKV) presenta afectación articular en la mitad de las ocasiones. Esta afectación puede derivar en una artritis erosiva que, dada la elevada intervariabilidad en la presentación tanto clínica como serológica y el probable papel del condicionamiento genético en la gravedad y cronificación del cuadro, supone un gran reto diagnóstico y terapéutico. Existe una importante falta de evidencia científica que nos permita caracterizar la variabilidad del paciente y decidir el abordaje más adecuado.
Chikungunya virus infection (CHIKV) is associated with joint involvement in half of the cases. This can lead to erosive arthritis which, given the high intervariability of clinical and serological presentations, and the probable role of genetic conditioning in the severity and chronification of the condition, represents a great diagnostic and therapeutic challenge. There is an important lack of scientific evidence that would enable us to characterize the variability of the patient and choose the most appropriate approach.
Los alfavirus se asocian con formas inflamatorias de artritis clínicamente severas que, pueden autolimitarse o persistir en el tiempo, simulando formas persistentes de artritis no infecciosas.
El virus Chikungunya (CHIKV) es un arbovirus de la familia Togaviridae del género Alfavirus, tal y como lo son también el O’nyong-nyong virus, el Sindbis virus, el Ross river virus, el Mayaro virus, el Semliki virus o el Barmah virus. Descubierto en Tanzania en 1952, el CHIKV se ha extendido ampliamente, causando brotes masivos con inicio explosivo en la región del océano Índico. Tradicionalmente fue percibida como una enfermedad tropical hasta que se produjo un brote en Italia en 2007. La distribución de los vectores (Aedes aegypti y Aedes albopictus) es amplia, y desde finales de 2013 las infecciones por CHIKV se han difundido desde los estados del sur de Estados Unidos hasta el norte de Argentina. Estos mosquitos son los mismos responsables de la transmisión del dengue, de la fiebre amarilla, del Zika, de la fiebre del Nilo occidental, de la encefalitis japonesa y del virus de la encefalitis equina del este.
El debut típico la enfermedad cursa con fiebre elevada de 3 a 10días, añadiéndose en la mitad de pacientes dolor y/o derrame articular1 que se inicia de 2 a 5días después de la fiebre e incluye habitualmente la afectación de más de 10 articulaciones de manera simétrica, siendo manos, seguido de muñecas y tobillos, las más afectadas2,3. La participación del esqueleto axial se ha observado en algo menos de la mitad de los pacientes según las series. Los anticuerpos cítricos citrulinados (ACPA) y el factor reumatoide (FR) son típicamente negativos.
La escasa prevalencia de esta enfermedad en Europa y América del Norte hasta el momento actual ha hecho que para los reumatólogos de esta área no haya sido una patología habitual en la práctica clínica diaria. Sin embargo, el aumento de incidencia en nuestro entorno debido al incremento de viajes internacionales y el calentamiento global hacen que los casos deban ser revisados con mayor detalle.
Caso clínicoAcude a nuestro servicio a mediados de diciembre de 2014 una mujer de 40años que realiza un viaje a Cartagena de Indias a principios de diciembre de ese mismo año. Al tercer día de su llegada a Colombia debuta con escasa secreción mucosa y gingivitis, iniciando al quinto día una monoartralgia en carpo derecho que evoluciona en un día a poliartralgias bilaterales simétricas y distales que afecta ambos carpos y tobillos. Más tarde se añaden artralgias en interfalángicas proximales y distales de primer y cuarto dedo. No mialgias. Al octavo día, ya de regreso en España, realiza un episodio febricular de 37.1°C con un exantema maculopapular no confluente que respeta palmas y plantas. Analíticamente destaca una proteína C reactiva de 1,9mg/dl, linfopenia y monocitosis. Se pauta entonces tratamiento con antiinflamatorios no esteroideos (AINE) y paracetamol. Al duodécimo día se añaden sinovitis y derrame en ambos carpos y tobillos constatados por reumatólogo. La paciente niega entonces fiebre termometrada pero añade diaforesis nocturna. Al decimoctavo día debuta con un síndrome de túnel carpiano de predominio derecho. Se confirma en ese momento serología IgM positiva para CHIKV y se inicia tratamiento con 30mg de prednisona.
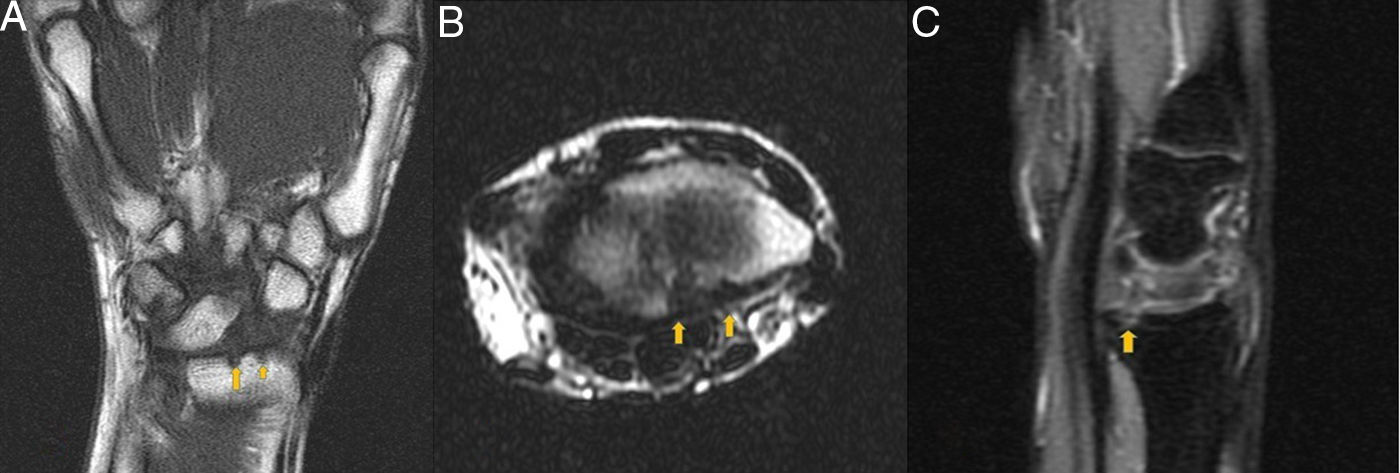
En mayo de 2015, ya sin sinovitis, persiste una limitación funcional con importante dolor asociado en carpo derecho. La resonancia magnética nuclear (RMN) de muñeca derecha de octubre de 2015, 11meses después del inicio de cuadro, muestra dos erosiones en la cara articular de la epífisis radial derecha (fig. 1). En nuestro caso, la paciente permaneció 18 meses con artritis controlada con corticoesteroides, inicialmente en pauta fija y más tarde progresivamente descendente hasta su resolución. En contexto de deseo gestacional expreso de la paciente, se descartó inicio de fármacos antirreumáticos moduladores de la enfermedad sintéticos clásicos (FAMEsc). Tras un año y medio de clínica con presencia de derrame articular se consiguieron retirar los corticoides. La paciente permanece en el momento actual sin signos clínicos ni ecográficos de artritis de ninguna articulación aunque con persistencia de dolor a la flexión extrema del carpo derecho.
DiscusiónSe ha descrito en la literatura la posibilidad de una poliartritis erosiva de muñecas, manos y tobillos1,4,5, participando en ocasiones articulaciones inusuales como las esternoclaviculares o temporomandibulares. La severidad de la sintomatología en las etapas iniciales de la infección por CHIKV podría determinar el tiempo de resolución y el riesgo de desarrollar una artritis de larga evolución1. La cronificación de la artritis debe plantear un diagnóstico diferencial para evitar la persistencia en el tiempo de una artritis que puede acabar en una destrucción articular6.
Los mecanismos que pueden llevar a la cronificación de la artritis no han sido bien establecidos. De momento, la presencia de ARN de CHIKV en líquido sinovial en la fase aguda ha sido solamente demostrada en modelos animales. Asimismo, se ha demostrado un papel central de la activación de los macrófagos de la sinovial en la inflamación articular persistente. Actualmente existe un estudio patrocinado por la Universidad George Washington que trata de demostrar la presencia de virus en líquido sinovial humano y valorar su papel en la cronificación de la artritis, así como la presencia o no del virus en suero7. La persistencia prolongada de IgM en suero podría indicar la presencia del virus en los tejidos. Sin embargo, no hay evidencia de que la persistencia del virus sea necesaria para el desarrollo de una inflamación crónica y tampoco guarda clara relación con la severidad de la enfermedad.
Una hipótesis es que, a través de mecanismos de mimetismo molecular y condicionamiento genético individual, la infección desate una reacción autoinmunitaria que condicione la aparición de una artritis crónica. Científicos indios concluyeron significativamente en 2014 que la frecuencia del alelo HLA-DRB1*11 y del haplotipo DRB1*11/DQB1*03 era inferior en los pacientes que en los controles, confiriéndoles resistencia. Asimismo evidenciaron que el haplotipo DRB1*04/DQB1*03 era significativamente más elevado en los enfermos con artritis cronificada, encontrándose el alelo HLA DQB1*04 únicamente en este grupo de pacientes. En 2010, el mismo grupo de trabajo, a partir del seguimiento longitudinal de una cohorte de 203 pacientes durante 10meses, constató que solo un 51% de los pacientes se curaron al noveno mes. Observaron que, de los que tenían dolor articular (74%), un 36% cumplían criterios del Colegio Americano de Reumatología para artritis reumatoide y testaron a 20 de estos para FR y ACPA. Todas las serologías resultaron negativas, excepto un paciente que fue ACPA positivo y en el que se demostraron signos de destrucción articular por RMN1,8.
Si revisamos los datos del brote del año 2006 en la Isla de Reunión, vemos que la mayoría de los pacientes jóvenes se recuperaban, siendo la prevalencia de la persistencia claramente mayor en las personas de más de 60años, quienes además tenían una carga viral más elevada. Se demostró la instauración rápida de una respuesta innata con incremento de la activación de la células NK y los linfocitos CD4 y CD8, seguida de una respuesta débil de la citoquinas Th1/Th2, así como altos niveles de IFN-alfa9.
Están descritos casos en la literatura en los que una artritis crónica prosigue a una infección por CHIKV. Algunos de estos pacientes, a pesar del origen postinfeccioso, se han tratado con FAMEsc dada naturaleza crónica de la afección, con buenos resultados. Hay que destacar que la eficacia de los FAMEsc en esta indicación no ha sido correctamente evaluada. Investigadores franceses han postulado que la resistencia o la dependencia de corticoides más allá de los 3meses serían altamente sugestivas de cronificación10.
En la actualidad, el tratamiento es fundamentalmente de soporte, incluyendo antiinflamatorios. Los antivirales y la cloroquina no han demostrado eficacia y, de momento, no hay vacuna disponible. En formas crónicas y pacientes seleccionados, los corticoesteroides, el metotrexato y otros agentes inmunomoduladores pueden ser de utilidad10,11.
ConclusiónLa producción científica dirigida a este tema es limitada y la evidencia en todos los aspectos es escasa. Aunque las artritis por CHIKV son autolimitadas y leves en algo más de la mitad de las ocasiones, en algunas de las series hasta el 49% de los pacientes se cronifican más de 9meses, causando en ocasiones destrucción articular1. Se desconoce si la instauración precoz de tratamiento tendría un papel en la disminución de la probabilidad de sufrir erosiones. El diagnóstico es serológico; la IgM se presenta desde el primer hasta el duodécimo día después del inicio de los síntomas, y la IgG, a partir del segundo mes, siendo posible que persista elevada durante años. Se debe tener en cuenta que es posible que existan reacciones cruzadas de laboratorio o producirse una coinfección, puesto que comparte vector con el dengue. La evolución serológica y clínica es altamente variable y el condicionamiento genético podría jugar un papel fundamental en la etiopatogenia de la cronificación. La infección genera anticuerpos que protegen a la persona de por vida.
FinanciaciónNo hay fuentes de financiación, toda la información se ha obtenido de la práctica clínica habitual.
Conflicto de interesesTodos los autores declaran no tener conflictos de interés para este artículo.
A todos nuestros compañeros del Servicio de Reumatología y de la Sección de Radiología Musculoesquelética por su apoyo y por hacernos las cosas más fáciles cada día.