Elaborar recomendaciones para la prevención de infección en pacientes adultos con enfermedades reumáticas autoinmunes sistémicas (ERAS).
MétodosUn panel de expertos, seleccionados con base en su currículum y experiencia, identificó preguntas clínicas de investigación relevantes para el objetivo del documento. Se realizaron revisiones sistemáticas de la evidencia, que se graduó de acuerdo con los criterios del Scottish Intercollegiate Guidelines Network. Tras ello, se formularon las recomendaciones.
ResultadosSe seleccionaron cinco preguntas, referentes a la prevención de infección por Pneumocystis jirovecii con trimetoprim-sulfametoxazol, medidas profilácticas contra el virus de la hepatitis B, vacunación contra el virus del papiloma humano, vacunación contra el Streptococcus pneumoniae y vacunación contra el virus de la gripe. Se formularon un total de 18 recomendaciones, estructuradas por pregunta, con base en la evidencia encontrada para las diferentes ERAS y/o consenso de expertos.
ConclusionesExiste suficiente evidencia sobre la seguridad y eficacia de las vacunaciones y otras medidas profilácticas frente a los microrganismos revisados en este documento como para ser recomendadas específicamente en pacientes con ERAS.
To develop recommendations for the prevention of infection in adult patients with systemic autoimmune rheumatic diseases (SARD).
MethodsClinical research questions relevant to the objective of the document were identified by a panel of experts selected based on their experience in the field. Systematic reviews of the available evidence were conducted, and evidence was graded according to the Scottish Intercollegiate Guidelines Network criteria. Specific recommendations were made.
ResultsFive questions were selected, referring to prevention of infection by Pneumocystis jirovecii with trimethoprim/sulfamethoxazole, primary and secondary prophylactic measures against hepatitis B virus, vaccination against human papillomavirus, vaccination against Streptococcus pneumoniae and vaccination against influenza virus, making a total of 18 recommendations, structured by question, based on the evidence found for the different SARD and/or expert consensus.
ConclusionsThere is enough evidence on the safety and efficacy of vaccinations and other prophylactic measures against the microorganisms reviewed in this document to specifically recommend them for patients with SARD.
La infección grave es una de las principales causas de morbimortalidad en pacientes con enfermedades reumáticas autoinmunes sistémicas (ERAS)1–4. En el lupus eritematoso sistémico (LES), una de las ERAS más prevalente, se estima que la mortalidad secundaria a infección es hasta cinco veces mayor que en la población general5. Aunque muchos de los factores de riesgo de infección se comparten con la población general, existen factores específicos de las ERAS, como factores genéticos o las características inherentes a la enfermedad y sus tratamientos6–9. El riesgo de infección grave no es uniforme en todas las ERAS, siendo menos frecuente en el síndrome de Sjögren primario (SSp) que en el LES10. Respecto a los tratamientos, los inmunosupresores (IS) y los glucocorticoides (GC) son factores de riesgo de infección bien conocidos6. Las terapias dirigidas, tanto biológicas, como pequeñas moléculas, aunque tienen dianas moleculares muy específicas, pueden alterar la respuesta inmune frente a infecciones, e interferir con el control de estas. Esto es especialmente relevante en las terapias dirigidas contra los linfocitos B, como el rituximab (RTX)11. Por otra parte, el control del proceso inmunopatogénico de la enfermedad con estas terapias podría, a su vez, reducir el riesgo de infección intrínseco a las ERAS12.
La prevalencia de infecciones prevenibles en las ERAS no está bien investigada, aunque la mayoría de los estudios sugiere que es mayor que en la población general para el virus de la influenza, Streptococcus pneumoniae, virus del herpes zoster (VHZ) y virus del papiloma humano (VPH)13. Algunas infecciones, como el S. pneumoniae y el VPH, parecen ser más comunes en las ERAS, especialmente en el LES, que en las artropatías inflamatorias crónicas, después de ajustar por el nivel de inmunosupresión 9,13,14. Asimismo, la prevalencia del VHZ parece ser mayor en algunas ERAS, como las miopatías inflamatorias (MI) o la arteritis de células gigantes (ACG)13. Aunque la información sobre otros virus, como el de la hepatitis B (VHB) o el virus de la hepatitis C (VHC), es escasa, la prevalencia de ambas parece ser similar o incluso menor en las ERAS que en población general6,15,16.
La mayoría de las infecciones graves en pacientes con ERAS son causadas por microorganismos comunes, en localizaciones habituales2,10. Sin embargo, existen infecciones oportunistas, como la infección por Pneumocystis jirovecii (PCj), especialmente en pacientes tratados con dosis altas de GC u otras formas de inmunosupresión intensa17–19. En el estudio más amplio publicado hasta el momento, realizado en Taiwán en 76.966 personas con ERAS y artritis reumatoide (AR), el riesgo de infecciones oportunistas fue más alto durante el primer año tras el diagnóstico, mayor en las MI, seguidas del LES, esclerosis sistémica (ES), AR y SSp20.
Se ha descrito mayor gravedad y letalidad de algunas infecciones, como las producidas por S. pneumoniae o por virus de la influenza en pacientes inmunocomprometidos con ERAS21–23. Por último, un evento infeccioso puede desencadenar brotes de actividad de la enfermedad en las ERAS24–27.
Justificación de recomendaciones específicas para ERASLas ERAS son un grupo de enfermedades complejas y con frecuencia graves, que comparten mecanismos y tratamientos que comprometen la respuesta inmune, siendo frecuentes las infecciones graves. La mortalidad por infección es, además, mayor que en otras enfermedades reumáticas inmuno-mediadas, por lo que la prevención de infecciones debería ser un objetivo ineludible, constituyendo un desafío para los clínicos implicados en su manejo.
La evidencia disponible acerca de la incidencia y la prevención de las infecciones en ERAS, así como sobre la inmunogenicidad y la seguridad de las vacunas, u otras medidas profilácticas en pacientes con estas enfermedades es muy limitada13,28. Por este motivo, es pertinente desarrollar recomendaciones específicas para las ERAS, basadas en la mejor evidencia disponible y en la opinión sistematizada de grupos de expertos multidisciplinares.
Existen recomendaciones de la European League Against Rheumatism (EULAR), recientemente actualizadas, sobre la vacunación en pacientes con enfermedades reumáticas inmuno-mediadas29, pero la amplitud de los objetivos planteados condiciona que la extensión con la que se tratan las peculiaridades propias de las ERAS resulte insuficiente, quedando cuestiones sin responder. Además, al analizar únicamente las enfermedades prevenibles con vacunas, se excluyen aspectos particularmente relevantes en las ERAS, como el caso de la quimioprofilaxis de la infección por PCj30,31, o la prevención de la reactivación de la hepatitis B32.
ObjetivoDesarrollar recomendaciones específicas para la prevención de infección en pacientes adultos con ERAS, apoyadas en revisiones sistemáticas (RS) y/o consenso de expertos, en aquellas preguntas consideradas prioritarias por el grupo de panelistas, en función de su repercusión clínica, las peculiaridades de cada infección en las ERAS y la disponibilidad de recursos.
MétodosEn el desarrollo de estas recomendaciones, se ha utilizado una síntesis cualitativa de la evidencia científica y técnicas de consenso, que recogen el acuerdo de expertos en función de la evidencia disponible y de su experiencia clínica.
El proceso para el desarrollo del proyecto ha sido el siguiente:
- 1.
Se constituyó un panel de expertos formado por seis reumatólogos, dos especialistas en enfermedades infecciosas y uno en medicina preventiva. La coordinación fue realizada por dos reumatólogos y dos especialistas en metodología de la Unidad de Investigación de la Sociedad Española de Reumatología (UI-SER).
- 2.
Se definieron los contenidos y aspectos clave del documento, planteándose las preguntas clínicas de investigación con más impacto en la práctica clínica. Las preguntas se reformularon en formato paciente, intervención, comparación, outcome o desenlace (PICO).
- 3.
Se realizó una búsqueda de la evidencia científica publicada hasta abril del 2019. Para ello, se utilizaron las bases de datos PubMed (MEDLINE), EMBASE, y Cochrane Library (Wiley Online). El proceso se completó con una búsqueda manual en las referencias de los estudios identificados. Las estrategias de búsquedas bibliográficas de las RS pueden consultarse en el material suplementario.
- 4.
Reumatólogos expertos en revisión de la evidencia de la SER llevaron a cabo las RS y la síntesis de la evidencia científica. Se evaluó el nivel de la evidencia científica, utilizando los criterios del Scottish Intercollegiate Guidelines Network (SIGN)33.
- 5.
El grupo de expertos formuló las recomendaciones, basándose en la evaluación formal o «juicio razonado», de la evidencia, para cada una de las preguntas. Se tuvo en cuenta la calidad, cantidad y consistencia de la evidencia científica, la generalidad de los resultados, su aplicabilidad y su impacto clínico. Para aquellas cuestiones en las que la evidencia no era suficiente, se formularon recomendaciones basadas en el consenso del grupo de expertos. Para la formulación de estas se utilizaron dos rondas de consenso; primero, con el sistema de consenso de «juicio razonado», todos los expertos redactaron y discutieron las recomendaciones. Después, en presencia de los metodólogos, mediante la técnica modificada de consenso nominal se estableció el grado de acuerdo entre los expertos con el contenido y la redacción de cada una de las recomendaciones. La graduación de estas últimas se realizó con el sistema de SIGN33 (Anexo).
- 6.
El borrador del documento se sometió a revisión externa, para asegurar la validez y exactitud de las recomendaciones y, posteriormente a exposición pública, con el propósito de que otros socios de la SER y distintos grupos y entidades potencialmente interesadas pudieran evaluar el documento y formular las apelaciones o sugerencias.
La información completa sobre los resultados obtenidos de la revisión de la evidencia para cada pregunta de investigación está disponible en la web de la SER (www.ser.es).
Consideraciones generales previasEs conveniente resaltar que las recomendaciones desarrolladas en este documento deberían enmarcarse en una estrategia global de gestión de riesgo de infección en las ERAS.
En primer lugar, para afrontar la prevención de infecciones en estas enfermedades, es esencial realizar una estimación del riesgo individual de infección, que incluya el registro de eventos infecciosos graves previos y la presencia de infecciones virales crónicas (virus de la hepatitis, VIH o VPH) o tuberculosis latente. El hacer recomendaciones sobre las estrategias de cribado de infección en ERAS excede los objetivos de este documento, siendo aplicables las recomendaciones generales para pacientes inmunocomprometidos o las que se deriven del uso de fármacos específicos como las terapias biológicas o dirigidas. En la estimación del riesgo de infección, deben considerarse factores como edad, etnia, tipo de ERAS, consumo de tabaco, comorbilidades, gravedad de enfermedad, tratamientos activos, daño acumulado etc., ya que todos ellos condicionan el nivel de riesgo17,19. Es también imprescindible recoger la historia vacunal de la forma más precisa y fiable posible (vacunas administradas hasta la fecha, valencias, dosis, booster, ubicación en el tiempo, etc.), o de profilaxis de tuberculosis previamente completada. La determinación de subpoblaciones linfocitarias y/o inmunoglobulinas debe considerarse en caso de sospecha de disminución, a consecuencia del tratamiento o de la propia ERAS.
La prevención de la reactivación de la infección latente por Mycobacterium tuberculosis no ha sido abordada en este documento, por considerarse adecuadamente revisada en recomendaciones recientes, emitidas por otros grupos34,35.
Deben fomentarse, de manera proactiva, medidas generales de higiene corporal y bucodental36, así como evitar tabaquismo o contactos con pacientes con enfermedades infecciosas activas potencialmente graves. La adecuada cumplimentación de los programas de vacunación en convivientes puede contribuir a reducir riesgos derivados de la exposición a agentes infecciosos en el entorno, de acuerdo con la denominada «estrategia de capullo» (cocoon vaccination strategy)37. Consejos específicos en caso de viajes a áreas geográficas con riesgos especiales pueden resultar críticos en términos de protección.
El grupo de panelistas sugiere la implementación de programas estructurados de educación por parte de enfermería entrenada, donde este tipo de recurso esté disponible, dada la eficacia de estos programas en el fomento de la vacunación38,39, siempre en colaboración con los servicios de Medicina preventiva.
Cabe recordar aquí que la optimización o «ajuste fino» del tratamiento IS, minimizando la dosis de GC, es una medida ampliamente admitida, sobre la que existe acuerdo en práctica clínica. En este sentido, conviene recordar que una dosis diaria de prednisona (o equivalente) igual o superior a 7,5 mg, se ha asociado a mayor riesgo de infección grave en pacientes con LES40. Por otro lado, los antipalúdicos han sido relacionados, de forma consistente, con una reducción del riesgo de infección grave en pacientes con LES17,41, disminuyendo también la mortalidad asociada a la misma42. Recientemente, incluso se ha sugerido que su uso continuado podría reducir la incidencia de neumonía por PCj43.
El panel cree conveniente puntualizar que las sugerencias contenidas en este apartado de consideraciones generales previas no se han sometido a la revisión de evidencia ni a la metodología estandarizada de consenso de expertos seguida en el desarrollo del documento. Por último, para las situaciones en las que no se ha revisado la evidencia, el panel de expertos se remite a las recomendaciones EULAR de vacunación en enfermedades reumáticas inmuno-mediadas, recientemente actualizadas29, al consenso de la SER de gestión de riesgo de tratamiento con terapias biológicas en enfermedades reumáticas44 y a las recomendaciones desarrolladas por otros grupos para pacientes inmunocomprometidos45, sin desoír las establecidas para la población general, cuando sean aplicables.
Terminología- -
Inmunogenicidad: capacidad de las vacunas de inducir una respuesta inmunológica medible.
- -
Seroconversión: incremento en el título de anticuerpos tras la administración de una vacuna, hasta hacerse detectable en su medición o incrementarse en un nivel predeterminado respecto a los niveles previos.
- -
Seroprotección: evidencia serológica de inmunidad frente a una enfermedad infecciosa, que iguala o supera el umbral de correlación inmunitaria de protección.
- -
Serorreversión: pérdida de la protección inmunológica proporcionada por una vacuna con el transcurso del tiempo.
- -
Concentraciones medias geométricas (CMG): medida del título promedio de anticuerpos generados por una vacuna en un grupo de individuos.
Se han formulado un total de 18 recomendaciones que abordan el uso de trimetoprim-sulfametoxazol como profilaxis frente al PCj, las medidas profilácticas primarias y secundarias frente al VHB y la vacunación frente al VPH, el S. pneumoniae y el virus de la gripe (tabla 1).
Recomendaciones SER sobre prevención de infección en ERAS
| Recomendaciones | G R |
|---|---|
| Trimetoprim-sulfametoxazol como profilaxis frente al Pneumocystis jirovecii | |
| Recomendación:se recomienda la profilaxis de la infección por Pneumocystis jirovecii con trimetoprim-sulfametoxazol en los pacientes con ERAS tratados de forma continuada con glucocorticoides (≥ 20 mg/día). No se puede establecer un tiempo mínimo de tratamiento con glucocorticoides a partir del cual esté indicada la profilaxis.Recomendación:independientemente del tratamiento inmunosupresor, en cualquier paciente con recuento sostenido de linfocitos T CD4+ inferior a 200/mm3, se recomienda también la profilaxis contrimetoprim-sulfametoxazol.Recomendación:se recomienda utilizar la dosis de trimetoprim-sulfametoxazol de 400 mg/80 mg/día, ya que es la pauta mejor documentada, en términos de seguridad y eficacia, en la profilaxis de la infección por Pneumocystis jirovecii en pacientes con ERAS.Recomendación:en tratamientos con trimetoprim-sulfametoxazol superiores a un mes de duración, se recomienda suplementar con ácido fólico. | B√C√ |
| Medidas profilácticas primarias y secundarias frente al virus de la hepatitis B | |
| Recomendación: en pacientes con LES o con enfermedad de Behçet, se recomienda la vacunación frente al virus de la hepatitis B, con 3 dosis de vacuna recombinante (20 μg de HBsAg purificado) en la fase inactiva o de baja actividad y sin tratamiento inmunosupresor.Recomendación: en pacientes con otras ERAS, se sugiere aplicar las recomendaciones expuestas anteriormente. Aunque no hay evidencia directa, se considera que este grupo de pacientes tiene suficientes similitudes con el LES como para extrapolar la recomendación.Recomendación: en todos los pacientes con ERAS que estén en situación de inmunosupresión (por tratamiento previo o actual), se sugiere considerar pautas vacunales con 4 dosis y/o con mayor carga antigénica (40 μg de HBsAg purificado)Recomendación: se recomienda verificar la respuesta vacunal frente a hepatitis B al completar la pauta indicada, mediante determinación de niveles de anticuerpos frente a antígeno de superficie (anti-HBsAg), 1 mes después de la vacunación.Recomendación: en todos los pacientes con ERAS con infección crónica por VHB y que vayan a recibir tratamiento inmunosupresor, terapia biológica (especialmente anti-CD20) o glucocorticoides (prednisona o equivalente ≥ 20 mg/día durante 4 semanas), se recomienda el tratamiento concomitante con antivirales, preferentemente entecavir 0,5 mg/día, debido a la elevada tasa de resistencia a lamivudina, para prevenir la reactivación de la infección por VHB. | D√√√√ |
| Vacunación frente al virus del papiloma humano | |
| Recomendación:en todos los pacientes con ERAS se deben seguir las recomendaciones de vacunación del VPH indicadas en población general, esto es:1. Se recomienda vacunación universal para niñas, idealmente a los 12 años de edad.2. En pacientes mayores de edad con tratamiento excisional de cérvix y/o síndrome de WHIM (verrugas, hipogammaglobulinemia, infecciones y síndrome de mielocatexis), así como en menores de 26 años en situación de prostitución, infección por VIH y hombres que practican sexo con hombres.Recomendación: en pacientes adultos con ERAS, especialmente con LES que no estén incluidos en los grupos anteriores, la decisión de vacunar se debe individualizar, considerando el riesgo previo de exposición al virus del papiloma y el riesgo de contacto futuro con el virus.Recomendación:se recomienda administrar la vacuna antes del inicio de la inmunosupresión y en los períodos de remisión o baja actividad de la enfermedad para evitar el efecto potencial de los inmunosupresores en la respuesta vacunal. | DD√C |
| Vacunación frente al Streptococcus pneumoniae | |
| Recomendación: se recomienda vacunar frente al Streptococcus pneumoniae a todos los pacientes con ERAS ya que, aunque confiere una inmunogenicidad discretamente menor en comparación con individuos sanos (especialmente en pacientes con LES), es suficientemente efectiva y segura.Recomendación: se recomienda administrar la vacuna antes del inicio de la inmunosupresión, particularmente si esta es con rituximab y en períodos de remisión o baja actividad de la enfermedad, para evitar que el uso de inmunosupresores pueda disminuir la respuesta vacunal.Recomendación: como esquema de vacunación en pacientes con ERAS se recomienda el utilizado en la población general, consistente en la estrategia secuencial, iniciando con una dosis de vacuna conjugada y continuando con otra de la vacuna polisacárida (o no conjugada), un mínimo de 2 meses después. | BC√ |
| Vacunación frente al virus de la gripe | |
| Recomendación:en pacientes con LES, se recomienda la vacunación frente al virus de la gripe, con la vacuna de las cepas AH1N1, AH3N2 y virus de la influenza B, preferiblemente con adyuvante.Recomendación:en pacientes con otras ERAS diferentes al LES, se sugiere aplicar la recomendación expuesta anteriormente. Aunque no hay evidencia directa, se considera que este grupo de pacientes tiene suficientes similitudes con los pacientes con LES, como para poder extender la recomendación.Recomendación:en pacientes con ERAS se sugiere el empleo de una segunda dosis de refuerzo, al cabo de 3-4 semanas de la primera, en las siguientes circunstancias:Uso de fármacos inmunosupresoresTratamiento con rituximab en los 3 meses previos. | BCC |
ERAS: enfermedades reumáticas autoinmunes sistémicas; LES: lupus eritematoso sistémico; GR: grado de recomendación (Anexo).
En pacientes con ERAS tratados con GC u otros medicamentos con efecto inmunosupresor, ¿cuál es la eficacia o efectividad y la seguridad del trimetoprim-sulfametoxazol como profilaxis frente al PCj?
Recomendación: se recomienda la profilaxis de la infección por PCj con trimetoprim-sulfametoxazol en los pacientes con ERAS tratados de forma continuada con GC (≥20 mg/día). No se puede establecer un tiempo mínimo de tratamiento con GC a partir del cual esté indicada la profilaxis (recomendación de grado B).
Recomendación: independientemente del tratamiento inmunosupresor, en cualquier paciente con recuento sostenido de linfocitos T CD4+ inferior a 200/mm3, se recomienda también la profilaxis con trimetoprim-sulfametoxazol (recomendación de grado √).
Recomendación: se recomienda utilizar la dosis de trimetoprim-sulfametoxazol de 400 mg/80 mg/día, ya que es la pauta mejor documentada, en términos de seguridad y eficacia, en la profilaxis de la infección por PCj en pacientes con ERAS (recomendación de grado C).
Recomendación: en tratamientos con trimetoprim-sulfametoxazol superiores a un mes de duración, se recomienda suplementar con ácido fólico (recomendación grado √).
La neumonía por PCj es una infección oportunista frecuente en los pacientes inmunodeprimidos46. Puede causar insuficiencia respiratoria y, en casos graves, la muerte, tanto en pacientes VIH como no VIH. Sin embargo, en el primer grupo, el tratamiento anti-retroviral y el uso frecuente de profilaxis frente a PCj ha disminuido considerablemente la tasa de infección y la mortalidad por este microorganismo a lo largo de los años47,48. La incidencia de infección por PCj en pacientes con ERAS se considera por lo general, muy baja49. Por otra parte, no se dispone de datos suficientes para establecer con fiabilidad qué pacientes tienen más riesgo de desarrollar esta infección, aunque sí está bien definido que los GC a dosis moderada-altas constituyen un claro factor de riesgo independiente50–52. Aunque se ha descrito mayor predisposición a infección por PCj en pacientes con determinadas ERAS, los estudios son de calidad limitada, al ser retrospectivos y tener factores de confusión, como puede ser la inmunosupresión asociada y el tiempo de tratamiento. Por otro lado, múltiples estudios han demostrado que la evolución de la infección es peor en pacientes inmunodeprimidos no VIH, como pueden ser aquellos con ERAS, y que el uso de tratamiento IS contribuye de manera significativa al riesgo de infección48,53,54. No obstante, de acuerdo con los resultados de un estudio, llevado a cabo en EE. UU., el porcentaje de reumatólogos que prescriben profilaxis para PCj en situaciones de riesgo es sub-óptimo y hasta un 30% de los encuestados reconocieron no realizarla nunca55.
Aunque de la RS llevada a cabo para esta recomendación se puede concluir que la intervención reduce el riesgo de neumonía por PCj, no se identificó ningún ensayo clínico aleatorizado (ECA) que comparase profilaxis con cotrimoxazol (TMT/SMX) vs. placebo. Un estudio de casos y controles, ajustando para un propensity score, mostró que la quimioprofilaxis fue eficaz disminuyendo no solo la incidencia de neumonía por PCj sino también la mortalidad (HR 0,08 [IC 95% 0,0006 a 0,71]) (nivel evidencia 2+)56.
Respecto a la dosis de TMT/SMX usadas para la quimioprofilaxis de PCj, un ECA evaluó la eficacia de dosis de TMP-SMX por debajo de la dosis estándar de 400 mg/80 mg diarios; se concluyó que la dosis de 200 mg/40 mg diarios era igualmente eficaz como profilaxis, con menor tasa de eventos adversos (EA) leve-moderados, además de menor tasa de abandonos57 (nivel de evidencia 1+). Un estudio retrospectivo sugiere que la pauta con «escalada de dosis» (iniciando tratamiento con un 10% de la dosis 400 mg/80 mg de TMP-SMX e incrementándola en días sucesivos hasta alcanzar el 100%) puede ser igual de efectiva pero con menor tasa de abandonos58 (nivel de evidencia 3). Otros estudios indican que pautas profilácticas de dos o tres veces a la semana pueden ser también efectivas y provocar menos suspensiones y EA50,59, aunque el alto riesgo de sesgo de estos estudios hace que se deba ser prudente a la hora de establecer una recomendación sustentada en ellos (nivel de evidencia 1-3). Para responder a esta cuestión serían necesarios nuevos ensayos, que comparen la pauta diaria con aquellas de menor frecuencia semanal a igual dosis. Por todo lo expuesto, dada la ausencia de presentaciones de 200 mg/40 mg en nuestro medio, el grupo elaborador se inclina por recomendar la dosis de 400/80 mg diaria. De cualquier modo, en caso de toxicidad no grave, se podría recurrir a regímenes con menor dosis TMT/SMX.
Un estudio encontró mayor tasa de EA en pacientes con LES y enfermedad mixta del tejido conectivo (EMTC)60 (nivel de evidencia 3). Los resultados de uno de los estudios revisados sugirieron que, a mayor dosis de GC, mayor probabilidad de beneficiarse de la profilaxis frente a PCj, en términos de un mejor balance n.° necesario a tratar/n.° necesario para dañar (NNT/NNH)56 (nivel de evidencia 2+).
En los diferentes estudios que han evaluado la seguridad de TMP-SMX, los EA más frecuentes son elevación de transaminasas, erupción cutánea, trombocitopenia, fiebre58,60, taquicardia y alteraciones electrolíticas51,56,57,59,61. Los EA más graves son insuficiencia renal aguda, trombocitopenia y síndrome de Stevens Johnson56–59,61.
No se han encontrado datos que permitan concluir cuándo es el momento idóneo para iniciar la profilaxis en pacientes con ERAS. Si se extrapolan los datos y recomendaciones de expertos de otros grupos de pacientes inmunodeprimidos, se sugiere iniciar profilaxis cuando el recuento de CD4 sea < 200/mm362,63. Respecto a la duración de la profilaxis, idealmente se debe mantener mientras el paciente se considere de riesgo, esto es, mantenga dosis elevadas de prednisona o el recuento de linfocitos CD4 sea >200 mm3, pero no hay estudios que evalúen esto en particular.
Por último, en pacientes con intolerancia y/o posible alergia al TMP-SMX el grupo elaborador sugiere considerar otros esquemas de tratamiento, extrapolando recomendaciones expuestas en guías de consenso para otros grupos de pacientes inmunodeprimidos. Muy resumidamente, estos serían: pentamina aerosolizada en dosis de 300 mg cada cuatro semanas, dapsona 100 mg/día o atovacuona 1.500 mg/día, todas ellas disponibles en España30,49,64.
La información completa sobre los resultados obtenidos de la revisión de la evidencia está disponible en la web de la SER (www.ser.es).
Medidas profilácticas primarias y secundarias frente al virus de la hepatitis BEn pacientes con ERAS, ¿cuál es la eficacia o efectividad y seguridad de las medidas profilácticas primarias y secundarias frente al VHB?
Recomendación: en pacientes con LES o con enfermedad de Behçet (EB), se recomienda la vacunación frente al VHB, con tres dosis de vacuna recombinante (20 μg de antígeno de superficie del virus de la hepatitis B [HBsAg] purificado) en la fase inactiva o de baja actividad y sin tratamiento inmunosupresor (recomendación de grado D).
Recomendación: en pacientes con otras ERAS, se sugiere aplicar las recomendaciones expuestas anteriormente. Aunque no hay evidencia directa, se considera que este grupo de pacientes tiene suficientes similitudes con el LES como para extrapolar la recomendación (recomendación de grado √).
Recomendación: en todos los pacientes con ERAS que estén en situación de inmunosupresión (por tratamiento previo o actual), se sugiere considerar pautas vacunales con cuatro dosis y/o con mayor carga antigénica (40 μg de HBsAg purificado) (recomendación de grado √).
Recomendación: se recomienda verificar la respuesta vacunal frente a hepatitis B al completar la pauta indicada, mediante determinación de niveles de anticuerpos frente a antígeno de superficie (anti-HBsAg), un mes después de la vacunación (recomendación de grado √).
Recomendación: en todos los pacientes con ERAS con infección crónica por VHB y que vayan a recibir tratamiento inmunosupresor, terapia biológica (especialmente anti-CD20) o GC (prednisona o equivalente ≥ 20 mg/día durante cuatro semanas), se recomienda el tratamiento concomitante con antivirales, preferentemente entecavir 0,5 mg/día, debido a la elevada tasa de resistencia a lamivudina, para prevenir la reactivación de la infección por VHB (grado de recomendación: √).
La hepatitis por virus B es una de las infecciones más prevalentes a nivel mundial, por lo que la Organización Mundial de la Salud recomienda desde hace años la vacunación universal65. Los pacientes con ERAS presentan un estado de inmunosupresión, intrínseco de la enfermedad y/o secundario a los tratamientos empleados, particularmente el RTX66, que podría interferir con la eficacia de la vacuna frente al VHB o facilitar su reactivación. Por otro lado, se han reportado varios casos de ERAS atribuidos a la vacuna contra el VHB67.
Profilaxis primaria: vacunación frente al VHBLa evidencia identificada es escasa, solamente dos estudios evaluaron la vacunación contra el VHB uno en pacientes con LES inactivo y otro con EB. Ambos mostraron una aceptable inmunogenicidad de la vacuna recombinante (> 90%), usando la pauta estándar (tres dosis de 20 μg de HBsAg)68,69 (nivel de evidencia 3, 2-).
La vacunación no se asoció con reactivación del LES o las dosis de prednisona u otros IS, en comparación con el año previo a la vacunación68 (nivel de evidencia 3). Lo mismo sucedió en la EB, donde solo se observaron EA leves como reacciones locales en el punto de inyección69 (nivel de evidencia 2-).
En pacientes con ERAS e inmunodepresión, los expertos sugieren considerar pautas vacunales con cuatro dosis y/o con mayor carga antigénica, debido a que se presume que la respuesta inmunológica se encuentra alterada en estos individuos. En este sentido cabe señalar que, en otros pacientes inmunocomprometidos, como los trasplantados renales, el uso de vacunas con mayor carga antigénica ha mostrado un incremento en las tasas de seroconversión29,70. Es recomendable verificar el nivel de anticuerpos protectores alcanzado29,70–72.
Profilaxis secundaria: uso de antiviralesAlgunos estudios han mostrado riesgo de reactivación de la hepatitis por VHB en pacientes con ERAS que recibían tratamiento IS o prednisona a dosis > 5 mg/día, uno de ellos con resultado fatal32,73,74,75 (nivel de evidencia 2, 3).
Varios estudios de baja calidad, bien pequeñas series o casos clínicos, informaron de un posible efecto protector de la lamivudina frente a la reactivación de la infección por VHB en ERAS76–81 (nivel de evidencia 3).
En una serie de 17 casos con vasculitis crioglobulinémica asociada a VHB, HBsAg positivo, ninguno de los siete pacientes tratados con antivirales análogos de nucleótidos (entecavir, adefovir o lamivudina) presentó progresión de la enfermedad y el ADN viral fue indetectable82 (nivel de evidencia 3). Se han comunicado también casos de pacientes con ERAS e infección por VHB, tratados con RTX o infliximab, cuya carga viral ha permanecido estable, sin signos de progresión de la infección, con el empleo de antivirales83,84.
El grupo elaborador concluye que debe considerarse iniciar la profilaxis secundaria con antivirales en todos los pacientes con ERAS en regímenes de IS con riesgo alto y moderado, y monitorizar aquellos con bajo riesgo85,86. Los pacientes con ERAS en tratamiento IS deben considerarse en riesgo de reactivación del VHB cuando exista infección crónica o pasada (anti-HBc positivos, con o sin HBsAg positivo). Además de los factores del huésped y del virus, debe tenerse en cuenta el tipo, grado y duración de la inmunosupresión como factor de riesgo clave para la reactivación de la infección85,87 (tabla 2). Se desconoce el nivel de riesgo de otros IS no incluidos en la tabla 2, como el micofenolato mofetilo (MMF), el tacrolimus o la ciclosporina.
Riesgo de reactivación del VHB según tratamiento inmunosupresor
| Riesgo alto (> 10%) | Riesgo medio (1-10%) | Riesgo bajo (< 1%) |
|---|---|---|
| Terapias anti-CD 20 | Otras terapias biológicas (anti TNF) | Metotrexato |
| Dosis altas de GC (≥ 20 mg/día durante más de 4 semanas) | Dosis moderadas de GC (10-20 mg/día) | Azatioprina |
TNF: tumoral necrosis factor; GC: glucocorticoides.
La información completa sobre los resultados obtenidos de la revisión de la evidencia está disponible en la web de la SER (www.ser.es).
Vacunación frente al virus del papiloma humanoEn pacientes con ERAS, ¿cuál es la eficacia o efectividad y seguridad de la vacunación frente al virus del papiloma humano?
Recomendación: en todos los pacientes con ERAS se deben seguir las recomendaciones de vacunación del VPH indicadas en población general, esto es:
- 1.
Se recomienda vacunación universal para niñas, idealmente a los 12 años de edad (recomendación de grado D).
- 2.
En pacientes mayores de edad con tratamiento excisional de cérvix y/o síndrome de verrugas, hipogammaglobulinemia, infecciones y síndrome de mielocatexis (WHIM), así como en menores de 26 años en situación de prostitución, infección por VIH, y hombres que practican sexo con hombres (recomendación de grado D).
Recomendación: en pacientes adultos con ERAS, especialmente con LES, que no estén incluidos en los grupos anteriores, la decisión de vacunar se debe individualizar, considerando el riesgo previo de exposición al virus del papiloma y el de contacto futuro con el virus (recomendación de grado √).
Recomendación: se recomienda administrar la vacuna antes del inicio de la inmunosupresión y en los períodos de remisión o baja actividad de la enfermedad para evitar el efecto potencial de los IS en la respuesta vacunal (recomendación de grado C).
El riesgo de infección por VPH está aumentado en pacientes con ERAS, especialmente en pacientes con LES9,88,89. En consonancia, la prevalencia de lesiones cervicales pre-invasivas y cáncer de cérvix está aumentada consistentemente en pacientes con LES90–95 y se ha constatado, en algunos estudios, una mayor prevalencia de infección por genotipos oncogénicos del VPH96,97. Aunque lo mismo podría estar sucediendo en el SSp98, no se dispone de datos suficientes ni en esta ni otras enfermedades del grupo, que permitan aseverarlo99.
Los estudios identificados evaluaron la vacuna tetravalente (cepas 6, 11, 16 y 18) frente a VPH únicamente en pacientes con LES. Asimismo, conviene señalar que la mayoría de las pacientes en las que se probó la vacuna, tenían baja actividad o remisión del LES.
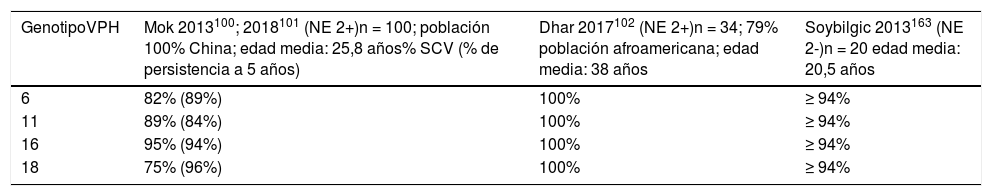
Inmunogenicidad tras la vacunaciónEn lo que respecta a la inmunogenicidad, la tasa de seroconversión osciló entre 75 y 100%, según los estudios y el serotipo vacunal evaluado (tabla 3):
Seroconversión tras vacunación frente al VPH
| GenotipoVPH | Mok 2013100; 2018101 (NE 2+)n = 100; población 100% China; edad media: 25,8 años% SCV (% de persistencia a 5 años) | Dhar 2017102 (NE 2+)n = 34; 79% población afroamericana; edad media: 38 años | Soybilgic 2013163 (NE 2-)n = 20 edad media: 20,5 años |
|---|---|---|---|
| 6 | 82% (89%) | 100% | ≥ 94% |
| 11 | 89% (84%) | 100% | ≥ 94% |
| 16 | 95% (94%) | 100% | ≥ 94% |
| 18 | 75% (96%) | 100% | ≥ 94% |
VPH: virus del papiloma humano; NE: nivel de evidencia; SCV: seroconversión.
Mok et al. evaluaron además la persistencia de anticuerpos protectores a los cinco años de la administración de la vacuna, que osciló entre 84 y 96%. También se objetivó una asociación significativa entre la serorreversión y las dosis acumuladas de prednisona, MMF y tacrolimus100,101 (nivel de evidencia 2+).
En un ensayo clínico fase I realizado en pacientes mayoritariamente afroamericanas con LES inactivo y de alto riesgo de infección por VPH, se observó una tasa de seroconversión del 100%. Sin embargo, en este ensayo se incluyeron únicamente pacientes con dosis de prednisona < 15 mg/día o equivalentes y sin IS102 (nivel de evidencia 1+). A diferencia de los individuos sanos, en estas pacientes no se apreció una respuesta anamnésica de la vacuna. Posiblemente, la propia disfunción del sistema inmune intrínseca a esta enfermedad tenga que ver en este hecho. Los autores concluyen, por tanto, que no es útil solicitar anticuerpos para VPH antes de administrar la vacuna a pacientes con LES103 (nivel de evidencia2+).
Seguridad de la vacunaciónEn lo que respecta a la seguridad de la vacuna, la evidencia indica que los EA son leves en la mayoría de los casos, siendo relativamente frecuente las reacciones en el sitio de inyección (5 a 62%)101,102 (nivel de evidencia 2+,1+). Por otra parte, en un estudio prospectivo, caso-control, la incidencia de EA en LES resultó similar a la de la población general100 (nivel de evidencia 2+). Respecto al posible incremento de riesgo de trombosis venosa profunda, sugerido con base en algunos casos aislados, este no parece sostenerse en la evidencia publicada hasta el momento102 (nivel de evidencia 2+).
En lo que concierne a la actividad de la enfermedad, el índice de actividad del lupus eritematoso sistémico (SLEDAI) resultó similar antes y después de la vacunación en todos los estudios evaluados, sin diferencias en el número de brotes respecto a los no vacunados103. Tampoco se objetivaron cambios serológicos ni trombosis100–102, aunque estos estudios se realizaron mayoritariamente en pacientes con actividad leve o en remisión. Interesantemente, Mok et al., en su estudio a cinco años, objetivaron una mayor incidencia de brotes en pacientes que experimentaron serorreversión asociada al uso de metilprednisolona101(nivel de evidencia 2+). Por último, informes de casos aislados indican la posibilidad de aparición de brotes graves de la enfermedad tras la vacunación104,105(nivel de evidencia 3).
La información completa sobre los resultados obtenidos de la revisión de la evidencia está disponible en la web de la SER (www.ser.es).
En la actualidad, esta vacuna está incluida en el calendario vacunal español para población general femenina106, además de contemplarse para personas de ambos sexos con ciertas patologías de riesgo o algunas prácticas sexuales de riesgo106,107. Aunque la vacuna nonavalente amplía la protección frente a las cepas de VPH causantes de cáncer de cérvix108,109, no hay evidencias disponibles sobre eficacia y seguridad de esta vacuna en ERAS ni datos que permitan emitir recomendaciones específicas sobre su empleo en pacientes ya vacunados con la tetravalente.
Vacunación frente al S. pneumoniaeEn pacientes con ERAS, ¿cuál es la eficacia de la vacunación frente al S. pneumoniae?
Recomendación: se recomienda vacunar frente al S. pneumoniae a todos los pacientes con ERAS, ya que, aunque confiere una inmunogenicidad discretamente menor en comparación con individuos sanos (especialmente en pacientes con LES), es suficientemente efectiva y segura (recomendación de grado B).
Recomendación: se recomienda administrar la vacuna antes del inicio de la inmunosupresión, particularmente si esta es con RTX y en períodos de remisión o baja actividad de la enfermedad, para evitar que el uso de inmunosupresores pueda disminuir la respuesta vacunal (recomendación de grado C).
Recomendación: como esquema de vacunación en pacientes con ERAS, se recomienda el utilizado en la población general, consistente en la estrategia secuencial, iniciando con una dosis de vacuna conjugada y continuando con otra de la vacuna polisacárida (o no conjugada), un mínimo de dos meses después (recomendación de grado √).
Las tasas de infección neumocócica invasiva son mayores en pacientes con ERAS8,110,111. Se han identificaron 14 estudios (dos RS, cuatro ensayos clínicos, siete estudios observacionales y un caso), que abordan tanto la inmunogenicidad como la seguridad de la vacunación. Cabe mencionar que la mayoría de los estudios evaluaron aisladamente la vacuna conjugada o la polisacárida y solo tres evaluaron estrategias de vacunación combinada secuencial.
Pacientes con LESEficacia de la vacuna
Varias RS con metaanálisis de estudios controlados y observacionales, que han evaluado tanto la vacuna no conjugada (polisacárida) 23-valente (PPV23) como las conjugadas 7-valente y 13-valente (PCV13 y PCV7) no han encontrado diferencias significativas entre pacientes con LES y controles sanos en la respuesta inmunogénica112,113 (nivel de evidencia2++). Dos estudios utilizaron la estrategia de vacunación secuencial (conjugada seguida de no conjugada), uno la PCV13 seguida de la PPV23 y otro (un ECA) la PPV23 sola vs. PCV7 seguida de la PPV23, concluyendo que la pauta secuencial no era superior a la vacuna única, en términos de inmunogenicidad ni de persistencia. A pesar de la heterogeneidad de los estudios, sus resultados indican que la vacuna anti-neumocócica es generalmente inmunogénica, aunque una proporción de los pacientes pueden serorrevertir a largo plazo113 (nivel de evidencia 2+).
Predictores de la respuesta a la vacunaDiferentes estudios informaron de una menor respuesta inmunogénica en pacientes menores de 18 años o > 60 años y en los tratados con IS. De los resultados de estos estudios puede concluirse que es recomendable vacunar a los individuos con LES preferentemente antes de iniciar el tratamiento con IS113 (nivel de evidencia 2-). Sin embargo, en el caso del belimumab, un ECA informó que el tratamiento con este agente biológico no afectó a la respuesta a la vacuna 23-valente114 (nivel de evidencia 1+).
En cuanto a la seguridad, en una RS de Adawi et al. no se informaron EA graves de las vacunas antineumocócicas, conjugadas o no conjugadas. Tampoco se encontraron diferencias en brotes de actividad clínica o serológica, con respecto a los controles113 (nivel de evidencia 2+).
Pacientes con otras patologíasTanto la vacuna PPV23 como la PCV13 parecen eficaces y seguras en pacientes con SSp115 (nivel de evidencia 1+) con una posible peor respuesta en aquellos tratados con metotrexato (MTX)116 (nivel de evidencia 2+). Las vacunas antineumocócicas son también inmunógenas en la ES, si bien en al menos un estudio se sugiere una disminución de la eficacia en pacientes tratados con fármacos modificadores de la enfermedad (FAME)117,118 (nivel de evidencia 2-, 2+). En los pacientes con vasculitis asociadas a anticuerpos anticitoplasma de neutrófilo (ANCA), la vacuna antineumocócica podría no ser efectiva si se administra en los períodos de inducción de remisión, sugiriendo que la inmunosupresión de alta intensidad reduce su inmunogenicidad119,120(nivel de evidencia 2+). En fase de mantenimiento, también se ha constatado, en un estudio con un grupo más heterogéneo de vascultis sistémicas, una menor respuesta a la vacunación en pacientes con IS, particularmente RTX121 (nivel de evidencia 2+). En pacientes con vasculitis ANCA y serología positiva para citomegalovirus (CMV), un ECA demostró que el empleo de valaciclovir durante seis meses, con el objetivo de suprimir la reactivación de CMV, incrementaba la eficacia de la vacuna PCV13122(nivel de evidencia 1+). Un estudio retrospectivo encontró una reducción de la mortalidad por cualquier causa en los pacientes con vasculitis ANCA que habían respondido a la vacuna antineumocócica, si bien otros factores confusores, ajenos a la vacunación en sí, podrían también explicar ese interesante resultado121 (nivel de evidencia: 2+). Con respecto a la seguridad, la vacuna ha resultado segura y bien tolerada en pacientes con vasculitis sistémica29,120, sin aumento en la tasa de recidiva de vasculitis relacionada con la vacuna121 (nivel de evidencia 2+). En pacientes con EB, se han comunicado casos de reacciones inflamatorias locales y/o febriles, no graves y autolimitadas, interpretadas como una posible activación desproporcionada del inflamasoma, en consonancia con la propia patogenia de la EB123,124 (nivel de evidencia 3).
La información completa sobre los resultados obtenidos de la revisión de la evidencia está disponible en la web de la SER (www.ser.es).
Vacunación frente al virus de la gripeEn pacientes con ERAS, ¿cuál es la eficacia o efectividad y la seguridad de la vacunación frente al virus de la gripe?
Recomendación: en pacientes con LES, se recomienda la vacunación contra el virus de la gripe, con la vacuna de las cepas AH1N1, AH3N2 y virus de la influenza B, preferiblemente con adyuvante (recomendación de grado B).
Recomendación: en pacientes con otras ERAS diferentes al LES, se sugiere aplicar la recomendación expuesta anteriormente. Aunque no hay evidencia directa, se considera que este grupo de personas tiene suficientes similitudes con aquellas con LES, como para poder extender la recomendación (recomendación de grado C).
Recomendación: en pacientes con ERAS, se sugiere el empleo de una segunda dosis de refuerzo, al cabo de tres a cuatro semanas de la primera, en las siguientes circunstancias (recomendación de grado C):
- -
Uso de fármacos IS
- -
Tratamiento con RTX en los tres meses previos.
Los pacientes con ERAS, especialmente cuando reciben terapia IS, tienen un mayor riesgo de presentar infecciones víricas que, en ocasiones, pueden complicarse y llegar a resultar mortales. La vacunación es la principal medida de prevención de infecciones como la gripe. Sin embargo, la vacunación contra la gripe de pacientes con ERAS podría resultar en una menor producción de anticuerpos protectores contra el virus o en una reactivación de las ERAS125–127.
Eficacia/efectividad de la vacunación frente al virus de la gripe en las ERASDiversos metaanálisis han concluido27,112,128 que la inmunogenicidad de la vacuna antigripal en el LES es, en general, adecuada, en comparación con controles sanos, si bien depende de la cepa del virus, con una menor respuesta para la cepa H1N1 (nivel de evidencia 2++). Otros estudios prospectivos en pacientes con LES mostraron la misma tendencia129,130 (nivel de evidencia 1+, 2+), observándose en uno de ellos, además, un efecto booster tras la segunda inoculación130 (nivel de evidencia 2+). Otro estudio que comparó pacientes LES vacunados con controles históricos no vacunados mostró una diferencia significativa en la razón de títulos de anticuerpos a favor de los vacunados (n = 19, CMG: 141,05 vs. n = 11, CMG: 8,89; p = 0,018)131 (nivel de evidencia 2+). Por último, el estudio antes-después realizado por Launay et al. informó de un aumento significativo de los títulos de anticuerpos para las tres cepas, tras la vacunación132 (nivel de evidencia 2+).
En cuanto a las medidas de resultado clínicas en pacientes con LES, al menos un estudio mostró menor tasa de gripe en los seis meses postvacunación (5 vs. 55% en no vacunados; p< 0,01), e, interesantemente, menor tasa de otras infecciones víricas131 (nivel de evidencia 2+). Chang et al., utilizando una base de datos administrativa, encontraron que la vacuna de la gripe se asoció con una menor probabilidad de hospitalización, admisión en unidad de medicina intensiva, bacteriemia o septicemia y muerte133 (nivel de evidencia 2++).
En pacientes con otras ERAS (ES, SSp, EMTC o MI) no se han encontrado, en general, diferencias significativas respecto a controles sanos en inmunogenicidad de la vacuna antigripal ni tampoco en las tasas de seroprotección o seroconversión, que se reportan similares o ligeramente inferiores en algún caso, en los diferentes estudios revisados134–141 (nivel de evidencia 2+). Lo mismo sucede en el caso de las vasculitis asociadas a ANCA, aunque con mayor nivel de evidencia, con base en los resultados de dos ECA y un estudio no aleatorizado142–144 (nivel de evidencia 1+, 2+). Otros trabajos en pacientes con ERAS considerados colectivamente, han mostrado seroprotección, seroconversión y CMG suficiente para alcanzar los criterios del Committeefor Medicinal Products for Human Use (CHMP), aunque sus valores fueran inferiores a los controles sanos129,145–147. Asimismo, un estudio abierto y prospectivo, que comparó la inmunogenicidad de la vacuna antigripal A/09/H1N1 en pacientes con ERAS, observó tasas de seroconversión y de seroprotección significativamente menores en el grupo de pacientes, que, sin embargo, se igualaron tras una segunda inoculación de la vacuna126 (nivel de evidencia 2+).
Factores predictivos de no respuesta a la vacunación frente al virus de la gripeEn pacientes con LES, un metanalisis y diversos estudios revisados sugieren que el tratamiento IS reduce la respuesta a la vacuna de la gripe, incluyendo tanto los GC como los IS propiamente dichos (azatioprina [AZA], MMF, MTX y ciclofosfamida [CFM])128,130,131 (nivel de evidencia 2+). En la misma dirección, varios estudios indican que los pacientes con LES tratados con dosis de prednisona ≥10 mg/día o ≥0,15 mg/kg/día presentan menor tasa de seroconversión130,131,146 (nivel de evidencia 2+). Aunque, la hidroxicloroquina no parece tener efecto en la eficacia de la vacuna128 (nivel de evidencia 2+), un estudio ha sugerido que la inmunogenicidad de la vacuna frente a AH1N1/2009 en pacientes con dosis de prednisona >20 mg con o sin IS, podría ser restablecida por los antimaláricos148 (nivel de evidencia 2+). Respecto al tratamiento con belimumab, un estudio cuasiexperimental concluyó que no afectaba a la respuesta inmunológica de la vacuna de la gripe149 (nivel de evidencia 2+).
Respecto a la actividad del LES, varios estudios relacionan el nivel de actividad con el fallo de seroconversión frente a la vacuna de la gripe130,131,146 (nivel de evidencia 2+).
Un metaanálisis indica que la ausencia de adyuvante en la vacuna frente a AH1N1 se asocia a menor tasa de seroconversión y seroprotección cuando se compara con la adyuvada128 (nivel de evidencia 2+).
En diversos estudios sobre otras ERAS (ES, SSp, MI o EMTC) no se ha conseguido demostrar que los IS sean un factor predictivo de menor respuesta a la vacuna de la gripe134,137,139–141(nivel de evidencia 2+). Lo mismo sucede en pacientes con vasculitis, aunque con mayor nivel de evidencia con base en dos ECA y un estudio no aleatorizado142–144 (nivel de evidencia 1+, 2+). Sin embargo, estudios que han incluido pacientes con diferentes enfermedades reumáticas, incluyendo ERAS, observaron que la inmunogenicidad estaba reducida significativamente por el tratamiento con MTX, leflunomida u otros IS (AZA, MMF y CFM)126 (nivel de evidencia 2+). En un ensayo clínico, Kostianovsky et al. encontraron que la terapia biológica (RTX, etanercept, adalimumab e infliximab) se asociaba con un marcado descenso en la tasa de seroconversión, seroprotección y CMG129 (nivel de evidencia 1+). Por su parte, Adler et al. mostraron que los pacientes con menor respuesta inmunológica a la vacuna de la gripe, en comparación con controles sanos, son los que reciben MTX, RTX o abatacept (p = 0,045)145 (nivel de evidencia 2+). En cuanto a las características de la enfermedad, Litinsky et al. informaron que los pacientes con ES y enfermedad pulmonar intersticial difusa muestran una menor respuesta frente a la vacuna, en comparación con los que no la presentan135 (nivel de evidencia 2-). En pacientes con MI, los niveles más elevados de aldolasa, podrían asociarse con mayor frecuencia de fallo en la seroconversión140 (nivel de evidencia 2+).
Seguridad de la vacunación frente al virus de la gripeEn términos generales, se constata una muy baja frecuencia de EA graves en pacientes con ERAS que reciben vacunas antigripales, en los diferentes estudios. En un metanalisis ya mencionado previamente y otros estudios adicionales, no se encontró más incidencia de EA en pacientes con LES en comparación con los controles sanos27,128,131,149 (nivel de evidencia 2+). En relación con un posible aumento de la actividad de la enfermedad, en el RS y metaanálisis de Pugès et al., la vacuna no modificó el SLEDAI112 (nivel de evidencia 2++). Un estudio tampoco encontró diferencias significativas en los títulos de anticuerpos anti-ADN ni en otros autoanticuerpos150. En contraste, en otro estudio se concluyó que la vacuna de la gripe puede inducir anticuerpos anticardiolipina o aumentar sus títulos, aunque sin traducción clínica151 (nivel de evidencia 2+).
En los estudios llevados a cabo en pacientes con otras ERAS (ES, SSp, MI o EMTC) no se encontraron diferencias en los porcentajes de EA respecto a controles sanos134–141 (nivel de evidencia 2+/2-). Tampoco se apreció empeoramiento clínico significativo, de ninguna de las ERAS mencionadas, tras la vacunación. De forma similar a lo que sucede en el LES, dos trabajos en SSP constataron un aumento de ciertas citocinas proinflamatorias (interferón γ, interleucina [IL]4 o IL17) y autoanticuerpos (anti-Ro y anti-La), sin que ninguno de ellos se relacionara con empeoramiento clínico137,138 (nivel de evidencia 2+). En los estudios realizados en pacientes con vasculitis ANCA, la vacuna antigripal se ha mostrado segura, tanto en términos de efectos adversos como de actividad de la enfermedad, estimada con el índice Birmingham Vasculitis Activity Score (BVAS)142,144,152 (nivel de evidencia 1+, 2+). Una observación interesante, en una cohorte de 230 pacientes con vasculitis asociada a ANCA, fue que la ratio de recaída de la enfermedad por cada 100 pacientes fue menor en sujetos vacunados de la gripe que en no vacunados (3,4 vs. 6,3%)152 (nivel de evidencia 2+).
La información completa sobre los resultados obtenidos de la revisión de la evidencia está disponible en la web de la SER (www.ser.es).
El grupo elaborador considera que los resultados de los distintos estudios identificados resultan mayoritariamente consistentes, respecto a la eficacia/efectividad de la vacuna antigripal en pacientes con ERAS. Cabe remarcar que, aunque el grado de inmunogenicidad alcanzado en algunos casos, como en los pacientes con LES para ciertas cepas, es con frecuencia menor que el de los individuos sanos, este continúa siendo adecuado. Sin embargo, en ciertos perfiles de pacientes (por ejemplo: LES activo, con tratamiento IS o con dosis diarias de prednisona > 10 mg, u otras ERAS en tratamiento IS), la eficacia parece menor.
DiscusiónEn este documento, se han desarrollado recomendaciones de prevención de infecciones en ERAS, basadas en RS de la evidencia disponible, de mayor alcance que la llevada a cabo por los expertos de EULAR en su actualización de recomendaciones vacunales29, para el subgrupo concreto de las ERAS. En los casos en los que no se ha dispuesto de evidencia suficiente, las RS se han complementado con la opinión consensuada del panel de expertos. Constituyen, que sepamos, las primeras recomendaciones de prevención de infección específicamente desarrolladas para ERAS. Además, incluyen menciones a vacunas y quimioprofilaxis no contempladas en las preguntas PICO y medidas generales de prevención de infección, que debe formar parte del estándar de gestión de riesgo de infección en todo paciente inmunocomprometido.
De manera general se puede concluir que las vacunas analizadas son razonablemente seguras y efectivas en pacientes con ERAS, si bien su inmunogenicidad no siempre alcanza un nivel similar al de la población general. En algunas de las vacunas evaluadas en las ERAS, se ha observado una influencia negativa del tratamiento IS, particularmente documentada en pacientes con LES que reciben vacuna antigripal128. Conviene puntualizar que la gran mayoría de los estudios que no han demostrado un efecto negativo de los IS en la inmunogenicidad de las vacunas, carecen de suficiente potencia estadística.
Le estrategia de refuerzo vacunal, empleando una segunda dosis de la vacuna antigripal o mayor número de dosis frente al VHB, para potenciar la respuesta, es una recomendación novedosa en el terreno de las ERAS, que trata de sortear una posible respuesta subóptima, como consecuencia del tratamiento IS o de la alta actividad en el momento de recibir la vacuna. Esta estrategia se emplea con éxito en otras situaciones de compromiso de inmunidad, como en el trasplante de órgano sólido153.
Respecto a la quimioprofilaxis, solo se ha contemplado la prevención de neumonía por PCj. Si bien el panel reconoce que la incidencia de esta infección es baja en pacientes con ERAS49,154, dada su elevada mortalidad155–157, superior incluso a la observada en pacientes con VIH54 y la efectividad y relativa seguridad del TMT/SMX encontrada en la RS, se recomienda su empleo en subgrupos de riesgo. Apoyando su uso, existe un análisis coste-efectividad, con resultado favorable, en pacientes con vasculitis158.
Además de las contenidas en el cuerpo de evidencia, desarrollado a partir de las preguntas PICO, resulta pertinente resaltar otras ventajas potenciales de la quimioprofilaxis con TMT/SMX, como la prevención de otras infecciones respiratorias graves, distintas de la neumonía por PCj, en pacientes con vasculitis sistémicas tratadas con RTX159.
Otro potencial efecto beneficioso de la vacunación, ligado a la reducción de eventos infecciosos, es la contribución al control de la actividad en las ERAS, ya que las infecciones son desencadenantes conocidos de brotes de enfermedad en estos pacientes. Este efecto ha sido poco estudiado y se ha descrito únicamente con la vacuna de la gripe en el LES o las vasculitis asociadas a ANCA152.
Entre las limitaciones de estas recomendaciones, es necesario señalar, en primer lugar, su limitado espectro, al no incluir todas las infecciones para las que se dispone de medidas preventivas. En este sentido, el criterio del grupo de expertos ha sido no incluir recomendaciones para infecciones en las que se prevén cambios a corto plazo, como es el caso del virus varicela zóster (VVZ)
En segundo lugar, para algunas mejoras introducidas en las vacunas, como por ejemplo la vacuna nonavalente del VPH (VPH-9), que amplía el espectro antigénico sobre la tetravalente previa (VPH-4), sería deseable disponer de datos de seguridad específicos para las ERAS. No hay evidencia sobre si es o no recomendable revacunar con VPH-9, para ampliar la protección a pacientes ya vacunados con VPH-4. Quizás sería razonable hacerlo solo si persisten los factores de riesgo para el desarrollo de neoplasia cervical, o si a pesar de estar ya vacunado, el paciente se infecta por VPH. Son necesarios estudios para evaluar si esta práctica es segura y coste-efectiva en pacientes con ERAS.
En tercer lugar, la información de seguridad y eficacia de las vacunas contempladas en las recomendaciones hace referencia a pacientes en remisión o baja actividad y, por tanto, con dosis bajas de GC o inmunosupresión de mantenimiento o ausente, como escenario más común. Dada la estimulación de la inmunidad, intrínseca al proceso de vacunación, existe la hipotética posibilidad de que las vacunas desencadenen brotes de actividad en las ERAS. Sin embargo, la RS de la evidencia sugiere que, al menos en situación de remisión o de baja actividad, las vacunas revisadas no incrementan de forma relevante la actividad de las ERAS. Los datos en este sentido son particularmente sólidos para el LES, pero menos robustos en el resto de las ERAS, en las que, a pesar de que son consistentes con lo descrito en LES, resultan insuficientes.
En cuarto lugar, existe una limitación respecto a la población diana de determinadas vacunas, como la dirigida contra el VPH, que ha sido estudiada fundamentalmente en mujeres. Como es posible la existencia de diferencias sexuales en lo que a inmunogenicidad se refiere160–162, estos resultados no son directamente aplicables a hombres.
Por último, en las RS que sustentan estas recomendaciones, se encontró información limitada en cuanto a los desenlaces clínicos más relevantes, como evento infeccioso, hospitalización o mortalidad.
ConclusionesSe presenta el primer documento oficial de la SER de recomendaciones para la prevención de infecciones en pacientes con ERAS. Estas recomendaciones se han alcanzado mediante una metodología validada, de RS de la literatura científica y técnicas de consenso de expertos. Las recomendaciones pueden aplicarse directamente al sistema sanitario español, ya que todas las vacunas y agentes quimioprofilácticos incluidos están disponibles en España.
La RS de la evidencia indica que tanto las vacunas, como las quimioprofilaxis contempladas en estas recomendaciones son razonablemente seguras y eficaces en las ERAS. Se ha observado que algunas vacunas no alcanzan el mismo nivel de inmunogenicidad que la población general, algo que parece estar en relación, principalmente, aunque no exclusivamente, con el tratamiento IS. Para evitar el riesgo que supone retirar la terapia en pacientes con ERAS, en algunas vacunas como la de la influenza, se ha recomendado la estrategia de refuerzo vacunal, con una segunda dosis, dados sus buenos resultados en otras poblaciones de pacientes inmunosuprimidos.
FinanciaciónFundación Española de Reumatología.
Conflicto de interesesÍñigo Rua-Figueroa Fernández de Larrinoa declara no tener ningún interés en relación con este documento de recomendaciones.
Patricia E. Carreira ha recibido financiación de Pfizer, Roche, MSD, Nordic Pharma y Janssen para la asistencia a reuniones, congresos y cursos; honorarios de Actelion, Roche y GSK en concepto de ponencia; ha recibido financiación de Actelion, MSD y Roche por participar en una investigación y a título de consultoría para compañías farmacéuticas u otras tecnologías.
José María Pego Reigosa ha recibido financiación de Pfizer y Novartis para la asistencia a reuniones, congresos y cursos; honorarios de MSD en concepto de ponencia; y ayuda económica para la financiación de una investigación y a título de consultoría por parte de Pfizer.
José Alfredo Gómez Puerta ha recibido financiación de Pfizer, Roche y Abbvie para la asistencia a reuniones, congresos y cursos; honorarios de Pfizer para la realización de programas educativos o cursos y de MSD, BMS, Pfizer y Janssen como ponente; ha recibido ayuda económica de Inova/werfen en concepto de consultoría para compañías farmacéuticas u otras tecnologías.
Rafaela Ortega Castro ha recibido financiación de Pfizer, MSD, Abbvie, Janssen, Cellgener y Lilly para la asistencia a reuniones, congresos y cursos; honorarios de Pfizer, MSD, Abbvie, Janssen y Lilly en concepto de ponencia.
Beatriz Tejera Segura declara no tener ningún interés en relación con este documento de recomendaciones.
José L. Valencia Martín ha recibido financiación de Pfizer y Glaxo-Smithkline para la asistencia a reuniones, congresos y cursos;
José María Aguado García y Julián de la Torre Cisneros declaran no tener ningún conflicto de intereses.
El grupo de expertos del presente trabajo quiere manifestar su agradecimiento a Mercedes Guerra Rodríguez, documentalista de la SER, por su colaboración en las estrategias de búsqueda de la evidencia. También a la Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica.
El grupo de expertos quiere agradecer expresamente además a los siguientes especialistas revisores del documento, por su revisión crítica y aportaciones al mismo:
Maria Luisa Vargas Pérez. Jefa de Sección de Inmunología, Hospital Universitario de Badajoz. Badajoz.
Jaime Calvo Alén. Jefe de Servicio de Reumatología, Hospital Universitario Araba. Vitoria-Gasteiz, Álava.También quiere agradecer al Dr. Federico Diaz González, director de la Unidad de Investigación de la SER, por su participación en la revisión del manuscrito final y por contribuir a preservar la independencia de este documento.