Los pacientes con artritis reumatoide (AR) tienen mayor riesgo de presentar infecciones respecto a la población sana. Éste principalmente se debe a la enfermedad en sí, a la comorbilidad y al tratamiento inmunosupresor.
La evidencia clínica demuestra que la administración de las vacunas frente al neumococo y los virus influenza y hepatitis B en pacientes con AR no empeora la actividad de la enfermedad, y que éstas son eficaces, aunque parece que la respuesta inmunitaria se ve reducida por la propia enfermedad y el tratamiento con FAME y biológicos. Por ello, es aconsejable vacunar a los pacientes al diagnóstico, antes de iniciar el tratamiento con inmunosupresores.
También existen y se deben tomar medidas profilácticas para evitar la reactivación de infecciones latentes crónicas como la tuberculosis y la hepatitis B durante el tratamiento con biológicos.
Patients with rheumatoid arthritis (RA) are at increased risk of infection compared to healthy individuals. The increased risk may be associated with the underlying disease, comorbidities and immunosuppressive therapy required to control RA activity.
In several recent studies, influenza, pneumococcal and hepatitis B vaccines administered to RA patients were reported to be safe and serologically effective.
However, several lines of evidence suggest a possible aberrant immunologic response following vaccination due to the compromised immunity of these patients. Therefore, vaccination of RA patients prior to immunosuppressive treatment may serve as an alternative prophylactic approach and should be considered for future investigation.
Besides, prophylactic health measures should be taken to avoid latent chronic infections as tuberculosis and hepatitis B, during therapy with biological agents.
Se estima que los pacientes con artritis reumatoide (AR) tienen el doble de riesgo de padecer infecciones respecto a la población sana1. Este aumento del riesgo se debe por un lado a la propia enfermedad, puesto que los factores de mal pronóstico de la enfermedad han sido identificados como predictores de infección, y por otro, a la comorbilidad asociada (diabetes, alcohol, tabaco, enfermedad pulmonar obstructiva crónica)2 y al tratamiento con fármacos inmunosupresores3,4.
Hasta el momento, las recomendaciones para el manejo de AR determinan que estos pacientes se deben vacunar frente al neumococo, influenza y hepatitis B5. Para el resto de las vacunas, se deben seguir las mismas indicaciones que para la población sana, teniendo en cuenta que la administración de vacunas vivas está contraindicada.
Los pacientes con AR, además de tener un aumento del riesgo de primoinfecciones, tienen mayor probabilidad de sufrir reactivaciones de infecciones crónicas latentes como la tuberculosis (TBC) o la hepatitis B. En conjunto, todas estas infecciones conllevan un aumento tanto de la morbilidad como de la mortalidad de los pacientes; de ahí que la toma de conductas preventivas como la vacunación y la quimioprofilaxis sea esencial.
Sin embargo, a pesar de que las vacunas han demostrado ser eficaces en este grupo de pacientes inmunodeprimidos, son una medida hoy en día poco utilizada. Se estima que su uso se limita a un 40%, mientras que el de otras medidas preventivas como las dirigidas contra factores de riesgo cardiovascular asciende hasta un 90%. Esto se debe principalmente a la falta de concienciación del profesional sanitario y a la desconfianza que han suscitado las vacunas en lo que respecta a dos aspectos fundamentales como son su seguridad y eficacia6.
En cuanto a la seguridad, hemos de tener en cuenta que en los pacientes con tratamiento inmunosupresor las vacunas vivas están contraindicadas. También se debe tener precaución con la administración a convivientes de estos pacientes de la vacuna oral frente a la poliomielitis7 y con la vacuna frente al rotavirus8, ya que se ha demostrado que estos virus se eliminan por las heces tras la vacunación durante unos días y podrían infectar al paciente con AR.
Respecto al empleo de vacunas inactivas en pacientes con AR, la preocupación por la seguridad tiene su origen en una serie de casos publicados que sugieren un empeoramiento clínico de los pacientes tras la vacunación e incluso que las vacunas funcionan como desencadenantes de la enfermedad9,10. Sin embargo, tras diferentes estudios, no se ha demostrado causalidad entre las vacunas y el empeoramiento de la enfermedad, medido éste por parámetros clínicos (número de articulaciones dolorosas, número de articulaciones tumefactas, health assessment questionnaire, escala visual analógica de dolor del paciente) y de laboratorio (proteína C reactiva y velocidad de sedimentación globular) relacionados con la actividad de la AR. Así, la evidencia indica que la vacuna de la hepatitis B y la antineumocócica pueden administrarse con un grado de recomendación B11,12 y la antigripal con un grado A13–15.
Por otro lado, para evaluar la eficacia de las vacunas, lo correcto sería realizar estudios en los que se midiera el número de infecciones evitadas tras la vacunación. Sin embargo, en los estudios por ahora disponibles, se emplea la respuesta inmunitaria como sustituto de eficacia, la cual se determina mediante dos cuantificaciones: inmunogenicidad (capacidad de responder al antígeno, y por tanto, de producir un aumento de anticuerpos específicos) y protección (nivel de anticuerpos por encima de un determinado límite teórico a partir del cual se supone que se está protegido).
El objetivo de esta revisión es actualizar los conocimientos publicados acerca de medidas preventivas como la vacunación y la quimioprofilaxis en pacientes con AR y a partir de ésta establecer un posible calendario de vacunación y recomendaciones útiles para la práctica clínica diaria.
Vacuna frente al virus influenzaSe trata de una vacuna inactiva proteica compuesta por dos cepas de antígeno A y una cepa B que se modifican anualmente según las recomendaciones de la Organización Mundial de la Salud.
Existen diferentes estudios que han evaluado su eficacia en pacientes con AR.
Formin et al13 compararon la respuesta inmunitaria a la vacuna de la gripe entre un grupo de controles sanos y un grupo de pacientes con AR con diferentes tratamientos (FAME, etanercept o infliximab). En ambos grupos, los anticuerpos específicos frente a las cepas A se incrementaron significativamente, mientras que el aumento para la cepa B fue mayor en el grupo de sanos (p<0,05). En cuanto a la consecución de protección, no hubo diferencias estadísticamente significativas entre ambos grupos para las cepas A; sin embargo, la respuesta protectora a la cepa B fue alcanzada en el 67% de los pacientes con AR versus el 87% en controles sanos (p<0,05). Un dato relevante fue que el porcentaje de respondedores en el grupo de AR fue el mismo, independientemente del tratamiento que estuviese realizando.
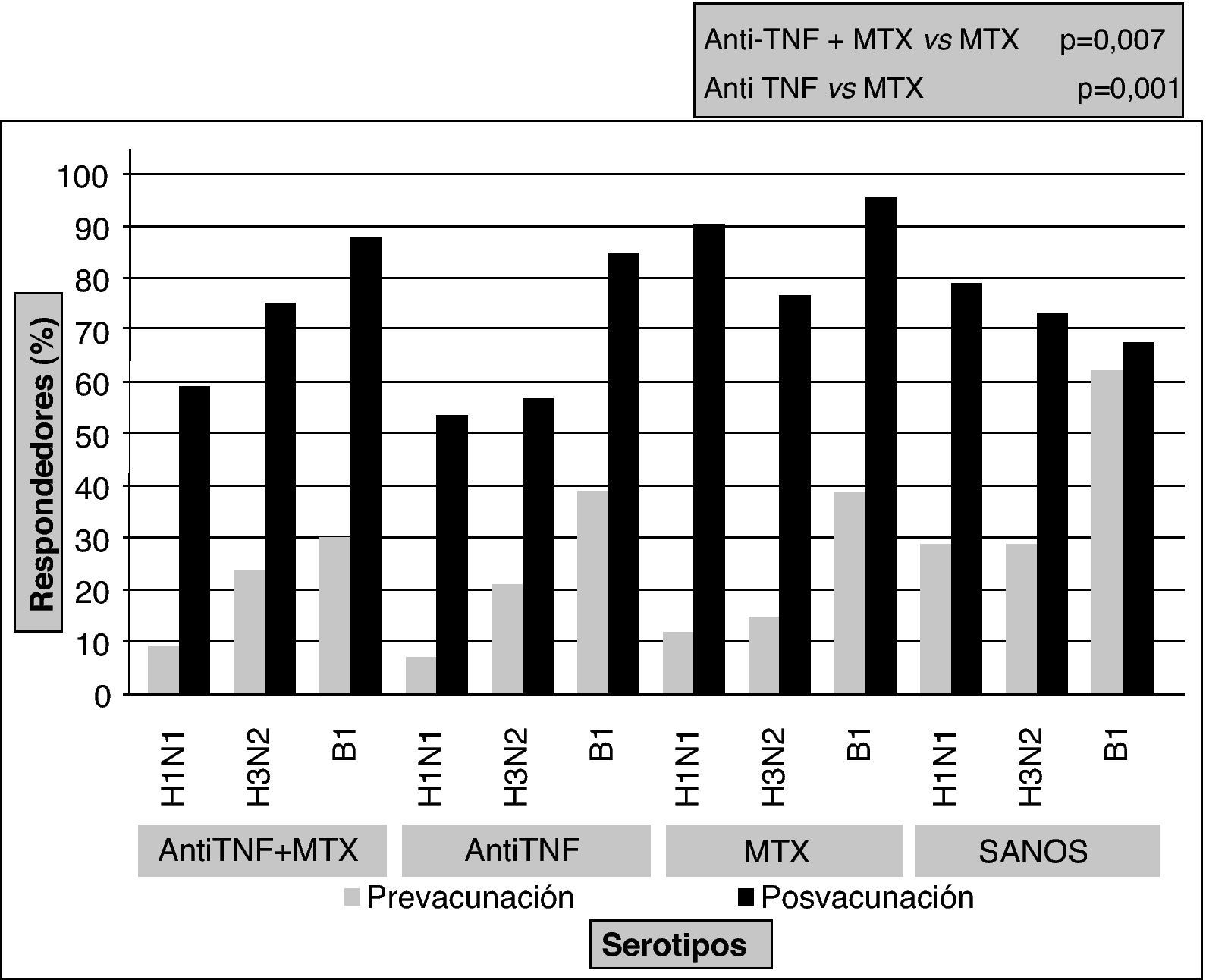
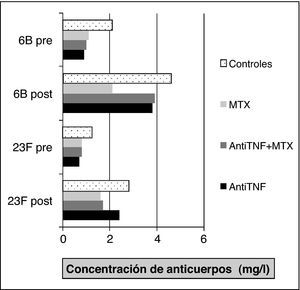
En un estudio realizado posteriormente16 se compara la respuesta a la vacuna de la gripe y del neumococo entre sanos y tres grupos de pacientes con AR (anti-TNF [infliximab o etanercept], metotrexato y terapia combinada). Se observó un incremento de los niveles de anticuerpos posvacunación para todas las cepas en todos los grupos, pero la respuesta protectora fue significativamente mayor en el grupo con metotrexato en monoterapia comparado con los grupos de tratamiento con anti-TNF (fig. 1). Sin embargo, estos resultados difirieron en el estudio de Kaine et al17, en el que el porcentaje de respondedores en ambos grupos (adalimumab±FAME versus placebo±FAME) fue similar y la respuesta inmunitaria a la vacuna no difirió por el uso de FAME concomitante.
Por otro lado, la eficacia de la vacuna frente a la gripe en pacientes con AR en tratamiento con rituximab también ha sido evaluada. Un primer estudio18 determina la respuesta a la vacuna en pacientes con AR tratados con rituximab y pacientes con FAME. Se observó que la proporción de respondedores para la cepa B fue menor en el grupo con rituximab (21% vs 67%; p=0,006), mientras que el porcentaje de respondedores para las cepas A fue similar en ambos grupos. Recientemente, se han publicado los resultados de un estudio14 que analiza la respuesta a la vacuna en pacientes con AR en tratamiento con rituximab (n=23), metotrexato (n=20) y sanos (n=29). El grupo de rituximab se dividió en dos subgrupos, uno que recibió la vacuna entre 4-8 semanas después de la última dosis de rituximab y otro al que se le administró 6-10 meses después del tratamiento. Tras la vacunación, los títulos de anticuerpos específicos para las tres cepas aumentaron de forma estadísticamente significativa en el grupo de sanos y en aquellos con metotrexato; sin embargo, no se produjeron incrementos significativos de anticuerpos en el grupo con rituximab. Por otro lado, la protección alcanzada para todas las cepas en sanos y para las cepas A en el grupo de metotrexato fue más frecuente que en el grupo de rituximab, siendo esta diferencia estadísticamente significativa. En este último grupo, sólo el 26% de los pacientes alcanzó protección inmunitaria, perteneciendo la mayoría al subgrupo con una diferencia de tiempo mayor entre la administración de rituximab y la vacuna (6-10 meses). Además, no se encontró correlación entre el nivel de células B séricas, los niveles iniciales de anticuerpos, la inmunogenicidad y la protección en los pacientes con rituximab. La discrepancia entre los resultados de este último estudio y el primero podría explicarse por la mayor diferencia de tiempo entre el tratamiento con rituximab y la vacunación en el estudio de Oren et al18.
En pacientes en tratamiento con abatacept, no existen datos sobre seguridad y eficacia de la vacuna. En el caso de tocilizumab, la evidencia es muy limitada19. Existe un estudio que compara la respuesta a la vacuna frente a la gripe en pacientes con AR en tratamiento con tocilizumab y aquella obtenida en pacientes con anti-TNF o FAME, en el cual no se encontraron diferencias estadísticamente significativas en los porcentajes de pacientes respondedores a cada cepa.
En resumen, se ha demostrado que la vacuna de la gripe es segura en pacientes con AR y que la respuesta inmunitaria en estos pacientes puede ser inferior que en la población sana. El tratamiento con anti-TNF y rituximab se ha asociado a una menor protección frente a la infección.
Vacuna antineumocócicaExisten dos tipos de vacuna contra el neumococo: la polisacárida, que contiene 23 serotipos causantes del 88% de las infecciones por neumococo, y la proteica (heptavalente y 13-valente) que sólo está indicada en menores de 5 años y es más inmunogénica, aunque no se ha administrado hasta el momento a pacientes con AR.
En cuanto a la evaluación de la eficacia de la vacuna polisacárida en la AR, un primer estudio12 compara la respuesta en pacientes con AR en tratamiento con FAME (la mayoría con metotrexato) y sanos. Los pacientes con AR tuvieron incrementos significativos en la concentración de anticuerpos específicos para todos los serotipos estudiados. El porcentaje de respondedores fue mayor en el grupo de sanos, aunque sólo se detectó una diferencia estadísticamente significativa en el serotipo 7F. No se observó que el tratamiento con prednisona, metotrexato, hidroxicloroquina o azatioprina influyera en la respuesta.
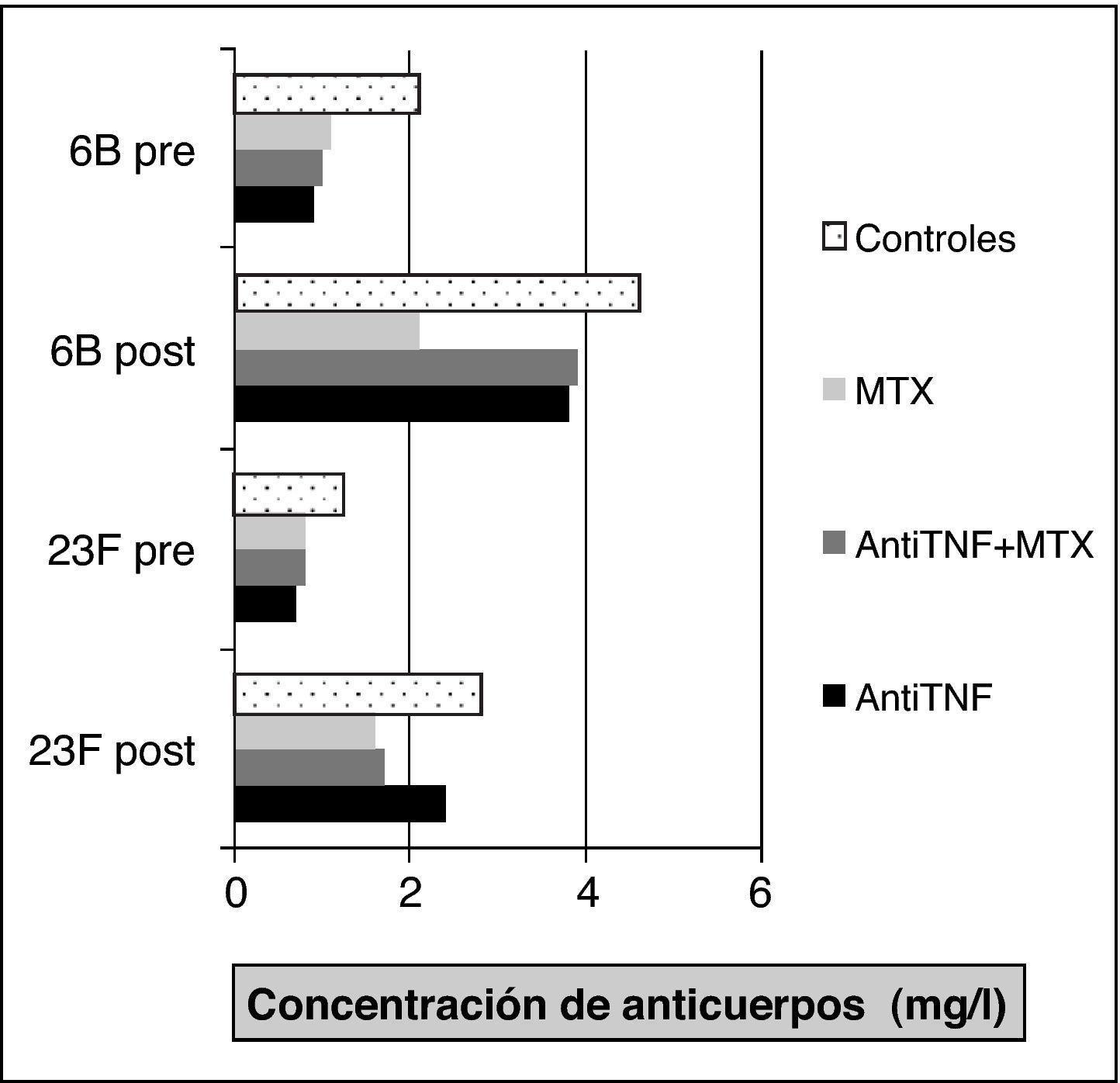
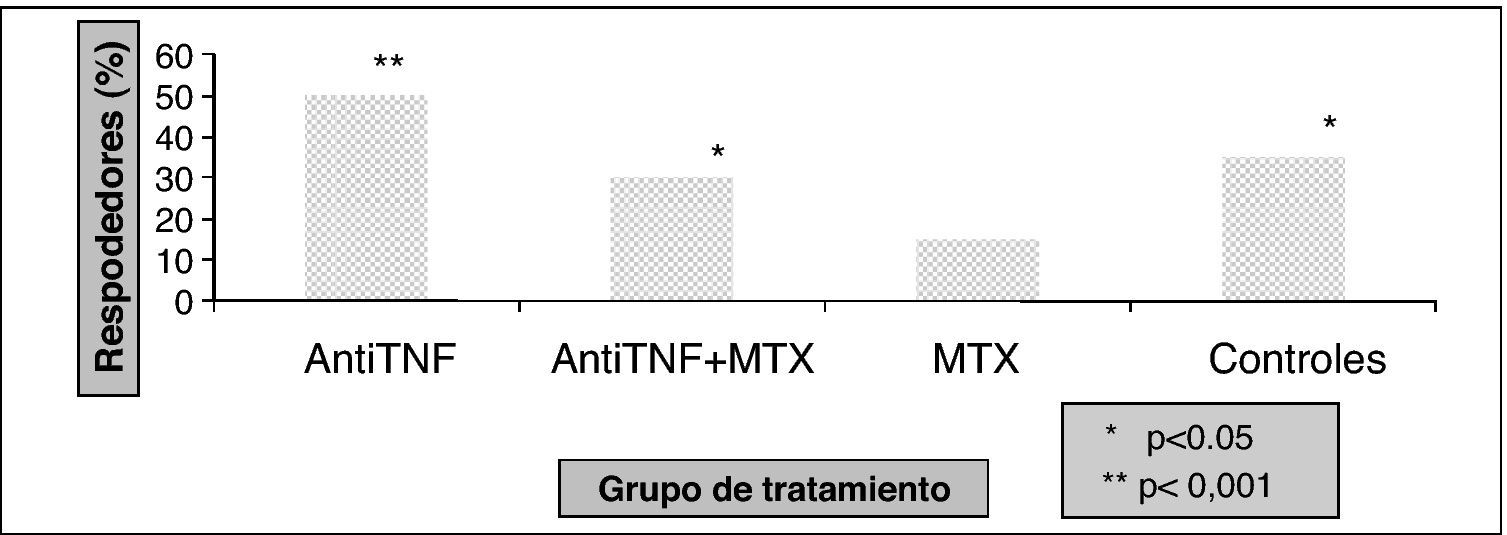
Kapetanovic et al16 analizaron la respuesta inmunitaria en 149 pacientes con AR (anti-TNF [infliximab o etanercept], metotrexato y terapia combinada) y 18 sanos. Los anticuerpos posvacunación se incrementaron significativamente en comparación con los niveles prevacunación para todos los grupos de tratamiento (fig. 2), aunque la respuesta protectora fue menor en el grupo del metotrexato, con diferencias estadísticamente significativas respecto al resto de grupos (fig. 3).
Otro estudio20 confirma los resultados anteriores en cuanto a la eficacia de la vacuna en pacientes con infliximab, y evalúa la respuesta en 70 pacientes asignados a tres grupos de tratamiento (infliximab 3mg/kg más metotrexato, infliximab 6mg/kg más metotrexato y placebo más metotrexato). No se identificaron diferencias en la respuesta a la vacuna entre los tres grupos.
Por otro lado, Kaine et al17 no encontraron diferencias entre el porcentaje de pacientes protegidos en el grupo con adalimumab y el de placebo. Determinaron que los FAME y los títulos protectores previos a la vacuna reducen de forma estadísticamente significativa la respuesta inmunitaria.
Recientemente21 se ha comparado la respuesta en un grupo de pacientes con AR tratados con rituximab, con o sin metotrexato, con un grupo de AR en tratamiento con metotrexato en monoterapia. Tras la administración de la vacuna (28 semanas después del tratamiento con rituximab), comprobaron que los niveles de respuesta en el grupo de rituximab eran menores respecto a los del metotrexato para todos los serotipos. Resalta el hecho de que los niveles séricos de células B no predijeron la respuesta en el grupo de rituximab y sólo se identificó como predictor significativo la concentración de IgG2 en el momento de la inmunización, de forma que por cada aumento de 1mg/dl de IgG2 la respuesta a la vacuna se incrementó un 1%.
La evidencia con otras terapias biológicas es muy limitada. En pacientes con AR en tratamiento con abatacept se evaluó la respuesta inmunitaria a la vacuna antineumocócica dentro del estudio ARRIVE22 (sin grupo control) y se comprobó que abatacept no inhibía completamente la respuesta inmunitaria a la vacuna. En pacientes en tratamiento con tocilizumab existe un estudio23 en el que todos los pacientes mostraron una respuesta protectora tras la vacunación.
En conclusión, la seguridad de la vacuna antineumocócica en pacientes con AR ha sido demostrada, y respecto a la eficacia, parece reducida tanto por la propia enfermedad como por el tratamiento con FAME, rituximab y abatacept.
Vacuna y quimioprofilaxis de la hepatitis BEn todos los pacientes con diagnóstico de AR, se debe realizar serología de hepatitis B y C durante la etapa de diagnóstico, o en su caso, antes de iniciar tratamiento con inmunosupresores, ya que, según la ficha técnica de metotrexato y leflunomida se ha de tener gran precaución en su administración a pacientes con enfermedades hepáticas, y los biológicos están contraindicados en pacientes con infección por virus de la hepatitis B (VHB).
De ser la serología negativa, se debe vacunar al paciente previamente al inicio del tratamiento que proceda. Se ha observado que la administración de esta vacuna en pacientes con AR es segura11. Hasta la fecha, no existen estudios que comparen directamente la respuesta inmune tras la administración de la vacuna frente al VHB en pacientes con AR y sanos. Se estima que entorno al 85% de la población sana responde a la vacuna, mientras que un estudio11 realizado en pacientes con AR en tratamiento con FAME observó inmunización protectora en el 68% de éstos. El tratamiento con metotrexato no afectó al porcentaje de respuesta; sin embargo, se ha comprobado que el tratamiento con etanercept en combinación con metotrexato o en monoterapia reduce significativamente la respuesta a la vacuna24. Es necesaria la realización de nuevos estudios que evalúen la eficacia de esta vacuna en pacientes con AR en tratamiento con otros biológicos.
En caso de que el paciente presente infección aguda o crónica activa por VHB, no se debe iniciar tratamiento inmunosupresor en ningún caso y se debe derivar al paciente al hepatólogo de referencia.
Sin embargo, en los pacientes con infección crónica inactiva o portadores ocultos, a pesar de estar contraindicados, los biológicos se están empleando en algunos casos debido a la elevada actividad de la enfermedad. Los datos que existen de pacientes con hepatitis B y enfermedad reumática en tratamiento inmunosupresor durante un largo periodo de tiempo están limitados a casos aislados o a series cortas de casos. Según estos datos, parece seguro iniciar el tratamiento con anti-TNF tras un mes de tratamiento antiviral (lamivudina, entecavir), el cual debe mantenerse mientras los pacientes reciban la terapia con anti-TNF, aunque siempre ha de realizarse en consenso con el hepatólogo. Durante este periodo, se deben monitorizar cada 4-8 semanas la serología hepática, la carga viral y los niveles de transaminasas séricos para detectar activación de la infección25. Para los pacientes con infección oculta, las directrices son menos claras. Parece que el riesgo de reactivación es bajo, pero se han comunicado dos casos durante el tratamiento con etanercept e infliximab26,27. Kim et al28 demostraron una baja tasa de reactivación de la infección en pacientes con infección oculta, por lo que en estos casos parece suficiente con la monitorización cada 4-8 semanas de niveles de transaminasas séricos, serología y carga viral.
Respecto al resto de biológicos, se han publicado en los últimos años dos casos de pacientes con infección por hepatitis B en tratamiento con rituximab, un paciente con AR y otro con espondilitis anquilosante. No existen datos publicados con otras terapias biológicas.
Vacuna del herpes zósterLa infección por herpes zóster es la complicación viral más frecuente en pacientes con AR en tratamiento con anti-TNF29. La inmunosupresión aumenta las complicaciones asociadas a la infección tales como el riesgo de rash severo, afectación visceral o muerte; sin embargo, la vacuna frente al virus del herpes zóster está compuesta por virus vivos atenuados, por lo que representa un riesgo para desarrollar la infección en pacientes inmunodeprimidos. De ahí, la controversia sobre la idoneidad de su administración en pacientes con AR en tratamiento con inmunosupresores.
El grupo de trabajo del American College of Rheumatology5 desaconseja su administración en este grupo de pacientes. Por el contrario, la CDC Advisory Comitte on Inmunization Practices30 recomienda vacunar a pacientes con AR mayores de 60 años que estén en tratamiento con prednisona (< 20mg/d), metotrexato (< 0,4mg/kg/semana) o azatioprina (< 3mg/kg/día) o que vayan a iniciar tratamiento con biológicos (al menos 15 días antes del comienzo). Todas las guías de manejo de la AR contraindican la vacunación en pacientes que hayan iniciado el tratamiento con biológicos.
Quimioprofilaxis de infección latente por tuberculosisExiste evidencia de una mayor incidencia de TBC en pacientes tratados con anti-TNF respecto a la población general y a la población con AR con otro tipo de tratamientos. Por ello, las recomendaciones nacionales31, establecen que a todo paciente con AR candidato a iniciar terapia biológica se le debe realizar Mantoux con respuesta booster y radiografía de tórax. Hasta el momento, el test de la tuberculina sigue siendo la prueba patrón de oro frente al quantiferon para la detección de TBC latente. De ser positiva la determinación (induración mayor de 5mm), se recomienda iniciar profilaxis con isoniacida durante 9 meses. Transcurrido un mes desde el inicio del tratamiento profiláctico, parece seguro iniciar la terapia biológica.
Se ha descrito que entre el 8-11% de los pacientes positivizan32,33 el Mantoux durante el primer año de tratamiento con anti-TNF, por lo que puede ser aconsejable la repetición periódica (anual) del Mantoux mientras se mantenga este tratamiento, aunque no está establecido cada cuánto tiempo debe realizarse.
ConclusionesLos pacientes con AR tienen mayor riesgo de presentar infecciones, éste se asocia a la propia enfermedad, la comorbilidad y el tratamiento inmunosupresor que precisan.
Este hecho justifica la gran importancia de conductas preventivas como las vacunas y la quimioprofilaxis.
Se ha demostrado que las vacunas frente al virus influenza, neumococo y VHB son seguras en estos pacientes. La efectividad de cada vacuna ha sido evaluada mediante diferentes estudios, en la mayoría de los casos se trata de estudios con grupos pequeños de pacientes que reciben distintos tratamientos, no aleatorizados, y con determinación de respuesta inmunitaria diferente, por lo que no es adecuada la comparación directa. Según los resultados que han obtenido, podemos decir que el porcentaje de respondedores a la vacuna frente a influenza se ve reducido por la AR en sí, y el tratamiento con anti-TNF y rituximab. Por otro lado, la eficacia de la vacuna antineumocócica parece afectarse por la AR y por el tratamiento con metotrexato, rituximab y abatacept. En el caso de la vacuna de la hepatitis B, la respuesta protectora es menor en pacientes con AR y en el tratamiento con anti-TNF.
Tras revisar la información disponible, un calendario de vacunación recomendable en pacientes con AR sería el siguiente:
- –
Vacuna antigripal anual.
- –
Vacuna antineumocócica con repetición cada 3-5 años.
- –
Vacuna de la hepatitis B.
Tal y como se ha comprobado, los tratamientos inmunosupresores pueden reducir la eficacia de la vacuna, por lo que se recomienda vacunar a los pacientes a su diagnóstico, ya que incluso medicamentos de primera línea como el metotrexato reducen la inmunización.
Se están llevando a cabo ensayos clínicos que evalúan la eficacia y seguridad de las vacunas en pacientes con AR tratados con biológicos; los resultados de éstos ampliarán la evidencia clínica de las recomendaciones establecidas en esta revisión.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Nota: Sección acreditada por el SEAFORMEC con 1,7 créditos. Consultar preguntas de cada artículo en: URL: http://www.reumatologiaclinica.org.