La artritis reumatoide (AR) presenta una mortalidad de 1,3-3 veces superior a la población general donde destaca la mortalidad de origen cardiovascular con un 40-50%. Actualmente se considera la enfermedad cardiovascular como una manifestación extraarticular de la AR, siendo un factor de riesgo independiente de los tradicionales, con un riesgo elevado de enfermedad cardiovascular (OR: 1,5-4,0). La medición ecográfica del grosor íntimo medial (GIM) de la arteria carótida común y la presencia de placas ateromatosas es un método no invasivo y marcador subrogado de arterioesclerosis subclínica.
ObjetivoEstablecer si los hallazgos de arterioesclerosis subclínica por ecografía carotídea pueden ser un buen predictor del desarrollo de eventos cardiovasculares (ECV) en una cohorte de pacientes con AR a 10 años.
MetodologíaSe evaluó una cohorte de pacientes con AR atendidos en consulta externa de Reumatología de una hospital de Castilla-La Mancha durante el año 2013. Se realizó una evaluación para el desarrollo de ECV a los 10 años siguientes de comenzado el estudio y se analizó su correlación con los hallazgos ecográficos previos de GIM y placas ateromatosas.
ResultadosOcho (24%) pacientes presentaron un ECV. Tres (9%), episodio de fallo cardiaco; 3 (9%) accidente cerebrovascular y 2 (6%) episodio de infarto agudo al miocardio. Los pacientes con AR que desarrollaron un ECV habían presentado un GIM mayor (0,97±0,08mm) en comparación con los pacientes con AR que no tuvieron complicaciones cardiovasculares (0,74±0,15mm) (p=0,003). La presencia de un GIM≥0,9mm y placas ateromatosas representó un riesgo relativo de 12,25 (p=0,012) y 18,66 (p=0,003), respectivamente, para el desarrollo de un ECV.
ConclusionesLa ecografía carotídea en pacientes con AR nos podría permitir la detección precoz de aterosclerosis subclínica antes del desarrollo de ECV, siendo fundamentalmente el GIM≥0,9mm el hallazgo más asociado a ECV y no influenciado por la edad.
Rheumatoid arthritis (RA) has a mortality rate 1.3–3 times higher than the general population, with cardiovascular mortality accounting for 40%–50% of cases. Currently, cardiovascular disease is considered an extra-articular manifestation of RA (OR: 1.5–4.0). Ultrasound measurement of the intima-media thickness (IMT) of the common carotid artery and the presence of atherosclerotic plaques is a non-invasive method and a surrogate marker of subclinical arteriosclerosis.
ObjectiveTo determine if subclinical arteriosclerosis findings through carotid ultrasound can serve as a good predictor of cardiovascular events (CVE) development in a cohort of RA patients over a 10-year period.
MethodologyA cohort of RA patients seen in the rheumatology outpatient clinic of a hospital in Castilla-La Mancha in 2013 was evaluated. A prospective evaluation for the development of CVE over the following 10 years was conducted, and its correlation with previous ultrasound findings of IMT and atherosclerotic plaques was analyzed.
ResultsEight (24%) patients experienced a CVE. Three (9%) had heart failure, three (9%) had a stroke, and two (6%) experienced acute myocardial infarction. RA patients who developed a CVE had a higher IMT (0.97±0.08mm) compared to the RA patients without cardiovascular complications (0.74±0.15mm) (P=.003). The presence of IMT≥0.9mm and atherosclerotic plaques had a relative risk of 12.25 (P=.012) and 18.66 (P=.003), respectively, for the development of a CVE.
ConclusionsCarotid ultrasound in RA patients may allow for early detection of subclinical atherosclerosis before the development of CVE, with IMT≥0.9mm being the most closely associated finding with CVE, unaffected by age.
Desde hace muchos años es conocido que el estado de inflamación crónica, independiente de su origen y traducido en la presencia de marcadores de inflamación, es considerado un predictor de eventos cardiovasculares (ECV)1. La artritis reumatoide (AR), prototipo de las enfermedades inflamatorias sistémicas crónicas, afecta al 0,5-1% de la población y presenta una mortalidad de 1,3 a 3 veces superior a la población general donde destaca la mortalidad de origen cardiovascular con un 40-50%2. Desde hace varios años se ha puesto de manifiesto, en este grupo de pacientes, el incremento del riesgo de infarto cardiaco (riesgo relativo [RR]: 2,0-2,13) y accidente cerebrovascular (RR: 1,48-1,94)3,4, considerándose actualmente la enfermedad cardiovascular como una manifestación extraarticular de la AR, siendo un factor de riesgo independiente de los tradicionales, con un riesgo elevado de enfermedad cardiovascular (OR: 1,5-4,0)5–8. Es por ello que hace más de una década la Liga Europea contra las enfermedades reumáticas (EULAR, por sus siglas en inglés: European League Against Rheumatism), propuso para la valoración del riesgo cardiovascular (RCV) el SCORE modificado (SCOREm) que consistía en multiplicar por un factor de conversión de 1,5 el resultado obtenido con el SCORE a los pacientes que reúnan 2 de los siguientes 3 criterios9:
- •
Duración de la enfermedad≥10 años.
- •
Factor reumatoide y/o antipéptido cíclico citrulinado positivo.
- •
La presencia de manifestaciones extraarticulares.
Sin embargo, a lo largo de estos años se ha observado cómo esta herramienta subestima dicho riesgo, objetivándose en los grupos clasificados de riesgo bajo e intermedio la presencia de aterosclerosis subclínica por ecografía carotídea y el desarrollo de ECV a corto-mediano plazo hasta en un 12-30%10–12.
Esto llevó a buscar herramientas adicionales que ayuden a identificar más acertadamente el nivel de RCV. De ellas, actualmente, ha cobrado gran relevancia y utilidad clínica el uso de la ecografía carotídea13–15, considerándose la medición del grosor íntimo medial (GIM) de la arteria carótida común y la presencia de placas ateromatosas (PA) un método no invasivo y marcador subrogado de arterioesclerosis subclínica.
Nuestro equipo realizó un estudio hace 10 años en una cohorte de pacientes con AR donde confirmó la falta de correlación entre el SCOREm y los hallazgos de arterioesclerosis subclínica por ecografía carotídea, así como el incremento del RCV por un GIM≥0,9mm y la presencia de PA en los pacientes con AR asociado fundamentalmente al grado de actividad sistémica16,17.
El objetivo del presente estudio fue establecer si los hallazgos de arterioesclerosis subclínica por ecografía carotídea pueden ser un buen predictor del desarrollo de ECV en una cohorte de pacientes con AR a 10 años.
MetodologíaSe evaluó una cohorte de pacientes con AR atendidos en consulta externa de Reumatología de un hospital de Castilla-La Mancha durante el año 2013. El comité de ética institucional local aprobó el estudio y se obtuvo el consentimiento informado de todos los pacientes. La información sobre el perfil clínico, los factores y la estratificación del RCV se ha publicado previamente16,17. La cohorte inicial estuvo compuesta por 119 pacientes (63,8% sexo femenino) con una edad media de 57,43±13,63 años, un Índice de masa corporal promedio de 27,44±5,04kg/m2 y con el siguiente perfil clínico: 25 (21%) fumador, 48 (40,3%) con hipertensión arterial, 36 (30%) con dislipidemia, 4 (3,36%) con diabetes mellitus, 2 (1,68%) con insuficiencia renal, 8 (6,72%) con ECV previo, 56 (47%) tenían más de 10 años de evolución de la enfermedad, 58 (48,7%) factor reumatoide (+), 82 (68,9%) antipéptido cíclico citrulinado (+) y 28 (23,53%) manifestaciones extraarticulares. Un mismo radiólogo vascular, que desconoció en todo momento el grupo de riesgo de cada paciente, realizó la ecografía carotídea según su protocolo habitual de exploración con el mismo ecógrafo Toshiba Aplio XG, modelo Ssa-790A, transductor lineal de 7-10MHz, objetivándose en 31 (31,63%) pacientes la presencia de placa ateromatosa (engrosamiento focal>1,5mm respecto del GIM adyacente) y en 19 (19,39%) pacientes un GIM≥0,90mm (valor promedio obtenido de la distancia existente entre la interfaz luz carotídea-íntima y la interfaz media-adventicia de la pared distal a lo largo de 10mm en 3 puntos distintos de cada arteria carótida), considerados ambos como datos de aterosclerosis subclínica.
A 10 años de la evaluación inicial de los factores de RCV, estratificación del riesgo y realización de la ecografía carotídea en esta cohorte de pacientes, se realizó una revisión del historial clínico y se registraron todos los ECV que se presentaron a lo largo de estos 10 años (no se realizó una nueva estratificación del riesgo ni ecografía carotídea de control). Para esta parte del estudio, los pacientes con antecedentes personales de ECV, hipertensión arterial, diabetes mellitus, dislipidemia, insuficiencia renal, obesidad (índice de masa corporal≥30kg/m2) y fumadores fueron excluidos para conseguir minimizar factores de riesgo que puedan influir en el desarrollo de los ECV. A lo largo de los 10 años del estudio, 2 pacientes descontinuaron seguimiento en nuestro hospital, por lo que el grupo final estuvo compuesto por 33 pacientes. Además de la presentación clínica, la cardiopatía isquémica se confirmó por electrocardiograma y biomarcadores cardiacos, los accidentes cerebrovasculares por resonancia magnética y/o tomografía computarizada cerebral, la enfermedad arterial periférica por Doppler/arteriografía y el fallo cardiaco por radiografía de tórax y marcadores analíticos.
La información recolectada se incluyó en una base de datos de Microsoft Excel diseñada para el estudio. Las variables cuantitativas se presentaron como media y desviación estándar, y las cualitativas como número y porcentaje. Se realizó la prueba de Shapiro-Wilk para evaluar la normalidad de los datos de la variable principal (GIM) y dado que no se objetivó una distribución significativamente diferente de una distribución normal, se utilizó la prueba t de Student para estas variables cuantitativas pareadas. Para evaluar la asociación entre los resultados de los hallazgos ecográficos y el desarrollo de ECV se calculó el RR.
Para observar el comportamiento de los ECV a los 10 años, se complementó la estadística clásica anterior con un diagrama de caja para visualizar cómo varían la distribución, la mediana, los cuartiles y los valores atípicos de la variable GIM, dependiendo de la existencia o no del ECV.
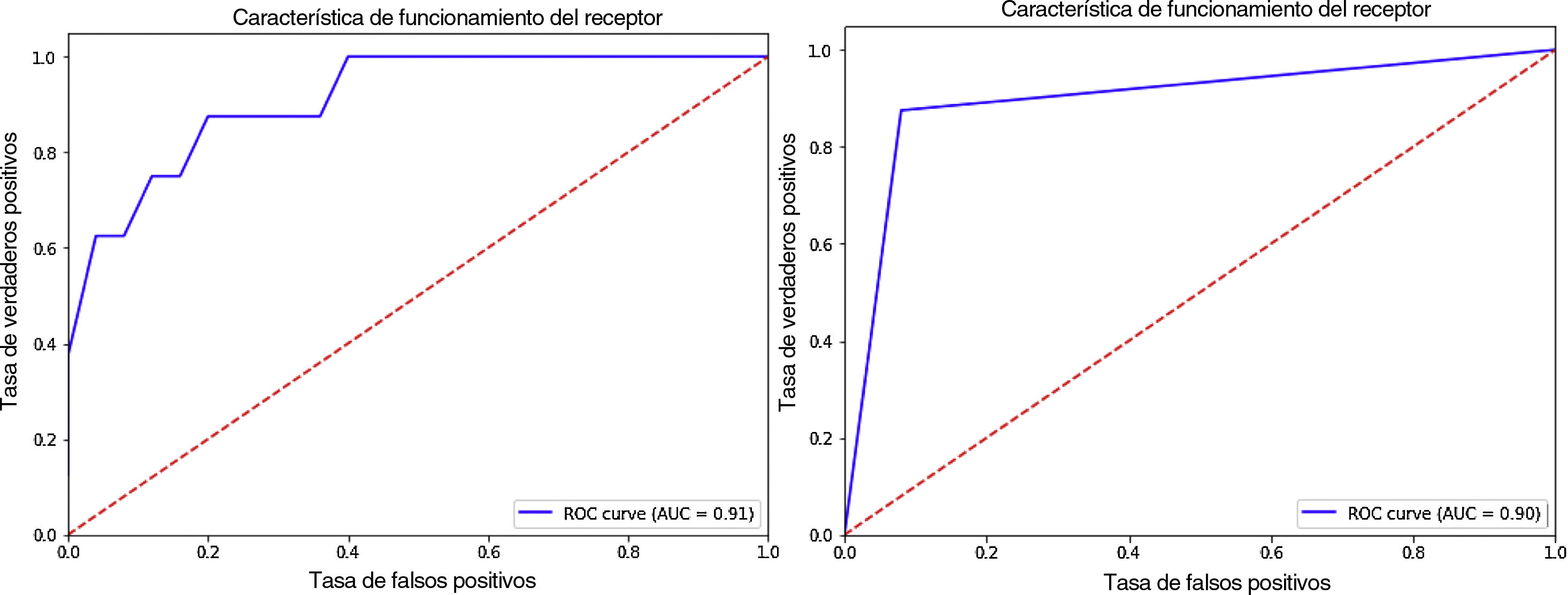
Posteriormente, se hizo una selección de las variables más significativas. Se consideró que el mejor análisis estadístico para tal fin fue el test mutual information18, ya que no solo registra relaciones directas o lineales entre variables, como los test clásicos F o chi, sino que además, capta relaciones complejas, inversas, etc. Una vez seleccionadas las variables más significativas, se examinó sus curvas ROC, clasificando según la presencia ECV o no, a partir de los valores de la variable. Un área bajo la curva alto significó que la variable en estudio (GIM o PA) fue sensible a los ECV.
Todos los análisis se realizaron con un nivel de confianza del 95% usando STATA 12,0.
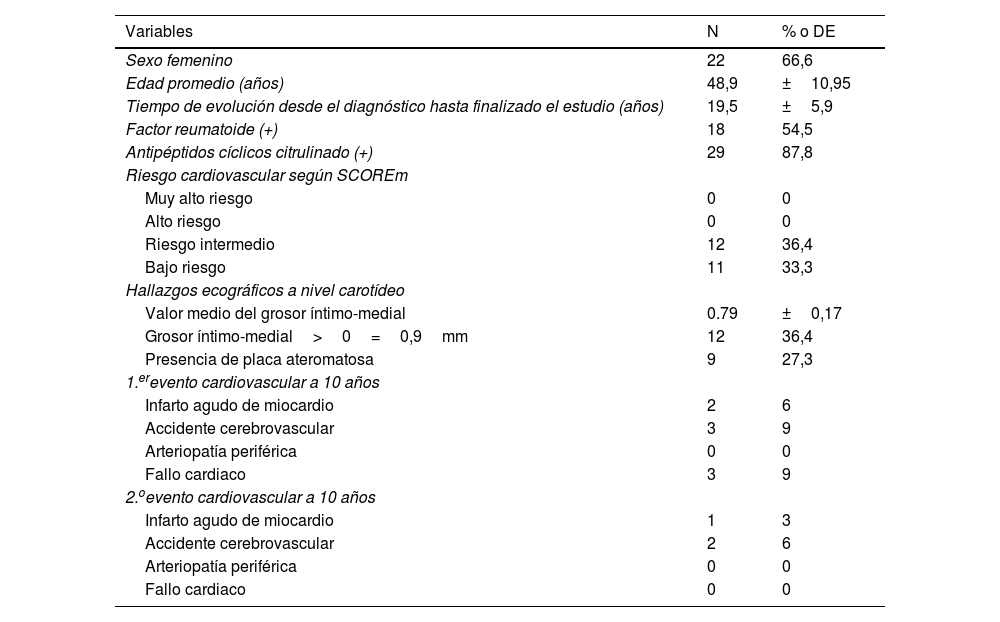
ResultadosA lo largo de los 10 años siguientes a la valoración inicial del RCV mediante el SCOREm y la realización de la ecografía carotídea, 8 (24%) pacientes presentaron un ECV, 3 de ellos presentaron un segundo episodio posterior. Tres (9%) episodio de fallo cardiaco, 3 (9%) accidente cerebrovascular y 2 (6%) episodio de infarto agudo al miocardio. El primer ECV se registró a los 3 años de iniciado el estudio y el último a los 9 años. Para efectos del análisis, se tomó como unidad de medida el paciente no el evento. Solo se registró un fallecimiento a causa de un shock hemorrágico en relación con una úlcera péptica. Las características clínicas se presentan en la tabla 1.
Características clínicas y valoración del riesgo cardiovascular de nuestra cohorte de pacientes con AR (n=33)
| Variables | N | % o DE |
|---|---|---|
| Sexo femenino | 22 | 66,6 |
| Edad promedio (años) | 48,9 | ±10,95 |
| Tiempo de evolución desde el diagnóstico hasta finalizado el estudio (años) | 19,5 | ±5,9 |
| Factor reumatoide (+) | 18 | 54,5 |
| Antipéptidos cíclicos citrulinado (+) | 29 | 87,8 |
| Riesgo cardiovascular según SCOREm | ||
| Muy alto riesgo | 0 | 0 |
| Alto riesgo | 0 | 0 |
| Riesgo intermedio | 12 | 36,4 |
| Bajo riesgo | 11 | 33,3 |
| Hallazgos ecográficos a nivel carotídeo | ||
| Valor medio del grosor íntimo-medial | 0.79 | ±0,17 |
| Grosor íntimo-medial>0=0,9mm | 12 | 36,4 |
| Presencia de placa ateromatosa | 9 | 27,3 |
| 1.erevento cardiovascular a 10 años | ||
| Infarto agudo de miocardio | 2 | 6 |
| Accidente cerebrovascular | 3 | 9 |
| Arteriopatía periférica | 0 | 0 |
| Fallo cardiaco | 3 | 9 |
| 2.oevento cardiovascular a 10 años | ||
| Infarto agudo de miocardio | 1 | 3 |
| Accidente cerebrovascular | 2 | 6 |
| Arteriopatía periférica | 0 | 0 |
| Fallo cardiaco | 0 | 0 |
Los pacientes con AR que desarrollaron un ECV habían presentado un GIM mayor (0,97±0,08mm) en comparación con el resto de los pacientes con AR que no tuvieron ECV (0,74±0,15mm) (p=0,003), no siendo la edad un factor determinante dado que no hubo diferencias (p=1,19) de edad entre los pacientes con un GIM≥0,9mm (49,67±9,86 años) y los que presentaron un GIM<0,9mm (48,48±11,75 años). Asimismo, 7 de los 9 pacientes que presentaron una PA (77,8%), desarrollaron un ECV a 10 años. La presencia de PA sí tuvo una asociación significativa (p=0,0001) con una mayor edad media (60,22±10,15 años) en relación con los negativos para este hallazgo (44,67±7,89 años).
Al analizar la asociación entre el GIM y la presencia de PA como predictor del desarrollo de ECV a lo largo de los 10 años siguientes se objetivó que la presencia de un a GIM≥0,9mm y placa ateromatosa presentaron un RR de 12,25 (p=0,012; IC95%: 1,70-87,98) y 18,66 (p=0,003; IC95%: 2,65-131,23), respectivamente, para el desarrollo de un ECV. Las curvas ROC (fig. 1) confirman la sensibilidad de las variables GIM y PA ante un ECV y muestran unas áreas bajo la curva muy elevadas con valores de 0,91 y 0,90, respectivamente.
Tras analizar las variables tiempo de evolución>10 años (p=0,77), presencia de factor reumatoide (p=0,21) o ACPA (p=0,96) no se objetivó asociación significativa. Sin embargo, como era de esperar, la edad fue un factor determinante y significativo (p=0,009) para el desarrollo de un ECV (57,38±10,47 años) en comparación con los que no presentaron este desenlace (46,2±9,82 años). Los test mutual information nos permitieron identificar las variables más significativas en la aparición de un ECV: SCOREm (0,35), BP=Placa ateromatosa (0,33), Activity=actividad de la enfermedad (0,26) y GIM=grosor íntimo medial (0,22).
DiscusiónLos resultados de nuestro estudio muestran que los hallazgos de arterioesclerosis subclínica mediante ecografía carotídea presentan un alto valor predictivo para el desarrollo de ECV a 10 años en nuestros pacientes con AR sin otros factores de RCV conocidos al momento de la realización del estudio ecográfico, siendo el GIM≥0,9mm el factor determinante no influyendo significativamente por la edad.
Hace más de una década, Gonzalez-Juanatey et al. realizaron un estudio prospectivo a 5 años en una serie de pacientes con AR, objetivando que un 17% presentó un ECV a los 5 años de seguimiento (9% infarto al miocardio, 6% ictus y 2% arteriopatía periférica) y un 6% falleció a causa del ECV19. Otro estudio observó que a los 5 años de seguimiento una cohorte de pacientes con AR presentó un incremento de ECV (3,9% ictus; 1,6% fallo cardiaco y 3,1% infarto al miocardio) que fue significativamente mayor que en una población sana con similares características clínicas y comorbilidades, concluyendo que los pacientes con AR presentan un riesgo de ECV a 5 años de 1,33 (IC95%: 1,07-1,65; p=0,010)20. Finalmente, un estudio reciente realizado por Corrales et al. en 327 pacientes con AR sin otros factores de RCV, observó que el 8,25% presentó un ECV a lo largo de los siguientes 5 años21, mientras que en nuestra cohorte a los 10 años el 24% presentó un ECV (9% episodio de fallo cardiaco, 9% accidente cerebrovascular y 6% episodio de infarto agudo al miocardio).
Con respecto a la ecografía carotídea, Gonzalez-Juanatey et al. observaron un mayor GIM carotídeo en los pacientes con AR que durante el seguimiento experimentaron un ECV (1,01±0,16mm) en comparación con los pacientes con AR restantes que no tuvieron complicaciones CV (0,74±0,12mm) (p=0,001), concluyendo que el GIM carotídeo podría presentar un alto poder predictivo para el desarrollo de ECV durante el período de seguimiento de 5 años, por lo que propusieron realizar una ecografía carotídea a todos los pacientes con AR para establecer un subgrupo de pacientes con alto riesgo de complicaciones CV19. Por otra parte, otro estudio realizado en 138 pacientes con AR que evaluó el valor predictivo del GIM o la presencia de PA determinó que a los 5,8±0,8 años siguientes, 10 pacientes experimentaron un total de 11 (7,97%) ECV. Además de la edad (p=0,01) y la corticoterapia crónica (p=0,01), un GIM elevado (≥0,9mm) estuvo asociado al desarrollo de ECV (p=0,01) con un riesgo de 1,65 (IC95%: 1,27.2,13; p<0,001) por cada incremento de 0,1mm del GIM22. En nuestra cohorte en los pacientes con AR, el desarrollo de un ECV estuvo asociado a un GIM mayor (0,97±0,08mm) en comparación con el resto de los pacientes con AR que no tuvieron complicaciones CV (0,74±0,15mm) (p=0,003), no siendo la edad un factor asociado determinante (p=1,19), lo que le confiere al GIM≥0,9mm un RR de 12,25 (p=0,012; IC95%: 1,70-87,98) y a la PA un RR de 18,66 (p=0,003; IC95%: 2,65-131,23). El riesgo asociado a la presencia de la PA fue mayor al observado en otros estudios que presentaron un riesgo de 5,25 (IC95%:1,41-19,50; p=0,01) de dichos ECV21.
Actualmente, se han publicado más de 2000 artículos donde se observa cómo el GIM carotídeo y la presencia de PA son actualmente buenos predictores del RCV23. Si bien, la edad es un factor que se asocia directamente a un incremento del GIM, considerándose parámetros normales en los varones el límite superior normal entre 0,59mm en los menores de 25 años y 0,95mm en los mayores de 65 años. Mientras que en las mujeres el límite superior normal osciló entre 0,52mm en las menores de 25 años y 0,93mm en las mayores de 65 años24. La ecografía carotídea sigue siendo la técnica de imagen ideal para mejorar la evaluación del riesgo de ECV en pacientes con AR debido a que la mayoría de las calculadoras de RCV desarrolladas subestiman el riesgo de ECV25.
Dada la alta prevalencia de enfermedad cardiovascular en la población con AR4,7, donde se ha demostrado que la actividad de la enfermedad inflamatoria sistémica se asocia a mayor RCV, hallazgos patológicos en la ecografía carotídea, ECV7,16 y que el estado de remisión o baja actividad inflamatoria asociado al control de los factores de RCV tradicionales se correlaciona con la reducción del RCV en este grupo de pacientes5,6,9, es importante la implicación del médico reumatólogo en la valoración del RCV.
Actualmente el uso del ecógrafo es habitual en la práctica clínica de la mayoría de los servicios de reumatología y la ecografía carotídea es una técnica que se ha incorporado a nuestra cartera de servicios como la capilaroscopia, biopsias, etc. Por ello la realización de este procedimiento como una herramienta de bajo coste, no invasiva, dinámica y de rápida realización nos permitirá una correcta estratificación del RCV en nuestros pacientes13,26,27.
ConclusionesLa ecografía carotídea en pacientes con AR nos podría permitir la detección precoz de aterosclerosis subclínica antes del desarrollo de ECV, siendo fundamentalmente el GIM≥0,9mm el hallazgo más asociado a ECV y no influido por la edad. Por todo ello, proponemos que se debería realizar una evaluación ecográfica de la arteria carótida a todos los pacientes con AR para establecer un subgrupo de pacientes con alto riesgo de ECV que requerirán un mejor control de la enfermedad inflamatoria y de los factores de riesgo tradicionales.
LimitacionesA pesar de que el tamaño de la muestra es pequeño, los resultados del estudio muestran resultados similares a los obtenidos por otros estudios de mayor número de pacientes. Asimismo, a pesar de que no se incluyó para el análisis a los pacientes con eventos previos ni factores de RCV tradicionales conocidos, la falta de controles sucesivos a lo largo de los 10 años siguientes al estudio inicial y la edad podrían haber influido también en los resultados.
Conflicto de interesesNinguno de los autores declara conflictos de interés.
El presente estudio no hubiera sido posible sin la dedicación y compromiso de los autores así como el apoyo desinteresado de los servicios de Reumatología y Radiodiagnóstico del Hospital Universitario de Ciudad Real.