Introducción
La terapia biológica dirigida contra el factor de necrosis tumoral (TNF) alfa (antagonistas del TNF*) ha representado uno de los avances más importantes en el campo del tratamiento de las artritis crónicas, como la artritis reumatoide, la artritis psoriásica y la espondilitis anquilosante (EA). Esto es especialmente relevante en esta última enfermedad, en que el arsenal terapéutico era realmente escaso, limitado básicamente a la fisioterapia y el uso de los antiinflamatorios no esteroideos (AINE). Sin embargo, deberíamos preguntarnos si existen suficientes evidencias en la actualidad de que estos fármacos biológicos modifican el curso natural de la enfermedad, es decir son verdaderos fármacos antirreumáticos modificadores de enfermedad (FAME) y si realmente han sido los primeros.
A la hora de evaluar el efecto de las distintas terapias en la EA, deberíamos conocer cuál es exactamente su historia natural. Ésta no es una tarea fácil, debido a la gran heterogeneidad en la expresividad clínica y radiológica de esta entidad. Carette et al1, en un estudio realizado a principio de los años ochenta y después de efectuar un seguimiento a largo plazo de 51 pacientes con EA, concluyen que sólo un 8% llega a una gran discapacidad después de un seguimiento medio de 38 años, a pesar de que casi la mitad de los pacientes te nían una anquilosis vertebral manifiesta; constatan también que los primeros 10 años de evolución de la enfermedad marcarán el pronóstico futuro de estos pacientes.
Estaríamos de acuerdo en considerar que un verdadero FAME sería aquel que pudiera alterar de forma positiva este curso de la enfermedad. Un FAME en la EA debería mejorar de forma sustancial los signos y síntomas de la enfermedad, mejorar la función física y la calidad de vida de los pacientes, tener un efecto notable en los parámetros biológicos de la inflamación y finalmente evitar la progresión del daño estructural (progresión radiológica). Los antagonistas del TNF* han demostrado su efecto positivo en todos y cada uno de estos parámetros, únicamente queda la duda de su efecto real en la progresión de la anquilosis vertebral.
Antagonistas del TNF* en la EA: eficacia clínica contrastada
Los distintos antagonistas del TNF*, actualmente aprobados para el tratamiento de la EA, los anticuerpos monoclonales quiméricos y humanos, infliximab y adalimumab, respectivamente, y el receptor soluble del TNF*, etanercept, han demostrado su eficacia clínica tanto en ensayos clínicos como en estudios observacionales en pacientes con EA resistente al tratamiento con AINE2-6. Además, se ha comprobado que la respuesta clínica es muy rápida, evidente ya en los primeros días de iniciada la terapia y que suele mantenerse a lo largo de los años7, aunque la enfermedad se reactiva a los pocos meses de abandonar la terapia incluso en aquellos en que se logró la práctica remisión clínica de la enfermedad8. Aunque no hay estudios comparativos entre los 3 antagonistas del TNF*, la tasa de respuesta es similar entre ellos (fig. 1).
Figura 1. Porcentaje de mejoría ASAS-20 en 3 ensayos clínicos con anti-TNF controlado con placebo. Resultados a las 12 semanas. Tomado de Braun et al2, Calin et al3 y Van der Heijde et al4.
Además muchos clínicos tienen el convencimiento de que los antagonistas del TNF* son más efectivos en la EA que en otras entidades como la artritis reumatoide. De hecho, todos los estudios que evalúan la tasa de mantenimiento de los biológicos en las distintas enfermedades reumáticas llegan a la misma conclusión. Dicha tasa, que no deja de ser un reflejo indirecto de la efectividad de un fármaco en la práctica diaria, es mejor en la EA que en la artritis reumatoide (AR). Así, en el registro español de fármacos biológicos (BIOBADASER) la tasa de mantenimiento de los antagonistas del TNF* en la EA a los 3 años de su introducción era del 76%, mientras que en la AR era notablemente inferior (65%)9. Por otra parte, un estudio observacional realizado en Noruega, mediante un análisis comparativo sobre la efectividad de los antagonistas del TNF* a 3 y 6 meses de seguimiento, en pacientes con AR y EA, pone de manifiesto que en estos últimos la mejoría de los distintos parámetros de eficacia (grado de dolor, fatiga, discapacidad, calidad de vida) era más evidente que en los pacientes con AR10. Finalmente, los distintos antagonistas del TNF* han demostrado su gran beneficio clínico no sólo en todas las manifestaciones articulares de la enfermedad (afectación axial, periférica y entesitis), sino también en diversas manifestaciones extraarticulares, como uveítis11, amiloidosis12 u osteoporosis13.
Los antagonitas del TNF* producen una reducción rápida y en ocasiones espectacular de los parámetros biológicos de inflamación14 y mejoran de forma significativa diversos parámetros metrológicos (test de Schober, expansión torácica, distancia dedos-suelo, etc.) que inicialmente se creía eran irreversibles3. Diferentes estudios que evalúan la función física y la calidad de vida confirman el efecto beneficioso de los fármacos biológicos en estos parámetros5.
La reciente introducción de la resonancia magnética (RM), como prueba de imagen para valorar el grado de inflamación en las espondiloartropatías, ha sido útil para confirmar el efecto de los fármacos biológicos en la inflamación vertebral y entesítica en la EA. Todos los antagonistas del TNF* han demostrado su capacidad para reducir y, en muchas ocasiones, prácticamente eliminar la inflamación vertebral en los pacientes con EA. En el primer ensayo multicéntrico, a doble ciego y controlado con placebo, infliximab redujo de forma significativa el edema vertebral valorado por RM a las 24 semanas de seguimiento respecto del grupo placebo. En un 63% de los tratados con infliximab, por RM no se observaba inflamación al final del seguimiento, mientras que esto sí se observaba en el 26% de los pacientes que recibieron placebo15.
Con todos estos datos es difícil no considerar a los fármacos biológicos como verdaderos FAME. No obstante, queda pendiente una cuestión importante: ¿estos fármacos son capaces de evitar la progresión de la anquilosis ósea, aspecto patológico y radiológico más característico de esta enfermedad?
Antagonistas del TNF* y anquilosis vertebral
No existe ningún estudio aleatorizado y controlado con placebo dirigido específicamente a evaluar el efecto de los antagonistas del TNF* en la progresión radiológica en la EA. Dicha circunstancia cabe atribuirla a distintas razones: la progresión variable de la enfermedad de un individuo a otro que hace difícil su correcta valoración; la escasa sensibilidad al cambio de los métodos radiológicos utilizados hasta la actualidad, que condiciona que el seguimiento de estos pacientes debe ser a largo plazo (mínimo de 2 años)16, y finalmente, cuestiones estrictamente éticas, ya que es imposible dejar por un período prolongado a pacientes con EA en una rama placebo, sabiendo que existe un tratamiento muy efectivo de la enfermedad.
Una posible solución a este problema sería utilizar, en los distintos estudios comparativos, controles históricos. De hecho, en 2 estudios controlados que intentan responder a la pregunta de si los biológicos son capaces de frenar la progresión de la anquilosis en la EA han utilizado este tipo de controles. Estos controles históricos (cohorte GESPIC de Alemania, con 41 pacientes, y cohorte OASIS de Bélgica, Francia y Alemania, con 186 pacientes) están formados por pacientes con EA evolucionada (media de 5,5 años en la cohorte GESPIC y 11,4 años en la cohorte OASIS) quienes no han sido incluidos en ningún criterio específico, no se los ha tratado con biológicos (sólo AINE y en ocasiones otros FAME, como la sulfasalazina) y de quienes se tiene un seguimiento radiológico anual o bianual, por lo que pueden ser útiles para conocer la progresión radiológica de la enfermedad con tratamiento convencional y sus factores pronósticos16. No obstante, cabe señalar que no dejan de ser controles históricos, con unas características de población distintas (p. ej., con una enfermedad claramente menos activa) de las de los pacientes incluidos en ensayos clínicos a quienes se ha tratado con biológicos, por lo que los resultados extraídos de estos estudios comparativos, aunque orientativos, deben tomarse con cautela.
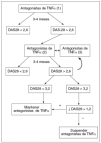
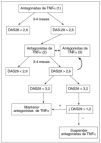
En el primero de estos estudios, que compara a 41 pacientes tratados con infliximab en un ensayo clínico y los 41 pacientes de la cohorte GESPIC, los autores no encuentran una menor progresión radiológica de la enfermedad en los primeros respecto de los segundos después de 2 años de seguimiento, utilizando el índice radiológico de Stokes modificado17. En un subanálisis, donde se incluye sólo a los pacientes con lesión radiológica basal manifiesta, sí hay una tendencia clara de una menor progresión en el grupo tratado con infliximab en comparación con placebo, aunque no llega a alcanzar significación estadística (fig. 2). En otro estudio, hasta la fecha publicado sólo en forma de resumen, no se observaron diferencias significativas en la tasa de progresión radiológica a los 2 años en el grupo de pacientes tratados con etanercept respecto del control histórico de la cohorte OASIS18.
Figura 2. Progresión radiológica a 2 años de seguimiento de 2 grupos de pacientes con espondilitis anquilosante (subgrupo con lesión radiológica basal). Tomado de Baraliakos et al17.
Así pues, cabría concluir que hasta el momento no existe una evidencia científica concluyente de que los antagonistas del TNF* disminuyan la proliferación ósea (anquilosis) en la EA. Esta circunstancia puede deberse simplemente a cuestiones técnicas o metodológicas (falta de estudios aleatorizados con controles adecuados, métodos radiológicos con escasa sensibilidad al cambio, errores estadísticos, etc.), aunque también podría haber una explicación patogenética: que los antagonistas del TNF* mejorarían sustancialmente la inflamación pero no la proliferación ósea; es decir, los procesos de inflamación y proliferación ósea quizá serían independientes o, en todo caso, esta última no debería considerarse como un simple proceso reparativo reactivo al proceso inflamatorio.
Existen ciertas evidencias de que los procesos de inflamación y anquilosis en la EA podrían tener cierto grado de independencia. Así, en un modelo experimental murino, la fenilbutazona evitó la anquilosis ósea con independencia de su acción antiinflamatoria19; más recien temente, Lories et al20, en otro modelo murino de espondiloartritis, demuestran que la inhibición del TNF* con etanercept no incidió en la gravedad o frecuencia de la anquilosis, aunque fue eficaz en controlar la inflamación articular. Probablemente en el proceso de neoformación ósea en la EA estén implicados otros mediadores, como el TGFß21, que explicarían esta aparente disociación entre inflamación y anquilosis ósea.
Finalmente, cabe preguntarse si antes de los biológicos han existido otros FAME en la EA. Es bien conocido que de los diversos FAME útiles en la EA, sólo la sulfasalazina ha demostrado cierta utilidad en las manifestaciones periféricas de la enfermedad22. En cuanto a los AINE, no cabe duda de que han representado una terapia muy beneficiosa para los pacientes con EA y desde su introducción a principios de los años cincuenta han beneficiado a millones de pacientes con esta enfermedad, representando hasta hoy en día la piedra angular del tratamiento. Pero ¿los AINE son verdaderos FAME o sólo es un tratamiento puramente sintomático? No es el objetivo de la presente revisión responder a este tema, pero el reciente estudio controlado que demuestra una inhibición de la progresión del daño radiológico a los 2 años de seguimiento, en pacientes que toman continuamente AINE comparados con aquellos que sólo lo hacen a demanda, cuestiona en parte el concepto de los AINE como fármacos puramente sintomáticos en la EA23.
En resumen, los antagonistas del TNF* son muy efectivos en la EA y representan el avance terapéutico más importante de los últimos cincuenta años en esta enfermedad. Modifican de forma sustancial la historia natural de la enfermedad y cabe considerarlos como verdaderos fármacos modificadores de enfermedad, a pesar de que su efecto en la progresión del daño estructural (anquilosis) esté por demostrar y de que quizá no han sido exactamente los primeros.