Aunque los tratamientos biológicos han supuesto un avance considerable en el protocolo terapéutico de los pacientes con artritis reumatoide (AR), en la actualidad no hay pruebas suficientes que demuestren que el uso de tratamientos con antifactor de necrosis tumoral (anti-TNF), anticuerpos anti CD20 o abatacept como primera línea de tratamiento suponga una clara ventaja a largo plazo en la práctica clínica diaria. Es más, los ensayos clínicos en los que se compara la monoterapia de metotrexato (MTX) frente a la combinación de MTX y anti-TNF han demostrado que el MTX en monoterapia es capaz de inducir la remisión y frenar la progresión radiológica en un porcentaje importante de pacientes con AR de inicio. Por esto, al tomar en cuenta que en 5 o 6 meses se puede saber si un paciente es refractario a MTX, se pueden seleccionar pacientes candidatos a anti-TNF con seguridad, sin tener que exponer a los riesgos de tratamiento combinado a pacientes que podrían evolucionar adecuadamente con monoterapia de MTX.
The development of biologic therapies has improved the prognosis of rheumatoid arthritis (RA). However, at present there is not enough evidence supporting that TNF antagonists, anti CD20 therapy or abatacept used as first line therapy provide relevant long-term benefits in daily clinical practice. Furthermore, clinical trials that analyze the effect of the combination of methotrexate (MTX) plus TNF antagonists against MTX monotherapy have shown that the later provides significant clinical responses and relevant radiological damage arrest in patients with early RA. Therefore, considering that in 5-6 months we can detect which patients do not respond adequately to MTX, we can select those patients for biologic therapy avoiding the exposure to the putative adverse events of combination therapy to those patients with optimal response to MTX monotherapy.
El curso evolutivo de los pacientes con artritis reumatoide (AR) ha cambiado de forma considerable en los últimos 10 años. Es indudable que el desarrollo de los tratamientos biológicos ha desempeñado un papel muy importante en este cambio tan beneficioso para los enfermos. Sin embargo, otros factores pueden haber desempeñado un papel tan importante como el de los tratamientos biológicos en la mejoría del pronóstico de la AR. Entre éstos, destacan 3 factores: a) el reconocimiento de la importancia del inicio precoz del tratamiento con fármacos modificadores de la enfermedad (FAME)1,2, que ha hecho ver a la artritis de reciente comienzo como una «urgencia» médica y llevó a la Sociedad Española de Reumatología (SER) a promover la instauración de Consultas de Artritis de Reciente Comienzo; b) la progresiva generalización de diversas herramientas que permiten evaluar la enfermedad en sus diversas facetas (actividad clínica, discapacidad, progresión radiológica) y tomar decisiones terapéuticas en consecuencia3,4, y c) un empleo más eficaz de los FAME no biológicos que ha favorecido incluso a que aquellos pacientes que no han recibido tratamientos biológicos hayan mejorado su actividad clínica, progresión radiológica y calidad de vida5–7.
Por otra parte, en los últimos años una serie de ensayos clínicos (EC) ha demostrado que el uso del tratamiento con antifactor de necrosis tumoral (anti-TNF) en combinación con metotrexato (MTX) consigue resultados superiores en los pacientes con AR de corta evolución en comparación con el uso de MTX en monoterapia8–10. En la actualidad, se están llevando a cabo EC con otros tratamientos biológicos (anticuerpos CD20 y CTLA-4-Ig) que muy probablemente pondrán de manifiesto parecidas conclusiones. Todos éstos EC, junto con el estudio BEST4,11, que compara diferentes estrategias terapéuticas en pacientes con AR de inicio, han puesto sobre la mesa la cuestión de si es preciso administrar tratamientos biológicos desde el inicio a los pacientes con AR.
En este artículo se presentan las razones por las que el autor cree que no hay motivo para cambiar las recomendaciones dadas en el III Consenso de la SER sobre cuando iniciar los tratamientos biológicos12. Al hacer una aplicación eficaz de estas recomendaciones, un paciente refractario a los FAME no biológicos podría iniciar tratamiento con anti-TNF desde los 6 a 12 meses de su primera visita a una consulta de Reumatología.
Aplicabilidad a la práctica diaria de los ensayos clínicos del tratamiento antifactor de necrosis tumoral en combinación con metotrexato frente a metotrexato en monoterapiaDesde el punto de vista estadístico, no cabe duda de que los pacientes de los grupos de combinación de MTX y anti-TNF presentan un mayor porcentaje de pacientes en remisión, una mejoría más rápida de la capacidad funcional y una menor progresión radiológica que los pacientes del grupo de MTX en monoterapia8–10. Sin embargo, estos resultados no son directamente generalizables a todos los pacientes de la práctica clínica diaria.
En primer lugar, el MTX en monoterapia induce la remisión en aproximadamente un 25% de los pacientes, de forma similar a como lo hacen el adalimumab o el etanercept en monoterapia8,13. Por tanto, estos pacientes no deberían exponerse al riesgo de un tratamiento combinado. Es más, esa cifra de remisión puede ser mayor en la práctica clínica diaria, ya que las poblaciones estudiadas en estos EC son más jóvenes, con formas de AR más grave, tanto en términos de actividad de la enfermedad, como de discapacidad o marcadores de gravedad que los pacientes que se envían desde Atención Primaria a las consultas de artritis de reciente comienzo (tabla 1). De hecho, estos EC excluyen a pacientes de mayor edad y probablemente a aquéllos con comorbilidades14, por lo que de nuevo hay una población de pacientes a los que no serían aplicables los hallazgos obtenidos.
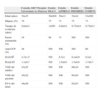
Características de los pacientes incluidos en ensayos clínicos de tratamiento con antifactor de necrosis tumoral en pacientes con artritis reumatoide de inicio
| Consulta ARCa Hospital Universitario La Princesa | Estudio ERA13 | Estudio ASPIRE10 | Estudio PREMIER8 | Estudio COMET9 | |
| Edad (años) | 54±15 | 50±ND | 50±12 | 52±14 | 51±ND |
| Mujeres (%) | 79 | 75 | 71 | 75 | 73 |
| Tiempo de evolución (años) | 0,6±0,4 | 1±ND | 0,9±0,8 | 0,75±0,8 | 0,75±0,3 |
| Factor reumatoide (%) | 54 | 88 | 71 | ND | ND |
| Anti-CCP (%) | 48 | ND | ND | ND | 69 |
| DAS28b | 4,7±1,5 | ND | 6,7±1 | 6,3±0,9 | 6,5±1 |
| HAQ-DI | 1,1±0,7 | ND | 1,5±0,6 | 1,5±0,6 | 1,7±0,7 |
| VGE del médico | 43±25 | ND | ND | 66±18 | ND |
| VGE del paciente | 45±22 | ND | ND | 65±24 | ND |
| EVA del dolor | 48±26 | ND | ND | 62±23 | ND |
ARC: artritis de reciente comienzo; Anti-CCP: anticuerpos antipéptidos cíclicos citrulinados; DAS28: Disease Activity Score ‘Puntaje de actividad de la enfermedad’; EVA: escala visual analógica; HAQ-DI: Health Assessment Questionnaire ‘Cuestionario de evaluación de salud’; ND: no disponible; VGE: valoración global de la enfermedad.
En segundo lugar, los pacientes de los EC tenían un tiempo de evolución mayor que los que llegan a las consultas de artritis de reciente comienzo (tabla 1), por lo que es posible que las tasas de respuesta clínica se hayan resentido al incluir pacientes con tiempos de evolución de hasta 3 años. Esto podría ser más claro en el caso de MTX en monoterapia. En este sentido, en el estudio ASPIRE la remisión (DAS28 inferior a 2,6) fue de un 15% en el grupo de MTX10, mientras que fue del 28% en el estudio COMET9, donde sólo se incluyeron pacientes con evolución menor de 2 años (tabla 1).
Relevancia de la inhibición de la progresión radiológica en pacientes con tratamiento antifactor de necrosis tumoralA diferencia de lo que ocurre con la actividad inflamatoria, donde los anti-TNF en monoterapia no han demostrado ser mejores que el MTX en monoterapia8,13, se ha insistido mucho en la espectacular inhibición de la progresión radiológica de los pacientes con AR tratados con anti-TNF, tanto en monoterapia, como en combinación con MTX8–10,13, e incluso en aquellos pacientes que no tenían respuesta clínica15. Sin embargo, a pesar de que las diferencias con el grupo tratado con MTX en monoterapia son significativas en todos los estudios, en aquéllos en los que se proporcionan datos más detallados (ERA y ASPIRE) puede comprobarse que al menos un 50% de los pacientes tratados sólo con MTX no tienen progresión radiológica10,13. Es más, ambos estudios coinciden en que el 80% de los pacientes tratados sólo con MTX tienen una progresión menor de 5 puntos por año con el método de Sharp10,13. Si se tiene en cuenta que la escala de este método de lectura radiológica oscila entre 0 y 448, parece que una progresión de 5 puntos no es mucho, poco más de un 1%.
Pero, ¿cuál es la mínima progresión clínicamente importante (MPCI) desde el punto de vista radiológico? La contestación que dan los expertos es que para el método de Sharp son 5 puntos16. En este estudio de Bruynesteyn et al, se definió repercusión clínica como la progresión radiológica que induciría a los expertos incluidos en el estudio a cambiar el tratamiento del paciente16. Para los reumatólogos es interesante esta definición de repercusión clínica porque el papel de éstos es recomendar al paciente un cambio de tratamiento cuando se cree que la enfermedad no evoluciona adecuadamente con los datos objetivos de los que se dispone. Sin embargo, es posible que desde el punto de vista del paciente la MPCI sea diferente.
Dos estudios han confirmado que el hecho de ser mujer, tener valores elevados de actividad inflamatoria, la edad y el deterioro radiológico se asocian a una mayor discapacidad medida por el HAQ (Health Assessment Questionnaire ‘Cuestionario de evaluación de salud’)17,18. Sin embargo, en el estudio de Welsing et al se pone de manifiesto que esta asociación no es directa, sino que depende de la edad y en menor medida del daño radiológico basal17. En este estudio se indica que para los pacientes en los que la AR se inicia a partir de los 75 años, la MPCI es de 20 puntos, para los pacientes en los que la AR comienza a los 55 años, la MPCI es de 6 a 7 puntos, mientras que para los pacientes que tienen 35 años cuando comienza la enfermedad, la MPCI es de 4 puntos17.
Conclusiones del estudio BESTDesde el punto de vista del autor de este artículo, el estudio BEST4,11 ha confirmado lo que ya parecía claro con el estudio TICORA3: para conseguir controlar la actividad de la AR lo que hay que hacer es proponérselo. Da igual cuál sea la estrategia que se elija, lo importante es ponerse un objetivo ambicioso. Es cierto que algunas estrategias a largo plazo cursaron con una peor progresión radiológica, pero en la práctica clínica diaria se tiene la ventaja de que si el paciente no ha respondido adecuadamente en 5 o 6 meses, puede iniciarse precozmente un tratamiento con anti-TNF. Como se ha visto anteriormente, en estos 5 o 6 meses muchos de los pacientes estarán en remisión con un FAME no biológico en monoterapia si éste se aplica de forma intensiva. Además, no hay que preocuparse por su progresión radiológica, ya que en ese período de tiempo menos de un 10% de los pacientes tendrán un deterioro articular clínicamente relevante.
Opinión personalEn resumen, el MTX en monoterapia es un fármaco capaz de controlar eficazmente la actividad de la enfermedad en un porcentaje elevado de los pacientes que acuden a las consultas de artritis de reciente comienzo. Además, esperar de 5 a 6 meses para comprobar que los pacientes responden al FAME en monoterapia no supone un deterioro radiológico clínicamente significativo.
El autor de este artículo cree que se debe continuar fomentando el establecimiento de unidades de artritis de inicio que faciliten la llegada precoz de los pacientes. Lógicamente, esto requiere una estrecha colaboración con la Atención Primaria y permitirá iniciar tratamiento con FAME de forma muy precoz. Este tratamiento debe ser intensivo y ajustado a objetivos ambiciosos: remisión o mínima actividad de la enfermedad. Por otra parte, dada la poca sensibilidad de los criterios del ACR (American College of Rheumatology) para la clasificación de la AR en los casos precoces y considerando la seguridad demostrada por fármacos como el MTX, no debe escatimarse este tratamiento a los pacientes con artritis indiferenciada19. Lo más que puede ocurrir es que, en algunos pacientes, después de unos meses de remisión se lo pueda suspender sin recaídas de la artritis.
Por último, es cierto que en la actualidad se dispone de marcadores que indican que los pacientes con artritis indiferenciada o AR de inicio tienen más posibilidades de evolucionar a formas de AR más destructivas. La presencia del factor reumatoide o de anticuerpos antipéptidos cíclicos citrulinados positivos y una mayor carga inflamatoria (la velocidad de sedimentación globular o la proteína C reactiva elevadas) desde el inicio de la enfermedad pueden indicar que los pacientes necesitarían una actitud terapéutica más intensiva19. En este sentido, el tratamiento combinado desde el inicio es una opción. Es cierto que el tratamiento tipo COBRA no agrada a pacientes ni a reumatólogos, pero se dispone de 6 combinaciones de FAME que han demostrado ser superiores a sus respectivas monoterapias: anti-TNF y MTX, MTX y leflunomida, MTX y ciclosporina A, MTX y sales de oro parenterales, el triple tratamiento, y la combinación de sulfasalacina y con leflunomida (véase GUIPCAR [Guía de la práctica clínica de la artritis reumatoide], tabla 24, pag. 98–9). La experiencia de EMECAR dice que los 2 primeros tratamientos son los preferidos por los reumatólogos españoles7.
Sin embargo, la presencia de marcadores de gravedad no indica que el tratamiento vaya a ser más efectivo en cada paciente. Por esto, el futuro está en el desarrollo de biomarcadores terapéuticos que permitan determinar qué FAME es el más adecuado para cada paciente. Esto permitirá ahorrar tiempo hasta conseguir el control de la enfermedad y evitará exponer al paciente a efectos secundarios innecesarios.