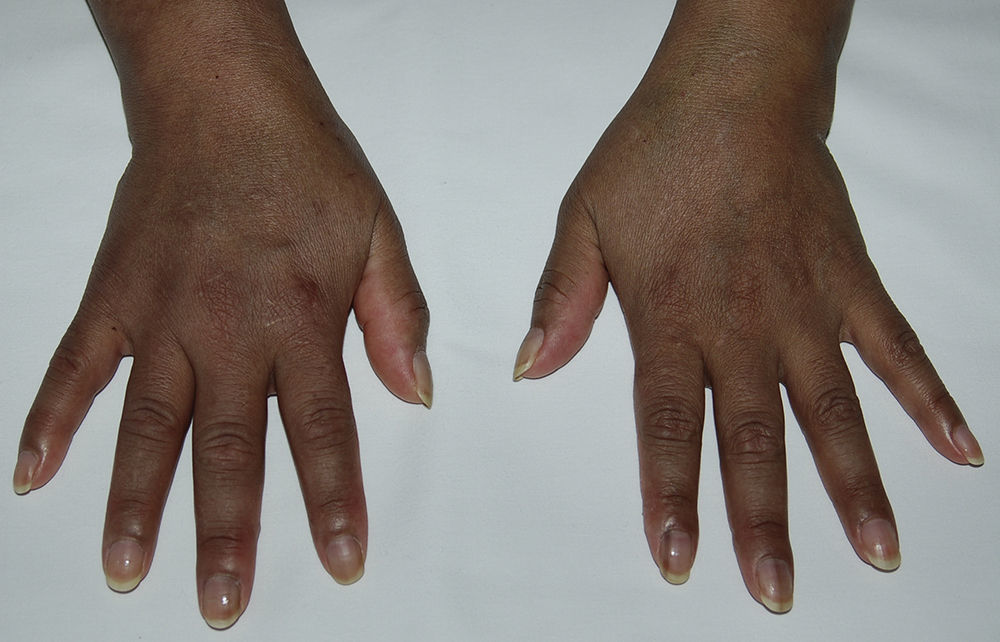
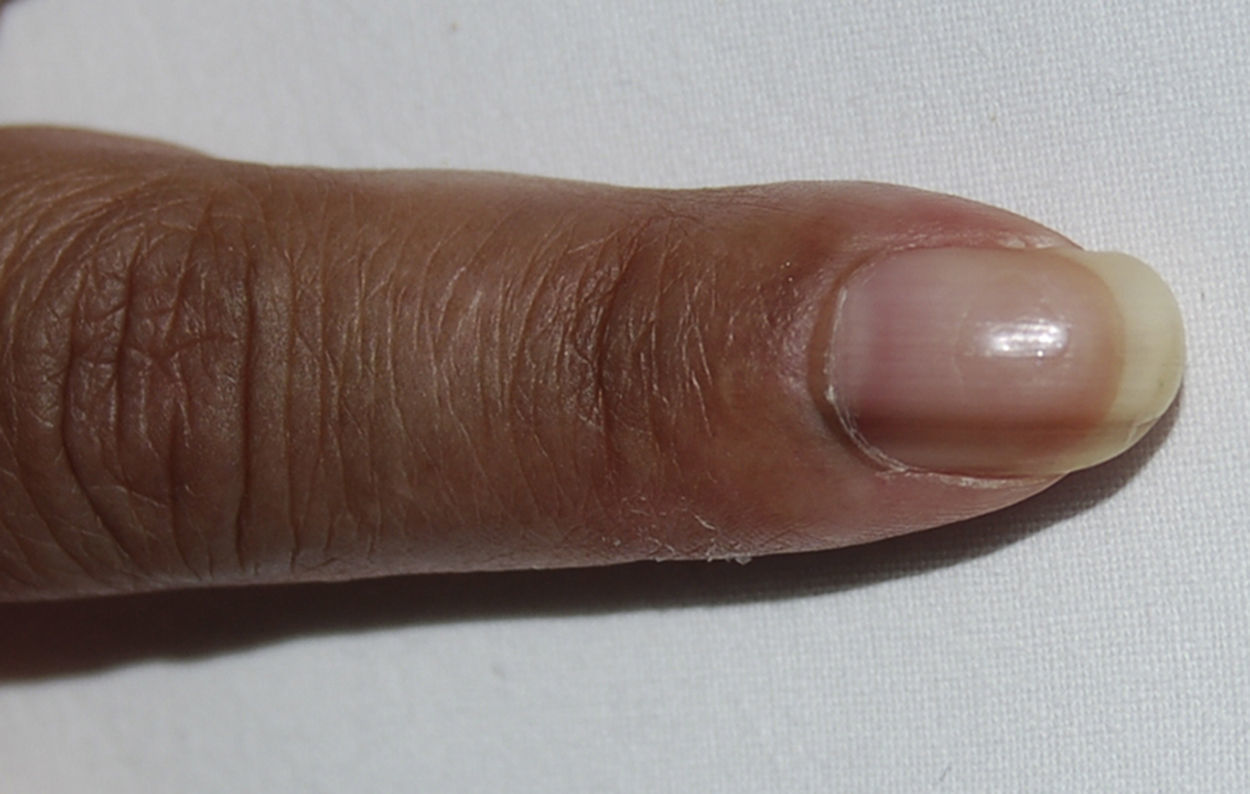
Una mujer de 48 años, originaria de Ecuador, fue diagnosticada de lupus eritematoso sistémico (LES) en marzo del 2004 basándose en poliartritis simétrica que afectaba a los carpos y las articulaciones pequeñas de las manos, aftas orales, anemia hemolítica Coombs positivo, leucopenia y positividad para anticuerpos antinucleares, anti-ADN, anti-Sm, antirribonucleoproteína, anti-Ro/SSA y anticardiolipina IgM e IgG. En mayo del 2004 desarrolló proteinuria con biopsia renal compatible con nefritis lúpica clase iii-C (esclerosante focal)1. Se inició prednisona 1mg/kg/día en pauta descendente y azatioprina 100mg/día, con buena respuesta clínica, pero este último fármaco fue suspendido temporalmente en mayo del 2009 por herpes zóster y definitivamente en octubre del 2010 por linfopenia persistente. En ese momento, se agregó hidroxicloroquina 200mg/día, desarrollando hiperpigmentación tras 12 meses de administración del fármaco. La exploración física mostraba pigmentación gris azulada generalizada, más intensa en el rostro y el dorso de las manos (fig. 1), así como bandas longitudinales de similares características en las uñas del 2.° dedo de la mano izquierda y el 3.° de ambas manos (fig. 2). No se evidenció hiperpigmentación en las mucosas. Los estudios analíticos, incluyendo bioquímica, hemograma, estudios hormonales (hormona tiroestimulante, cortisol, ACTH) y reactantes de fase, se encontraban en rangos normales. Tras descartar razonablemente otras causas de hiperpigmentación generalizada, incluyendo a la enfermedad de Addison2, se atribuyó este evento al tratamiento con hidroxicloroquina. Sin embargo, se decidió continuar con este fármaco, a pesar de las implicaciones estéticas, debido al riesgo de reactivación del LES tras su retirada3, permaneciendo la pigmentación estable durante el seguimiento y sin desarrollar complicaciones oculares.
Los antimaláricos, cloroquina e hidroxicloroquina, son fármacos de primera línea en el tratamiento del LES debido a su capacidad de prevenir las exacerbaciones, incluidas las graves, además de su efecto adyuvante para inducir o mantener la remisión, mejorar el perfil metabólico, reducir el riesgo trombótico y no inducir inmunosupresión4. Los eventos adversos asociados a estos fármacos por lo general son leves y reversibles, siendo uno de los más frecuente la hiperpigmentación mucocutánea, que ocurre hasta en el 10 al 25% de los casos5. Este evento es dependiente de la dosis, pudiendo afectar al mentón, el rostro, el paladar duro, el tronco y el lecho ungueal6. A nivel cutáneo, se presenta como máculas o placas confluyentes de coloración que varía de gris azulada a morado oscuro y que aparecen aproximadamente desde los 4 meses de tratamiento7. En nuestro caso, la hiperpigmentación fue difusa, no siendo esta la presentación habitual. Sin embargo, se han descrito casos con extensas áreas afectadas, cubriendo completamente las extremidades y el torso8. La afección ungueal es menos frecuente y puede manifestarse como bandas hiperpigmentadas (melanoniquia longitudinal) o ser difusa9. La pigmentación cutánea tiende a disminuir progresivamente en los meses siguientes a la retirada del antimalárico5, pero las lesiones ungueales tienen a persistir durante años, aunque pueden disminuir de intensidad10. El mecanismo por el que estos fármacos producen hiperpigmentación es desconocido, pero se ha indicado que su afinidad por la melanina puede dar lugar a su acumulación en la piel6. En el diagnóstico diferencial de la hiperpigmentación cutánea difusa se deben de tener en cuenta los trastornos metabólicos (hemocromatosis, porfiria cutánea tarda, pelagra), neoplasias (carcinoma pulmonar, melanoma metastásico, micosis fungoides), endocrinopatías (enfermedad de Addison, síndrome de Nelson, síndrome de secreción de ACTH ectópica, hipertiroidismo), enfermedades autoinmunes (esclerosis sistémica, cirrosis biliar primaria), intoxicación por metales pesados (oro, plata) y fármacos (colpromacina, amiodarona, tetraciclinas)2.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.