Glucocorticoides, aspirina, antipalúdicos e inmunosupresores convencionales constituyen la base del tratamiento del lupus eritematoso sistémico (LES). Hasta recientemente, los 3 primeros eran los únicos agentes aprobados para su tratamiento. El mejor conocimiento de la fisiopatología del sistema inmunitario ha permitido identificar nuevas dianas terapéuticas. De hecho, belimumab, un anticuerpo monoclonal humano inhibidor de BLyS, se ha convertido hace pocos meses en el primer fármaco aprobado para el tratamiento del LES desde 1957, lo que subraya las dificultades de todo tipo, incluyendo las económicas y organizativas, inherentes a los ensayos clínicos sobre esta enfermedad. Otras muchas moléculas se encuentran en distintas fases de desarrollo y en poco tiempo dispondremos de resultados concretos. En esta revisión repasamos el mecanismo de acción y los datos clínicos más relevantes de estas moléculas.
Glucocorticoids, aspirin, antimalarials and conventional immunosuppressants are the mainstay of treatment of Systemic Lupus Erythematosus (SLE). Until recently, the first three were the only agents approved for treatment. A better understanding of the pathophysiology of the immune system has identified new therapeutic targets. In fact, belimumab, a human monoclonal antibody to BLyS inhibitor has become, in recent months, the first drug approved for the treatment of SLE since 1957, underscoring difficulties of all kinds, including economic and organizational ones inherent to clinical trials on this disease. Many other molecules are in various stages of development and soon will have concrete results. In this review, we examined the mechanism of action and most relevant clinical data for these molecules.
En los últimos 15 años ha disminuido significativamente la mortalidad del lupus eritematoso sistémico (LES), que sin embargo continúa siendo muy importante. Bernatsky et al.1 siguieron la evolución de 9.547 pacientes durante un promedio de 8,1 años y encontraron una tasa de mortalidad estandarizada (relación entre muertes observadas y muertes esperadas o TME) global de 2,4, siendo mayor en el grupo de los pacientes menores de 40 años (TME: 10,7) y en los que tenían un tiempo de evolución de la enfermedad menor de 1 año (TME: 5,4); entre las causas de mortalidad, las más importantes continuaban siendo la nefritis lúpica (NL) (TME: 7,9) y las infecciones (TME: 5,0). En contraste con la gravedad de estos indicadores, el arsenal terapéutico para esta enfermedad hasta hace unos meses estaba exclusivamente constituido por la aspirina, la hidroxicloroquina y los glucocorticoides; los restantes fármacos utilizados, incluyendo la ciclofosfamida, la azatioprina, el micofenolato mofetilo, la ciclosporina A y el metotrexato, no han sido aprobados para el LES y tienen un efecto inmunosupresor indiscriminado que con frecuencia conlleva efectos adversos graves e infecciones oportunistas. A pesar de ello, el empleo de estos fármacos off label, junto con el mejor manejo de las comorbilidades habituales en esta enfermedad, tales como hipertensión, dislipemia, síndrome nefrótico, etc., ha mejorado considerablemente su pronóstico a largo plazo, aunque debido a su estrecho margen terapéutico una cierta proporción de pacientes presentan efectos adversos que empeoran su calidad y esperanza de vida, muchos no logran un control adecuado de la enfermedad y otros presentan brotes frecuentes2. Por estas razones, la investigación de nuevos tratamientos continúa siendo una necesidad universalmente reconocida. Afortunadamente, el mejor conocimiento de los mecanismos patogénicos implicados en ella está permitiendo identificar nuevas dianas que podrían mejorar la eficacia y seguridad de los tratamientos actuales3, aunque persisten las dudas acerca de su coste-efectividad y de su seguridad a largo plazo.
Una panorámica sobre la fisiopatología del lupus sistémicoEn la patogenia del LES hay al menos 2 compartimentos bien diferenciados. Por un lado, la fisiopatología de la autoinmunidad y su consecuencia, los autoanticuerpos, que parecen el resultado de una interacción entre factores genéticos y ambientales exógenos o endógenos, que inciden sobre el sistema inmunitario para desencadenar la secuencia de eventos que conduce a la exacerbación de un fenómeno fisiológico, que es la autoinmunidad. Se reconoce que en esta exacerbación de la respuesta inmunitaria los antígenos nucleares y sus correspondientes autoanticuerpos desempeñan un papel amplificador tanto a través de los mecanismos de la inmunidad adquirida, como de los de la inmunidad innata. El segundo compartimento de la patogenia del LES es el desarrollo de inflamación y daño en los órganos diana4.
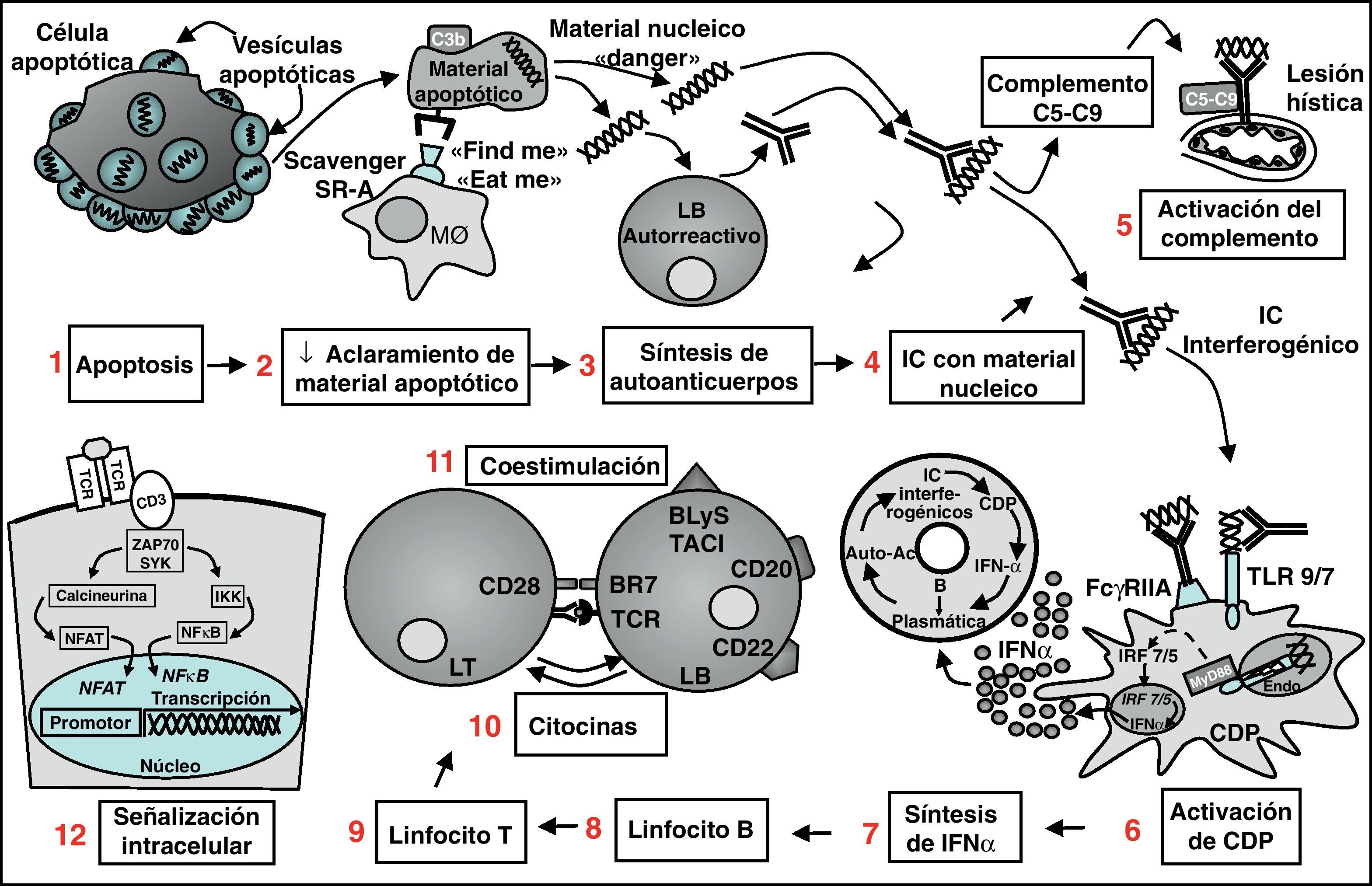
Las células apoptóticas parecen ser el origen de los autoanticuerpos (fig. 1); específicamente, las vesículas apoptóticas que se exponen en la superficie de la célula que entra en apoptosis y que contienen restos celulares, entre ellos ácidos nucleicos y nucleótidos. En circunstancias normales el sistema mononuclearfagocítico, particularmente los macrófagos, se encarga de retirar de la circulación esos restos apoptóticos. En este proceso participa el sistema del complemento, a través de la opsonización de las partículas apoptóticas por su factor C3b5. Intervienen también otras moléculas secretadas por la propia célula en apoptosis, como la lisofosfatidilcolina, que permite atraer a los fagocitos (señales find-me) y moléculas expuestas en su superficie como la fosfatidilserina oxidada, que son reconocidas por receptores scavenger (carroñeros) en la superficie del fagocito, como CD36 y oxLDL, facilitando su internalización (señales eat-me)6. En el LES existe tanto un incremento de la apoptosis como un aclaramiento deficiente de células apoptóticas y ambas alteraciones conducen a la acumulación de material necrótico secundario, capaz de desencadenar inflamación, y de fragmentos nucleares modificados que son identificados como señales de peligro por el sistema inmunitario (danger signals), el cual pondrá en marcha la síntesis y la secreción de anticuerpos dirigidos a su neutralización por parte de linfocitos B (LB) autorreactivos6.
Visión panorámica de la patogenia del Lupus sistémico. La célula apoptótica expone en su superficie las vesículas apoptóticas conteniendo antígenos nucleares (1); debido a un deficiente aclaramiento de las partículas apoptóticas por el sistema mononuclearfagocítico, aquellas se acumulan (2) y ganan acceso a los linfocitos B autorreactivos, los cuales sintetizan autoanticuerpos (3); los IC formados por esos anticuerpos y sus respectivos antígenos nucleicos (4) tienen capacidad para activar el complemento y conducir a lesiones en los tejidos (5) y también para activar a las CDP (6); las CDP responden con la producción de IFN-( por vías dependientes de TLR7 y TLR9 (7); IFN-α tiene múltiples efectos sobre el sistema inmunitario que favorecen el desarrollo de autoinmunidad, como la diferenciación de linfocitos B a células plasmáticas productoras de anticuerpos, la activación de células T y la maduración de las células dendríticas. Todo ello conduce a un círculo reverberante que intensifica y perpetúa el proceso autoinmunitario. Otras dianas terapéuticas están representadas por los LB (8) los LT (9), las citocinas (10), las moléculas de coestimulación (11) y las vías de señalización intracelular (12). CDP: células dendríticas plasmocitoides; IC: inmunocomplejos; IFN: interferón; LB: linfocito B; MØ: macrófago; TCR: receptor de células T; TLR: toll-like receptor.
Tras la secreción de autoanticuerpos y su unión a los antígenos nucleares se forman los correspondientes inmunocomplejos (IC), fundamentalmente ADN/anti-ADN, con capacidad para depositarse en los tejidos donde, con la participación del sistema del complemento, provocarán lesiones como ocurre típicamente en el glomérulo renal7. Estos IC que contienen productos nucleicos son también captados por las células dendríticas plasmocitoides (CDP) por medio de los receptores Fcγ-IIAr e interiorizados en los endosomas. Los receptores toll-like (TLR) 7 y 9, anclados en la membrana del endosoma, son activados por estos IC e inician la cascada de la transducción que conduce a la activación de los factores de transcripción IRF 7/5 y NFκB, con la consiguiente producción de grandes cantidades de IFN-α —las CDP son las productoras «profesionales» de IFNα— y, en menor medida, de otras citocinas proinflamatorias, como la IL-68. Esta capacidad de los IC con contenido nucleico para desencadenar una respuesta de IFN por parte de las CDP, justifica que se los denomine «complejos interferogénicos». Es de interés que la hidroxicloroquina, uno de los más antiguos fármacos utilizados en el LES, inhibe la unión de las cadenas de ácidos nucleicos a estos TLR a través de la elevación del pH del endosoma9 y, por tanto, son fármacos inhibidores de los TLR.
El IFN-α secretado por las CDP tiene efectos que favorecen la autoinmunidad: promueve la maduración de las células dendríticas, activa los linfocitos T (LT) (incluidos linfocitos autorreactivos, que pueden haber escapado a la tolerancia central) e interviene en la diferenciación de LB a células plasmáticas productoras de autoanticuerpos, lo cual a su vez implica una mayor formación de IC interferogénicos. De esta manera, el IFN-α es un gran activador del sistema inmunitario y con su aparición en escena se completa un circuito (fig. 1) en el que al aumentar la presencia de células plasmáticas se incrementa la síntesis de autoanticuerpos, se forman más IC conteniendo ácidos nucleicos y se activan más CDP, las cuales van a producir más IFN-α, cerrándose así un círculo reverberante que mantiene y multiplica los mecanismos de autoinmunidad.
Estudios con microarrays de oligonucleótidos han puesto de manifiesto en los pacientes con LES una sobreexpresión de genes relacionados con el IFN y con la granulopoyesis (véase más adelante), lo que apoya la hipótesis de que el IFN-α desempeña un papel protagonista en la fisiopatología de esta enfermedad.
Dianas terapéuticasLa investigación de nuevas dianas persigue la intervención terapéutica específica en puntos concretos de las vías patogénicas, evitando así el mecanismo de los inmunosupresores convencionales con los que, junto al efecto perseguido, se desencadenan otros no deseados. Los fármacos que se están investigando actualmente en el LES y en otras enfermedades autoinmunitarias, están dirigidos tanto a dianas celulares, incluyendo las moléculas de superficie del LB (CD20, CD22 y CD19) y las moléculas de coestimulación (CTLA-4, CD40/CD40L, ICOS/B7-H2), como a dianas extracelulares (citocinas, quimocinas) e intracelulares, es decir, a moléculas que intervienen en las rutas de transducción y transcripción, así como al proteosoma.
La accesibilidad a muchas de estas dianas ha sido posible gracias al advenimiento de los llamados fármacos biotecnológicos: anticuerpos monoclonales y proteínas de fusión recombinantes. Los anticuerpos monoclonales, usualmente de clase IgG, se identifican por su terminación «mab» (de monoclonal antibody); el sufijo «omab» indica que se trata de un anticuerpo murino; «ximab» se refiere a los anticuerpos quiméricos (aproximadamente un 30% de origen murino); «zumab», a los humanizados (menos del 10% de origen murino), y «umab» se refiere a los anticuerpos completamente humanos. Por su parte, el sufijo «cept» se utiliza para referirse a las proteínas de fusión obtenidas por técnica recombinante. A estos fármacos biotecnológicos hay que añadir los SMIP (small modular immunopharmaceuticals), polipéptidos que en una única cadena integran el dominio de unión, el efector y la zona bisagra, exactamente igual que una inmunoglobulina, pero de un tamaño mucho más pequeño y, por tanto, con mejor penetración en los tejidos y en las células10. Las dianas intracelulares como tyrosine kinases y Janus kinases, entre otras, son inhibidas mediante compuestos químicos, no biotecnológicos, de bajo peso molecular (<1kDa), llamadas «pequeñas moléculas», frecuentemente denominadas con el sufijo «inib» (de inhibidores) o «imod» (de inmunomoduladores). Además de su menor tamaño, las pequeñas moléculas presentan las ventajas sobre los fármacos biotecnológicos, de su menor coste, su administración oral y la ausencia de inmunogenicidad y su secuela, la formación de anticuerpos humanos anti-quiméricos (HACA) o anti-humanos (HAHA), que inhiben la acción del fármaco.
TolerágenosComo se señaló más arriba, el aclaramiento deficiente de restos apoptóticos con contenido nucleico, junto a una pérdida de la tolerancia son considerados los factores que determinan la formación de anticuerpos frente a componentes nucleares11. Una diana que ha atraído la atención de los investigadores es precisamente conseguir que estos restos nucleicos danger pierdan su capacidad inmunógena, es decir, tolerizarlos, con la pretensión de que no desencadenen una respuesta de autoanticuerpos. Con esa finalidad se han utilizado los llamados «tolerágenos». Entre ellos, abetimus y edretide han tenido un cierto recorrido, pero su desarrollo se interrumpió ya que, a pesar de disminuir la producción de autoanticuerpos, no parecen mejorar la enfermedad.
- –
Abetimus (Riquent®, Rentol®). Se trata de una molécula sintética formada por 4 secuencias de desoxinucleótidos unidas a una base de polietilenglicol, con capacidad para establecer enlaces cruzados con los receptores de los LB ADN-específicos en ausencia de linfocitos T e inducir anergia o apoptosis. Probado en múltiples ensayos en el LES, se ha mostrado capaz de disminuir la concentración de anticuerpos anti-ADN y de normalizar el complemento12; sin embargo, no acorta el tiempo hasta un nuevo brote de nefritis, por lo que su desarrollo se detuvo después de que el ambicioso ensayo ASPEN, en 890 pacientes con NL, fuera interrumpido por ineficacia en 2009.
- –
Edratide (TV-4710). Algo similar ocurrió con edratide, un péptido sintético de 19 aminoácidos con una secuencia basada en la región complementaria determinante 1 (hCDR1) de un anticuerpo anti-ADN monoclonal13, cuyo desarrollo fue suspendido por ineficacia tras el ensayo PRELUDE en 2007.
- –
Lupuzor (P140, IPP-201101, Rigerimod). El fosfopéptido 140 formado por los residuos fosforilados 131-151 de la proteína de 70K del spliceosoma dentro del antígeno U1-RNP tiene un mecanismo de acción no completamente entendido, pero al parecer actúa induciendo anergia o deleción en los linfocitos T autorreactivos, antagonizando de forma parcial o total el receptor de las células T (TCR) o a través de un efecto sobre los LT reguladores (Treg). Los resultados de un estudio fase IIb demuestran que además de ser seguro y bien tolerado, es capaz de reducir la actividad clínica y biológica del LES14. Actualmente, está en marcha un ensayo fase III que busca la confirmación de estos resultados.
El sistema del complemento desempeña un doble papel en la fisiopatogenia del lupus: sus componentes iniciales intervienen en la opsonización y el aclaramiento de los cuerpos apoptóticos, de manera que los déficits de esos primeros componentes conducen a la acumulación de material danger y predisponen a desarrollar la enfermedad. Por su parte, los componentes terminales intervienen en el proceso inflamatorio que conduce al daño en los tejidos y se asocian a las manifestaciones clínicas y la progresión de la enfermedad a juzgar por la elevación de los niveles séricos de C5a y C5b-C9 durante los brotes15. En los modelo murinos, la administración de anti-C5 mejora la evolución de la enfermedad renal, retrasa la aparición de proteinuria y aumenta la supervivencia. Por esas razones, la inhibición de la activación de la secuencia terminal del complemento, conservando la cascada inicial, constituye una diana atractiva.
- –
Eculizumab (Soliris®). Anticuerpo monoclonal humanizado que bloquea C5 impidiendo su partición en los fragmentos proinflamatorios C5a y C5b, aprobado actualmente para el tratamiento de la hemoglobinuria paroxística nocturna. Cuenta con un ensayo clínico fase I de 56 días en pacientes con LES, en el que demostró ser seguro y bien tolerado, y produjo una tendencia a la mejoría durante ese breve periodo15. Sin embargo, el riesgo de infecciones meningocócicas que representa la inactivación de la secuencia terminal del complemento puede suponer una limitación para su uso humano. A pesar de ello, actualmente se encuentra en marcha un ensayo fase II para evaluar su eficacia en la nefropatía membranosa lúpica.
- –
Otros inhibidores del complemento. Otro anticuerpo monoclonal frente a C5, denominado pexelizumab, se ha ensayado en el infarto agudo de miocardio y un antagonista recombinante del receptor humano de C5a (C5aRAM; CGS 27913) ha demostrado mejorar la nefritis en el modelo murino MRL/lpr16, pero por el momento ninguno de ellos se ha ensayado en humanos.
Las células dendríticas son un grupo celular heterogéneo derivado de la médula ósea, que participa en la inmunovigilancia, la presentación de antígenos y la tolerancia. Comprenden 2 subtipos, las células dendríticas convencionales y las CDP, siendo estas últimas las que han demostrado tener un papel protagonista en la patogenia del LES8. Las CDP participan en la inmunidad innata contra virus y bacterias intracelulares a través de sus receptores toll-like TLR7 (receptor para ARN monocatenario) y TLR9 (receptor para ADN hipometilado), localizados en el endosoma, y cuya activación resulta en la secreción de interferones tipo I y entre ellos, IFN-α17. Las grandes cantidades de IFN-α encontradas en los pacientes con LES, desproporcionadas a la baja concentración de CDP en sangre periférica, son atribuidas a la presencia de CDP activadas en ganglios linfáticos, piel y otros órganos diana8.
- –
IRS 954. Se ha probado indirectamente el potencial de las CDP como diana terapéutica en el LES a través de la inhibición de los TLR, pretendiendo con ello frenar el inicio de la señalización intracelular que culminará en la síntesis de IFN-α por estas células y evitando, por tanto, su producción. Los oligo-desoxi-nucleótidos (ODN) que contienen secuencias no metiladas CpG actúan como agonistas del TLR9, por lo que se han desarrollado secuencias modificadas mediante su sustitución por ribonucleótidos metilados, obteniéndose antagonistas para TLR9, para TLR7 o para ambos18. Uno de esos antagonistas duales, denominado IRS 954, ha sido probado en el modelo murino (NZB x NZW)F1, en el que ha demostrado un incremento de la supervivencia y una reducción tanto en los niveles de autoanticuerpos específicos, como en la proteinuria, la intensidad de la glomerulonefritis y el daño de otros órganos19.
- –
ST2825. La señal inicial producida por TLR7 y TLR9 es transducida exclusivamente a través de la proteína adaptadora MyD88, cuya ausencia atenúa el daño renal en modelos murinos20. Se ha desarrollado un compuesto peptidomimético denominado ST2825, que interfiere con MyD88, interrumpiendo así la ruta de señalización que utilizan estos receptores toll like. ST2825 ha demostrado in vitro bloquear la activación inducida por TLR9 en los LB memoria autorreactivos obtenidos a partir de pacientes con LES21. A pesar de ser tratamientos prometedores, aún no han sido ensayados en el LES humano.
La evidencia experimental y genética actual indica que el IFN-α es un mediador clave en la patogenia del LES. Al argumento de sus niveles aumentados en la sangre de los pacientes con LES y a sus conocidos efectos sobre los LT y LB, hay que añadir que estudios con microarrays de oligonucleótidos demuestran que el 70% de los adultos con LES, y hasta el 95% de los pacientes infantiles, presentan un patrón de sobreexpresión de genes relacionados con el IFN y con la granulopoyesis, introduciendo así la noción de que los neutrófilos pueden desempeñar algún papel patogénico en el LES. Este patrón de expresión genética se denomina la «firma» o la «rúbrica» del IFN en el lupus (IFN signature)22. Hay que añadir que se ha encontrado una firma del IFN en otras enfermedades autoinmunitarias. como la AR y la esclerosis múltiple (EM), y que no todos los pacientes con LES presentan esta rúbrica característica, por lo que probablemente se trate más de la «firma de la autoinmunidad» que de la «firma del lupus». Una sustancia denominada necrosis extracellular trap (NET), que se libera tras la muerte celular de los neutrófilos (por esa razón denominada NETosis), podría ser el nexo de unión entre el IFN y los neutrófilos en la patogenia del LES23. Tanto por sus efectos biológicos como por el argumento genético, el IFN-α se ha constituido en una de las dianas terapéuticas más perseguidas en la actualidad. Contamos con 2 anticuerpos monoclonales que bloquean el IFN-α, sifalimumab y rontalizumab, y con la inmunización frente a esta citocina mediante un quinoide, que ya han comenzado a ser ensayados en humanos.
- –
Sifalimumab (MEDI-545). Es un anticuerpo anti-IFN-α completamente humano, utilizado en un ensayo fase I en el que demostró una inhibición dosis-dependiente de la expresión de genes inducidos por IFN-α (la firma del IFN), así como una tendencia a la mejoría de la actividad de la enfermedad respecto del grupo placebo, menor requerimiento de tratamiento inmunosupresor y disminución significativa de los brotes24. En la actualidad un ensayo fase IIb se encuentra en periodo de reclutamiento.
- –
Rontalizumab. Anticuerpo humanizado anti-IFN-α, que se está estudiando actualmente en un ensayo fase II (ROSE) en 210 pacientes con LES de actividad moderada a grave (activo en julio 2011)25.
- –
IFN-α-quinoide. Una alternativa a la administración de anticuerpos monoclonales es la de generar una respuesta natural de anticuerpos neutralizantes anti-IFN-α, con una suerte de vacuna, denominada quinoide. Quinoides semejantes se encuentran en desarrollo frente al TNF-α y al VEGF. Los kinoides están formados por heterocomplejos que conjugan la citocina diana, en este caso el IFN-α, con una proteína portadora como la hemocianina de lapa, y que inducen una respuesta natural policlonal frente a los epítopos del IFNα. En un modelo murino la administración de este IFN-α-quinoide indujo la producción de anticuerpos neutralizantes, pero sin respuesta celular ni efectos colaterales aparentes, capaces de controlar las manifestaciones del lupus, incluyendo la lesión renal26. Los resultados de un fase I-II en pacientes con LES leve a moderado han sido presentados recientemente27 e indican que IFN-α-quinoide despierta una respuesta de anticuerpos anti-IFN-α suficiente para neutralizar la «firma del IFN» y para elevar los valores de C3.
Junto al importante papel de IFN-α, el IFN-γ interviene en la patogenia del LES por ser un potente mediador de inflamación e inducir la expresión del estimulador soluble del LB (BLyS)28. Se ha desarrollado un anticuerpo monoclonal completamente humano dirigido a IFN-γ (AMG 811, fontolizumab), sobre el cual se encuentran en etapa de reclutamiento sendos ensayos en fase I en NL29 y en lupus discoide30.
Depleción BOtro punto en el que se intenta interrumpir el círculo patogénico al que nos hemos referido (fig. 1) es a nivel de los propios LB, buscando su depleción31. Aunque el objetivo inicialmente perseguido por esta estrategia era disminuir la producción de anticuerpos, se ha visto que los LB, además de sintetizar anticuerpos, desarrollan otras funciones igualmente importantes: son eficientes células presentadoras de antígenos (APC), regulan la función de las células T autorreactivas, influyen sobre otras APC y producen diversas citocinas. En especial, los LB reguladores (Breg) constituyen una subpoblación identificada hace pocos años y definida como células que producen IL-10 y TGFβ, 2 citocinas con funciones supresoras de la inmunidad: inhiben la diferenciación de células T hacia el fenotipo inflamatorio Th2, así como la activación de macrófagos y las funciones proinflamatorias de las células dendríticas, entre otras32. Estas funciones reguladoras de los LB son inducidas por su activación a través del receptor de las células B (BCR, CD40) o de TLR9 y mediadas por IL-10. Por lo expuesto, se entiende que el efecto de la depleción B no se limita a disminuir la producción de anticuerpos, sino que además tiene otros muchos efectos, algunos de los cuales pueden ser beneficiosos para suprimir la autoinmunidad y, por tanto, podría se conveniente conservarlos. El concepto de células Breg hace que la estrategia terapéutica de la depleción B, tarde o temprano, tendrá que replantearse.
La depleción B se puede conseguir por 2 vías: mediante anticuerpos monoclonales frente a sus moléculas de superficie, como CD19, CD20 y CD22, o inhibiendo sus factores de supervivencia, como BLyS (B lymphocyte stimulator) o APRIL (A proliferation-inducing ligand).
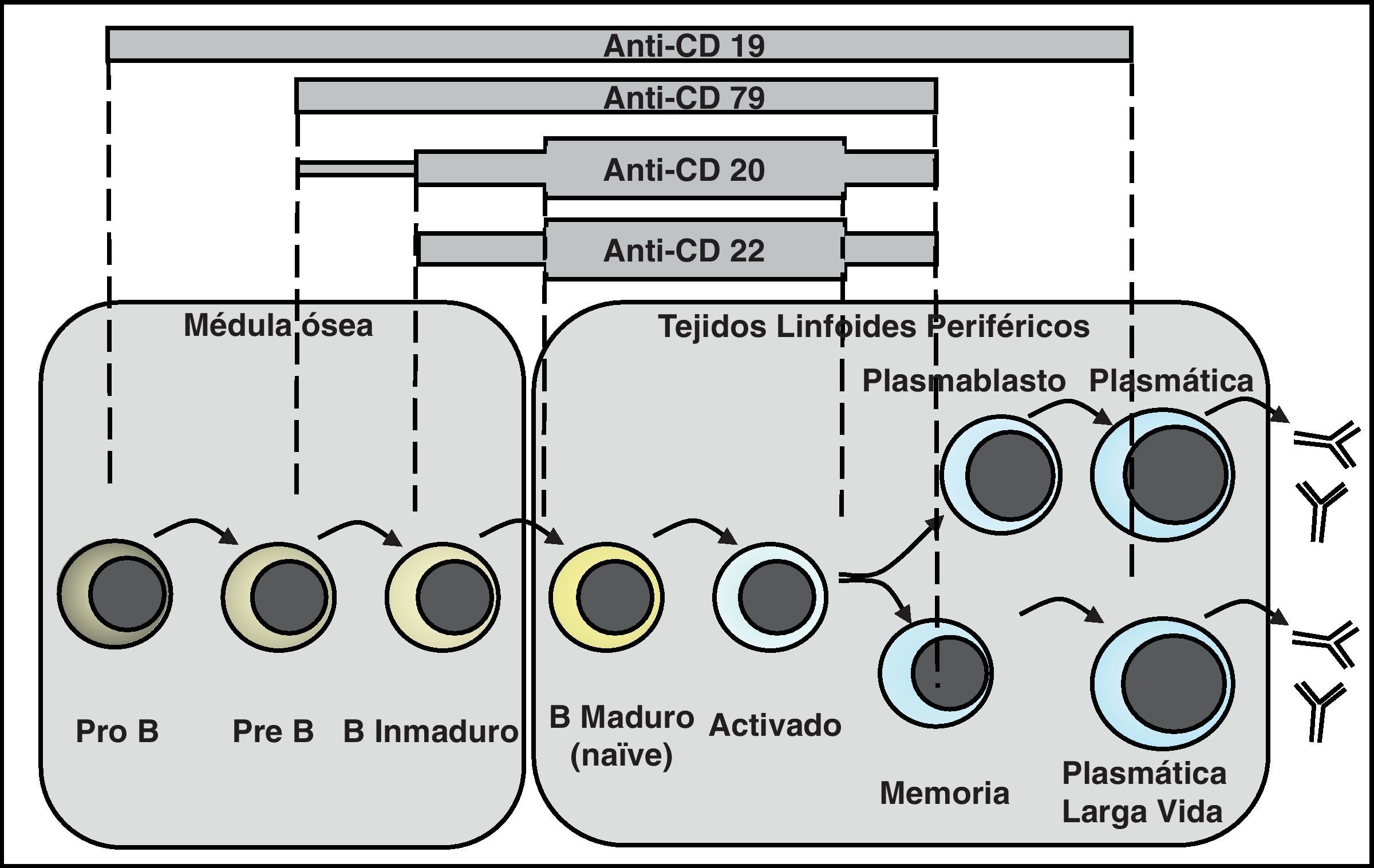
Anticuerpos anti-CD20CD20 es una proteína de membrana expresada por los linfocitos preB y B maduros, pero no por las células plasmáticas (fig. 2). En vista del papel central que tienen los LB en la patogenia del LES, se ha llevado a cabo una extensa investigación que ha conducido al desarrollo de al menos 6 anticuerpos monoclonales anti-CD20, cada uno con diferentes peculiaridades. Además del rituximab (RTX), contamos con el ocrelizumab (OCZ), que parece tener mayor afinidad por CD20 que sus competidores, ofatumumab, que induce más apoptosis y que ha sido probado en la EM; veltuzumab, que solo se ha probado en linfoma, y finalmente 2 fármacos producidos con la tecnología SMIP: SBI-087 y TRU-015. Todos los mencionados conducen a la depleción B por un triple mecanismo que incluye en mayor o menor medida apoptosis, citotoxicidad mediada por células y citotoxicidad mediada por anticuerpos.
- –
Rituximab. Se han llevado a cabo 2 grandes ensayos clínicos aleatorizados con RTX en LES. El estudio EXPLORER, en 169 pacientes con LES no renal y no neurológico, con actividad moderada a grave, tenía como objetivos valorar la respuesta completa o parcial sobre la base de la puntuación BILAG y la ausencia de brotes. No se logró demostrar diferencia respecto del grupo placebo; sin embargo, la respuesta en afroamericanos e hispanos fue mejor (33,8% vs. 15,7%; p=0,04) y hubo un importante descenso en los niveles de anti-ADN y mejoría de la hipocomplementemia33. El estudio LUNAR, realizado en 72 pacientes con NL tipo III y IV, tenía como objetivo valorar las respuestas renales completas y parciales a la semana 52 de tratamiento. A pesar de que numéricamente hubo más respondedores en el grupo RTX, no se encontró diferencia estadística respecto del grupo placebo. Al igual que en el EXPLORER, se encontraron mejores respuestas y mayor normalización de anti-ADN y complemento en afroamericanos e hispanos34. En ambos estudios se utilizó la pauta de 2 dosis de 1g separadas 15 días.
Espectro de las terapias de depleción B. Los anticuerpos anti-CD20, anti-CD22 y anti-CD79 tienen un espectro de actuación superponible, que incluye desde los linfocitos pre B o B inmaduros hasta los linfocitos B activados y memoria, sin afectar a las células plasmáticas. El espectro de anti-CD19 se extiende desde los linfocitos pro B hasta los plasmablastos y algunas células plasmáticas.
Los resultados desalentadores de estos 2 estudios contrastan con múltiples estudios abiertos que encontraron mejoría con el RTX en aproximadamente el 60% de los casos y respuesta renal hasta en el 66%35. Esta discordancia ha dado pie a una interminable controversia y a minuciosos análisis de las metodologías empleadas. Entre las explicaciones aducidas para justificar las discrepancias se han mencionado, entre otras, que en los ensayos se permitieron dosis de glucocorticoides e inmunosupresores que podrían haber enmascarado el efecto del anti-CD20, que los estudios han sido demasiado cortos, siendo así que RTX es más eficaz a medio/largo plazo, que se incluyeron pacientes no graves, mientras que el RTX es más eficaz en los casos más graves y que el BILAG es un índice muy exigente para valorar la respuesta al fármaco.
- –
Ocrelizumab. Anti-CD20 humanizado con el que teóricamente debería minimizarse el desarrollo de HACA que pueden presentarse con el quimérico RTX. Ha sido probado en el ensayo aleatorizado BELONG en pacientes con NL tipo III y IV, en el que 127 pacientes recibieron la dosis de 400mg y 128 la de 1.000mg. El objetivo fue valorar las respuestas renales completa y parcial en las semanas 48 y 96; sin embargo, el estudio tuvo que ser interrumpido debido a una inesperada incidencia de importantes efectos adversos, incluyendo infecciones graves. El análisis de los resultados obtenidos hasta el momento de su prematura interrupción, a las 32 semanas, demostró una superioridad numérica de respondedores en el grupo OCZ frente al grupo placebo, pero la diferencia no fue estadísticamente significativa; tampoco se encontraron diferencias entre ambas dosis36.
El estudio BEGIN, un fase III diseñado para evaluar la eficacia y seguridad de OCZ en pacientes con LES moderado a grave sin afectación renal, fue interrumpido a la vista de los resultados negativos alcanzados por el RTX en un estudio con un diseño superponible.
- –
SBI-087. Es un SMIP10 cuyo desarrollo en el LES se encuentra en la actualidad en fase I y cuyos resultados preliminares parecen indicar que es generalmente bien tolerado.
- –
TRU-015. Como el anterior, es un polipéptido de una sola cadena dirigido a CD20, con una vida media más larga que los anti-CD20 biotecnológicos convencionales, y diseñado para aumentar la potencia de los anticuerpos que actúan mediante citotoxicidad celular; sus resultados en un fase II sobre AR resultaron muy alentadores y confirmaron su capacidad para producir una depleción B. En el LES se investigó en un fase I.
CD22 es una glicoproteína transmembrana ligadora de azúcares, como ácido siálico, con un dominio Ig localizado en su N-terminal. Una vez activada, es internalizada y funciona como un receptor-inhibidor que regula la migración y actividad del LB2.
- –
Epratuzumab. EPZ es el único anti-CD22 que se ha utilizado en el LES. Los 2 primeros ensayos, ALLEVIATE A (LES moderado) y ALLEVIATE B (LES grave), evaluaron la eficacia de las dosis de 360mg/m2 y 720mg/m2 de EPZ contra placebo, pero tuvieron que ser suspendidos por falta de disponibilidad del fármaco. A pesar de ello, el análisis de los resultados en el momento de su precipitado final demostró una importante reducción en la actividad clínica y en el requerimiento de glucocorticoides, así como una mejoría en los indicadores de calidad de vida37. El tercer ensayo, denominado EMBLEM, fue realizado en 227 con LES moderado o grave, excluyendo NL III-IV y lupus neuropsiquiátrico grave; demostró una diferencia significativa en el porcentaje de pacientes respondedores en el grupo activo frente al placebo (43% vs. 21%; p = 0,02), sin que se encontraran diferencias en los eventos adversos38. Estos prometedores resultados han conducido a una serie de ensayos globales que, con el nombre corto de EMBODY, están en la actualidad en fase de reclutamiento.
Aunque no ensayadas en el lupus humano, existen otras moléculas de superficie de las células B, hipotéticas dianas:
- –
Anti-CD79. CD79 es una proteína transmembrana asociada al BCR, cuyo espectro de depleción es superponible al de anti-CD20 (pre-B a B maduros) (fig. 2), pero que actúa mediante una combinación de depleción e interrupción de la señalización a través del BCR.
- –
Anti-CD19 (MDX-1342). Quizás el más firme candidato a ser ensayado en el LES, tiene un espectro de depleción que va desde el linfocito pro-B hasta una fracción de las células plasmáticas31 (fig. 2). Ha sido probado hasta ahora solo en la AR y en enfermedades hematológicas.
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos. Los autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesAntonio C. Zea Mendoza es IP en estudios clínicos de Abbott Lab., MSD, Astra-Zeneca y UCB Pharma.
Alina L. Boteanu es investigador colaborador en un estudio clínico de Astra-Zeneca.
Los autores Walter A. Sifuentes Giraldo, María J. García Villanueva y Ana Lois Iglesias declaran no tener ningún conflicto de intereses.