La aparición de nueva información sobre las terapias biológicas en la espondiloartritis axial (EspAax) ha impulsado una nueva revisión de las recomendaciones de la Sociedad Española de Reumatología (SER) basadas en la mejor evidencia posible. Estas nuevas recomendaciones pueden servir de referencia para reumatólogos implicados en el tratamiento de estos pacientes.
MétodosSe creó un panel formado por nueve reumatólogos expertos en EspAax, previamente seleccionados por la SER mediante una convocatoria abierta. Las fases del trabajo fueron: identificación de las áreas clave para la actualización del consenso anterior, análisis y síntesis de la evidencia científica (sistema modificado de Oxford, CEBM, 2009) y formulación de recomendaciones a partir de esta evidencia y de técnicas de consenso.
ResultadosEsta revisión de las recomendaciones comporta una actualización en la evaluación de actividad de la enfermedad y objetivos de tratamiento. Incorpora también los nuevos fármacos disponibles, así como sus nuevas indicaciones, y una revisión de los factores predictivos de respuesta terapéutica y progresión del daño radiográfico. Finalmente, estas recomendaciones abordan también las situaciones de fracaso a un primer anti-TNF, así como la posible optimización de la terapia biológica. El documento incluye una tabla de recomendaciones y un algoritmo de tratamiento.
ConclusionesSe presenta la actualización de las recomendaciones SER para el uso de terapias biológicas en pacientes con EspAax.
Recent data published on biological therapy in axial spondyloarthritis (axSpA) since the last publication of the recommendations of the Spanish Society of Rheumatology (SER) has led to the generation of a review of these recommendations based on the best possible evidence. These recommendations should be a reference for rheumatologists and those involved in the treatment of patients with axSpA.
MethodsRecommendations were drawn up following a nominal group methodology and based on systematic reviews. The level of evidence and grade of recommendation were classified according to the model proposed by the Centre for Evidence Based Medicine at Oxford. The level of agreement was established through the Delphi technique.
ResultsIn this review, we did an update of the evaluation of disease activity and treatment objectives. We included the new drugs with approved therapeutic indication for axSpA. We reviewed both the predictive factors of the therapeutic response and progression of radiographic damage. Finally, we drafted some recommendations for the treatment of patients refractory to anti-tumor necrosis factor, as well as for the possible optimization of biological therapy. The document also includes a table of recommendations and a treatment algorithm.
ConclusionsWe present an update of the SER recommendations for the use of biological therapy in patients with axSpA.
El presente documento constituye la tercera actualización del consenso de la Sociedad Española de Reumatología (SER) sobre el uso de terapia biológica (TB) en pacientes con espondiloartritis axial (EspAax). Se incluyen recomendaciones que pretenden servir de referencia para ayudar y mejorar la toma de decisiones terapéuticas a los reumatólogos y a todos aquellos que, desde diversos niveles asistenciales o gestores, estén implicados en el tratamiento de esta enfermedad. Debido al elevado coste y a los márgenes de seguridad de la TB es necesaria una utilización racional y reflexiva de estos fármacos que debe estar basada en evidencias sólidas, en estudios bien diseñados, en resultados de los registros y en la experiencia acumulada en su utilización. El tratamiento con TB debe estar integrado dentro de una estrategia terapéutica amplia para la enfermedad, considerando todas las actuaciones posibles farmacológicas y no farmacológicas y teniendo en consideración la opinión del paciente.
La EspAax se caracteriza por la afectación de las articulaciones sacroilíacas y la columna vertebral. Tradicionalmente el diagnóstico se basaba en los criterios modificados de New York de 1984 para la espondilitis anquilosante (EA) que requerían de la presencia de daño estructural crónico, no reversible a nivel de las articulaciones sacroilíacas, detectable en la radiografía simple, lo cual suponía un retraso diagnóstico importante. La reciente publicación en 2009 de los criterios del grupo ASAS (Assessment in Ankylosing Spondylitis International Society) ha permitido mejorar la clasificación de los pacientes con espondiloartritis (EspA) en general y permite incluir a pacientes en estadios más precoces. Estos criterios publicados definen, por un lado, el grupo de EspAax para aquellos pacientes con síntomas predominantemente axiales pero que pueden tener también síntomas periféricos, y por otro, las EspA periféricas1.
La EspAax incluye tanto pacientes con criterios de EspAax que presentan además sacroilitis radiográfica (EA definida según criterios de Nueva York modificados), como individuos con EspAax no radiográfica (EspAax-nr). Aunque sigue existiendo un intenso debate en si considerar que se trata de dos entidades diferentes o una sola entidad con diferentes fenotipos clínicos, en este documento, y siguiendo las recientes recomendaciones EULAR, se considerará una sola entidad2.
Las EspA en conjunto tienen un impacto sociosanitario importante. De manera general, las cifras de prevalencia de las EspA se sitúan entre el 0,1 y el 2,5% de la población y se estima una incidencia que va desde los 0,84 casos a los 77 casos por cada 100.000 habitantes/año3. La incidencia anual estimada en España, según el estudio ESPIDEP, es de 62,5 casos por 100.000 habitantes4 y constituyen el 13% de los pacientes en los servicios de reumatología españoles. Un número considerable de pacientes con EspAax desarrollan una enfermedad discapacitante, con deterioro de su capacidad funcional y calidad de vida, incluso desde el inicio de la enfermedad, dando lugar a la pérdida de la capacidad productiva5.
Aunque la base del tratamiento de las EspAax sigue siendo la educación, la terapia física y los antiinflamatorios no esteroideos (AINE), las evidencias de la eficacia de los antagonistas del TNFα en todos los aspectos de la enfermedad se han incrementado notablemente6. No existen datos que apoyen el uso preferencial de un AINE sobre los demás, aunque en la práctica clínica tienden a usarse los de vida media larga. Los inhibidores específicos de la ciclooxigenasa 2 (COXIB) son un grupo de antiinflamatorios muy eficaces y, por tanto, a tener en cuenta en el tratamiento de estos pacientes7-9. Los estudios publicados no apoyan el uso de ninguno de los fármacos modificadores de enfermedad (FAME) clásicos en las manifestaciones axiales. La sulfasalazina ha demostrado, en estudios controlados, que es efectiva, aunque de forma modesta, sobre las manifestaciones articulares periféricas10. No existen estudios controlados que apoyen la eficacia de otros FAME, como el metotrexato o la leflunomida, sobre las manifestaciones articulares periféricas, aunque su uso no es descartable en la práctica clínica en las formas periféricas3.
Material y métodosEn este proyecto se ha utilizado una síntesis cualitativa de la evidencia científica y técnicas de consenso («juicio razonado» y «Delphi modificado») que recogen el acuerdo de expertos en base a su experiencia clínica y la evidencia científica.
Fases del procesoEn el desarrollo del documento de Recomendaciones se han seguido una serie de pasos que se describen a continuación:
- 1.
Creación del grupo de trabajo. La elaboración del documento se inició con la constitución de un panel de expertos elegidos mediante una convocatoria abierta a todos los socios de la SER. La Comisión de Guías de Práctica Clínica y Recomendaciones SER valoró el currículum vitae de los solicitantes según criterios objetivos de aportación al conocimiento de la EspAax, principalmente por la participación en publicaciones en revistas de impacto en los últimos 5años. El panel de expertos quedó constituido por 9 reumatólogos miembros de la SER. La coordinación de los aspectos clínicos y metodológicos se realizó por uno de estos reumatólogos, como investigador principal, y una especialista en metodología, técnico de la Unidad de Investigación de la SER.
- 2.
Identificación de las áreas claves para la actualización del consenso anterior. Todos los miembros del grupo de trabajo participaron para estructurar el documento y establecer los contenidos y aspectos claves. Se optó por la actualización de las recomendaciones provenientes tanto del Consenso anterior como de la última versión de la ESPOGUIA 20153. Primero se identificaron las preguntas clínicas que podrían tener más impacto en la utilización de TB en la EspAax. Después se fijaron los contenidos y resultados que no precisaban responder a la formulación de pregunta de investigación. Se definió también la metodología a seguir en el proceso de elaboración de las recomendaciones.
- 3.
Búsqueda bibliográfica. Las preguntas clínicas se reformularon en cuatro preguntas con formato PICO. Para responder a las preguntas se diseñó una estrategia de búsqueda y se realizó una revisión de la evidencia científica de estudios publicados hasta febrero de 2016. Se utilizaron las bases de datos: PubMed (Medline), EMBASE, y Cochrane Library (Wiley Online). Se completó el proceso con una búsqueda manual de referencias y pósteres y resúmenes de congresos que los revisores y expertos consideraron de interés. Las estrategias de búsquedas bibliográficas de las siete revisiones sistemáticas (RS) pueden consultarse en el material suplementario (en un anexo metodológico en la página web de la SER).
- 4.
Análisis y síntesis de la evidencia científica. Seis reumatólogos, del grupo de trabajo de revisores de la evidencia de la SER, se encargaron de revisar sistemáticamente la evidencia científica disponible. Tras la lectura crítica del texto completo de los estudios seleccionados para cada revisión, elaboraron un resumen mediante el uso de un formulario homogeneizado incluyendo tablas y texto para describir la metodología, los resultados y la calidad de cada estudio. Se detallaron los motivos de exclusión de los artículos no incluidos en la selección. Se evaluó el nivel global de la evidencia científica utilizando la modificación de los niveles de evidencia del Centro Oxford de Medicina basada en la evidencia CEBM (http://www.cebm.net/oxford-centre-evidence-based-medicine-levels-evidence-march-2009).
- 5.
Formulación de recomendaciones. Finalizada la lectura crítica el investigador principal y los componentes del grupo de expertos procedieron a la formulación de recomendaciones específicas basadas en la evidencia científica. Esta formulación se ha basado en la «evaluación formal» o «juicio razonado», resumiendo previamente la evidencia para cada una de las preguntas clínicas. Se tuvo en cuenta también la calidad, la cantidad y la consistencia de la evidencia científica, la generalidad de los resultados, su aplicabilidad y su impacto clínico. Para la formulación de las recomendaciones generales se utilizaron dos rondas de consenso: primero, en una reunión presencial, con el sistema de consenso de «juicio razonado», todos los expertos redactaron y discutieron las recomendaciones en presencia del metodólogo; después, mediante un cuestionario Delphi, se consensuó el grado de acuerdo de los expertos con la redacción de cada una de las recomendaciones usando una escala Likert del 1 al 5 (1: absolutamente en desacuerdo, 2: moderadamente en desacuerdo, 3: ni acuerdo ni desacuerdo, 4: moderadamente de acuerdo, 5: absolutamente de acuerdo). Se definió alto grado de consenso en la redacción cuando el porcentaje de panelistas que otorgaron valores ≥4 en la escala de Likert fue superior al 75%. El nivel de evidencia y la graduación de la fuerza de las recomendaciones se establecieron en base al sistema modificado de Oxford 2009. De algunas recomendaciones se derivan comentarios (a los que se ha añadido nivel de evidencia y grado de acuerdo) que el grupo elaborador ha considerado pertinente incluir como aclaraciones o consecuencias de lo expuesto en la propia recomendación.
- 6.
Exposición pública. El borrador de este documento de Recomendaciones SER fue sometido a un proceso de exposición pública por parte de socios miembros de la SER y de distintos grupos de interés (industria farmacéutica, otras sociedades científicas y asociaciones de pacientes), con objeto de recoger la valoración y su argumentación científica de la metodología o las recomendaciones.
El documento recoge todas las recomendaciones formuladas subdivididas en dos apartados: principios generales y recomendaciones específicas. A partir de las recomendaciones se ha elaborado un algoritmo terapéutico que presenta de forma resumida la aproximación al tratamiento de la EspAax.
Consideraciones previasTerapia biológica disponibleFármacos inhibidores del TNF alfa (anti-TNF)Actualmente disponemos de tres anticuerpos monoclonales (infliximab, adalimumab y golimumab), una proteína de fusión con el receptor p75 soluble (etanercept) y un fragmento Fab’ pegilado de un anticuerpo monoclonal humanizado recombinante (certolizumab pegol). La Agencia Europea del Medicamento (EMA) los ha aprobado tanto para la EA como para la EspAax-nr, a excepción del infliximab, que solo tiene indicación para la EA11. Estos fármacos han demostrado mejorar no solo la sintomatología clínica de la enfermedad, sino también la movilidad axial, la función física, la calidad de vida y los parámetros de inflamación biológicos, así como velocidad de sedimentación globular y proteína C reactiva (PCR) los signos de inflamación vertebral y sacroilíaca (objetivados por RM)12,13. La tasa de respuesta en pacientes con EA es similar entre ellos (ASAS20 58-61% vs 10-20% del placebo), por lo que la elección concreta dependerá del criterio médico y las circunstancias particulares de cada paciente12,13. Para más información, consultar consenso previo14 y ver la tabla en el material suplementario.
Certolizumab (CZP)Es el último anti-TNF aprobado y que no estaba incluido en el consenso anterior. La dosis recomendada es de 200mg cada 2 semanas, o de 400mg cada 4 semanas por vía subcutánea. El CZP ha demostrado ser igual de eficaz en pacientes con EA y en pacientes con EspAax-nr para reducir los signos y síntomas de la enfermedad15,16. El perfil de seguridad fue consistente con los datos de seguridad presentados para otros anti-TNF. Debido a la ausencia de la región Fc, el CZP no se une a los RnFc humanos y, en consecuencia, a diferencia de los otros anticuerpos monoclonales, no sufre de transferencia mediada por dichos receptores a través de la placenta, y tampoco se han detectado niveles de CZP significativos en la leche materna17.
Fármacos biosimilaresUn fármaco biosimilar es un fármaco biológico que contiene una versión de la sustancia activa de un producto biológico original ya autorizado (fármaco de referencia). El desarrollo de los biosimilares no está dirigido a demostrar un beneficio clínico en sí, sino a demostrar una eficacia y seguridad similares a las del fármaco de referencia18,19. Los biosimilares, al no tratarse de copias exactas del agente biológico de referencia, en ocasiones requieren ensayos clínicos específicos para cada una de las indicaciones del fármaco de referencia. A falta de estudios demostrativos publicados, la intercambiabilidad y sustitución terapéutica de un biológico original por un biosimilar no debería hacerse de forma automática y bajo criterios puramente económicos, pues debe primar siempre el beneficio de paciente18. El uso de biosimilares requiere programas estrictos de seguimiento de farmacovigilancia. Los medicamentos biosimilares actualmente autorizados por la EMA son biosimilares de infliximab y etanercept.
Los biosimilares de infliximab aprobados (en la actualidad disponemos ya de tres)20-22 son medicamentos biosimilares de Remicade® (infliximab) y tienen para las EspAax las mismas indicaciones, dosis e intervalos de administración que el fármaco de referencia. Al igual que el infliximab, carecen de indicación para la EspAax-nr. La EMA, en base a los datos aportados por la industria, aprobó los biosimilares de infliximab para todas las indicaciones de Remicade®, teniendo en cuenta los datos de ensayos realizados en pacientes con artritis reumatoide (AR) y EA23,24, aunque para su aprobación en el tratamiento de la enfermedad de Crohn y de la colitis ulcerosa pidió estudios adicionales.
El biosimilar de etanercept (a día de hoy disponemos solo de uno) ha sido aprobado por la EMA para las mismas indicaciones y circunstancias que el fármaco de referencia (tratamiento de la EA y EspAax-nr). El estudio de registro (SB4-G31-AR) se realizó en pacientes con AR y se extrapoló la indicación del biosimilar a todas las indicaciones y circunstancias propias del fármaco de referencia, incluyendo EA y EspAax-nr25.
Fármacos anti IL-17SecukinumabEs un anticuerpo monoclonal recombinante totalmente humano dirigido contra la IL-17A26. Secukinumab está indicado para el tratamiento de la EA activa en adultos que no han respondido adecuadamente al tratamiento convencional. En los estudios de registro del fármaco para conseguir su indicación terapéutica, secukinumab presentó una respuesta ASAS20 (objetivo primario a las 16semanas) de un 59% en comparación al 28% del grupo placebo; dichos resultados se mantuvieron hasta la semana 52, incluso en pacientes con respuesta previa inadecuada a los anti-TNF. De igual modo, se obtuvo mejoría en ASAS40, BASDAI, PCR y calidad de vida27. En una extensión a 2años se constató la persistencia de la respuesta clínica observada, así como que el 80% de los pacientes tratados con secukinumab no presentaron progresión radiográfica28. Secukinumab puede aumentar el riesgo de infecciones: la mayoría fueron infecciones leves o moderadas de las vías respiratorias altas que no precisaron la interrupción del tratamiento. Se debe tener precaución cuando se valore la administración de secukinumab en pacientes con infecciones crónicas o con antecedentes de infecciones recurrentes. Respecto a la tuberculosis, se deben mantener las mismas recomendaciones que para anti-TNF, aunque no se han notificado en los ensayos clínicos casos de tuberculosis. Se ha observado un aumento de la incidencia de infecciones mucocutáneas por cándida con una tasa ajustada de 0,9 por cada 100 pacientes-año, que se resolvieron con un tratamiento antifúngico estándar sin necesidad de interrumpir secukinumab. Se ha observado neutropenia (0,3%) y reacciones de hipersensibilidad (0,6%) de forma infrecuente y leve en la mayoría de los casos. El perfil de inmunogenicidad de secukinumab parece ser muy bajo (0,7% desarrollo de anticuerpos a las 52 semanas, cerca de la mitad de los casos son anticuerpos neutralizantes). No existen evidencias suficientes de la eficacia de anti-IL-17 en el tratamiento de la uveítis asociada a EspA. En cuanto al tratamiento de la enfermedad de Crohn activa moderada/grave, secukinumab no demostró ser eficaz y presentó una tasa de acontecimientos adversos superior al placebo29. Secukinumab no está contraindicado en insuficiencia cardíaca congestiva (ICC) ni en enfermedades desmilinizantes. Finalmente, los datos disponibles en la actualidad no sugieren que secukinumab incremente el riesgo de eventos cardiovasculares o de neoplasias. No existen datos suficientes del uso de secukinumab durante la gestación, ni en infecciones por virus hepatotropos (VHB y VHC), ni su uso concomitante con vacunas vivas, por lo que, en estas situaciones, deberán adoptarse las mismas medidas que para la terapia anti-TNF.
Posibles dianas futurasExisten numerosas moléculas actualmente en estudio para obtener la indicación para el tratamiento de los pacientes con EspAax que sin duda han de aumentar nuestro arsenal terapéutico. En la línea de IL-23 e IL-17, el ustekinumab (anticuerpo monoclonal dirigido contra la subunidad p40 común a IL-23 e IL-12) es la única molécula con datos preliminares publicados30. En cuanto a las llamadas «pequeñas moléculas» o FAME con diana terapéutica específica, el apremilast (inhibidor oral selectivo de la fosfodiesterasa 4) y el tofacitinib (inhibidor oral de las Janus kinasas) tienen ya datos preliminares publicados en pacientes con EA31,32.
ResultadosEl total de recomendaciones formuladas sobre el uso de terapias biológicas en EspAax es de 14 (tablas 1 y 2).
Recomendaciones SER sobre el uso de terapias biológicas en espondiloartritis axial. Recomendaciones generales
| Recomendaciones generales | GR | NE | GA ≥ 4 |
|---|---|---|---|
| Recomendación 1: Se recomienda iniciar el tratamiento farmacológico, en pacientes con EspAax tan pronto se haya realizado el diagnóstico | D | 2b, 4 | 100% |
| Recomendación 2: Se recomienda como objetivo terapéutico la remisión de la enfermedad o, en su defecto, una baja actividad de la misma | D | 5 | 100% |
| Recomendación 3: Se recomienda la monitorización frecuente (cada 1-3 meses) de la actividad de la enfermedad hasta alcanzar el objetivo terapéutico. Se recomienda realizar dicha monitorización mediante el índice ASDAS o, como alternativa, mediante el BASDAI | D | 5 | 100% |
| Recomendación 4: Se recomienda a la hora de establecer un régimen terapéutico tener en cuenta la eficacia, la opinión del paciente, la seguridad y las comorbilidades | D | 5 | 100% |
ASDAS: ASAS-endorsed disease activity score; BASDAI: Bath Ankylosing Spondylitis Disease Activity Index; EspAax: espondiloartritis axial; GA: grado de acuerdo; GR: grado de recomendación; NE: nivel de evidencia.
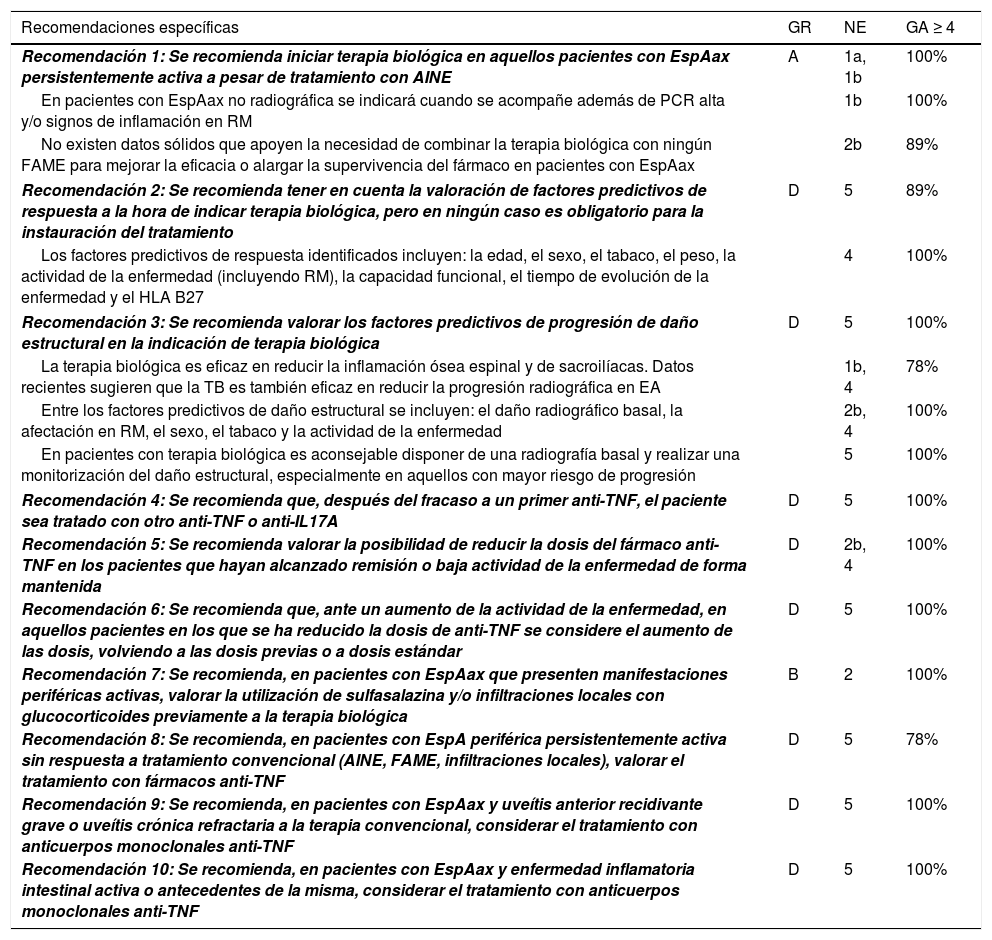
Recomendaciones SER sobre el uso de terapias biológicas en espondiloartritis axial. Recomendaciones específicasa
| Recomendaciones específicas | GR | NE | GA ≥ 4 |
|---|---|---|---|
| Recomendación 1: Se recomienda iniciar terapia biológica en aquellos pacientes con EspAax persistentemente activa a pesar de tratamiento con AINE | A | 1a, 1b | 100% |
| En pacientes con EspAax no radiográfica se indicará cuando se acompañe además de PCR alta y/o signos de inflamación en RM | 1b | 100% | |
| No existen datos sólidos que apoyen la necesidad de combinar la terapia biológica con ningún FAME para mejorar la eficacia o alargar la supervivencia del fármaco en pacientes con EspAax | 2b | 89% | |
| Recomendación 2: Se recomienda tener en cuenta la valoración de factores predictivos de respuesta a la hora de indicar terapia biológica, pero en ningún caso es obligatorio para la instauración del tratamiento | D | 5 | 89% |
| Los factores predictivos de respuesta identificados incluyen: la edad, el sexo, el tabaco, el peso, la actividad de la enfermedad (incluyendo RM), la capacidad funcional, el tiempo de evolución de la enfermedad y el HLA B27 | 4 | 100% | |
| Recomendación 3: Se recomienda valorar los factores predictivos de progresión de daño estructural en la indicación de terapia biológica | D | 5 | 100% |
| La terapia biológica es eficaz en reducir la inflamación ósea espinal y de sacroilíacas. Datos recientes sugieren que la TB es también eficaz en reducir la progresión radiográfica en EA | 1b, 4 | 78% | |
| Entre los factores predictivos de daño estructural se incluyen: el daño radiográfico basal, la afectación en RM, el sexo, el tabaco y la actividad de la enfermedad | 2b, 4 | 100% | |
| En pacientes con terapia biológica es aconsejable disponer de una radiografía basal y realizar una monitorización del daño estructural, especialmente en aquellos con mayor riesgo de progresión | 5 | 100% | |
| Recomendación 4: Se recomienda que, después del fracaso a un primer anti-TNF, el paciente sea tratado con otro anti-TNF o anti-IL17A | D | 5 | 100% |
| Recomendación 5: Se recomienda valorar la posibilidad de reducir la dosis del fármaco anti-TNF en los pacientes que hayan alcanzado remisión o baja actividad de la enfermedad de forma mantenida | D | 2b, 4 | 100% |
| Recomendación 6: Se recomienda que, ante un aumento de la actividad de la enfermedad, en aquellos pacientes en los que se ha reducido la dosis de anti-TNF se considere el aumento de las dosis, volviendo a las dosis previas o a dosis estándar | D | 5 | 100% |
| Recomendación 7: Se recomienda, en pacientes con EspAax que presenten manifestaciones periféricas activas, valorar la utilización de sulfasalazina y/o infiltraciones locales con glucocorticoides previamente a la terapia biológica | B | 2 | 100% |
| Recomendación 8: Se recomienda, en pacientes con EspA periférica persistentemente activa sin respuesta a tratamiento convencional (AINE, FAME, infiltraciones locales), valorar el tratamiento con fármacos anti-TNF | D | 5 | 78% |
| Recomendación 9: Se recomienda, en pacientes con EspAax y uveítis anterior recidivante grave o uveítis crónica refractaria a la terapia convencional, considerar el tratamiento con anticuerpos monoclonales anti-TNF | D | 5 | 100% |
| Recomendación 10: Se recomienda, en pacientes con EspAax y enfermedad inflamatoria intestinal activa o antecedentes de la misma, considerar el tratamiento con anticuerpos monoclonales anti-TNF | D | 5 | 100% |
AINE: antiinflamatorios no esteroideos; anti-IL17: inhibidora de la interleucina 17; anti-TNF: inhibidor del factor de necrosis tumoral; EA: espondilitis anquilosante; EspAax: espondiloartritis axial; FAME: fármacos antirreumáticos modificadores de la enfermedad; GA: grado de acuerdo; GR: grado de recomendación; HLA B27: antígeno leucocitario humano B27; NE: nivel de evidencia; PCR: proteína C reactiva; RNM: resonancia magnética; TB: terapia biológica.
Recomendación general 1
Se recomienda iniciar el tratamiento farmacológico, en pacientes con EspAax tan pronto se haya realizado el diagnóstico (GR: D; NE: 2b, 4; GA: 100%).
El diagnóstico precoz parece clave, pues son numerosos los estudios que apoyan que el retraso diagnóstico comporta peores desenlaces (BASDAI, BASFI, movilidad axial, progresión radiológica)33-35.
Los AINE y la TB son los únicos fármacos que han mostrado ser eficaces en el tratamiento de las manifestaciones axiales. Diversos ensayos en pacientes con EspAax precoz a los que se les ha administrado AINE y terapia anti-TNF han reportado resultados alentadores, con una mayor tasa de respuesta al tratamiento que en estudios efectuados con pacientes más evolucionados y con EA definida36. En este sentido, diversos estudios sugieren que el tiempo de evolución es un factor importante en predecir la respuesta al tratamiento37,38, así como en predecir el rebrote clínico de la enfermedad tras la suspensión de la terapia anti-TNF39. Los datos sobre reducción de la progresión radiográfica son controvertidos tanto para AINE como para la TB; sin embargo, existen algunas evidencias que sugieren que cuando el tratamiento consigue mantener un control estricto de la enfermedad (baja actividad) puede reducir la progresión radiográfica en estos pacientes40.
Recomendación general 2
Se recomienda como objetivo terapéutico la remisión de la enfermedad o, en su defecto, una baja actividad de la misma (GR: D; NE: 5; GA: 100%).
Recomendación general 3
Se recomienda la monitorización frecuente (cada 1-3 meses) de la actividad de la enfermedad hasta alcanzar el objetivo terapéutico. Se recomienda realizar dicha monitorización mediante el índice ASDAS o, como alternativa, mediante el BASDAI (GR: D; NE: 5; GA: 100%).
El objetivo del tratamiento de la EspAax es alcanzar la remisión de la enfermedad o, en su defecto, reducir al mínimo la actividad inflamatoria para alcanzar una mejoría significativa de los síntomas y signos (inflamación articular, dolor, rigidez axial y periférica, etc.), preservar la capacidad funcional, mantener una buena calidad de vida y controlar el daño estructural.
Evaluación de la actividad de la enfermedadDebido a la presentación heterogénea de la EspAax y la posibilidad de la coexistencia de diferentes manifestaciones clínicas, el uso de variables aisladas para medir la actividad de la enfermedad puede dar una falsa imagen y, por tanto, junto a la valoración del médico, se recomienda emplear índices compuestos que reflejen de una manera global la actividad de la enfermedad41.
Tradicionalmente, el índice empleado para monitorizar la actividad de la enfermedad y para indicar una TB ha sido el Bath Ankylosing Spondylitis Disease Activity Index (BASDAI)42. En base a este, la remisión de la enfermedad suele definirse como BASDAI≤2 y PCR sérica en rango normal. Sin embargo, este es un objetivo difícil de conseguir, y en ocasiones se puede considerar aceptable alcanzar un BASDAI<4 (que es el punto de corte habitualmente empleado para definir baja actividad de la enfermedad) junto a una PCR sérica en rango normal. No obstante, el BASDAI tiene una limitación principal, que es el hecho de ser un índice completamente subjetivo. Por ello mismo, en 2009 se desarrolló el Ankylosing Spondylitis Disease Activity Score (ASDAS), un índice que incluye tanto variables subjetivas como una variable objetiva de inflamación43. Desde su publicación, el ASDAS ha sido validado en diferentes poblaciones, incluyendo una cohorte de EspA de reciente comienzo en España44. La capacidad discriminativa y la sensibilidad al cambio del ASDAS también han sido demostradas en numerosos estudios, siendo estas superiores a las del BASDAI o cualquier otra medida aislada45. Además, el ASDAS ha demostrado ser la medida clínica que más se relaciona con el grado de inflamación detectado en RM de articulaciones sacroilíacas y de columna y con el grado de progresión radiográfica en estudios longitudinales40,46. Por todo ello, actualmente los panelistas de este documento recomiendan el ASDAS-PCR como índice principal para monitorizar la actividad de la enfermedad. En base a este índice, el objetivo terapéutico es alcanzar un ASDAS-PCR <1,3. No obstante, el panel considera que puede considerarse aceptable un ASDAS-PCR <2,147.
En cualquier caso, a la hora de definir si un paciente con EspAax ha alcanzado remisión o baja actividad de la enfermedad, además de uno de los índices compuestos (preferiblemente el ASDAS) se ha de tener también en cuenta la valoración global del médico, expresada preferiblemente en una escala análogo visual de 0-10cm y basada en la anamnesis, la exploración física, las pruebas complementarias y la ausencia de manifestaciones extraarticulares de la enfermedad.
El papel de la RM para monitorizar la actividad de la enfermedad en pacientes con EspAax aún está por definir. Hasta la fecha se desconoce cuál es su valor añadido respecto a los índices clínicos compuestos y, por tanto, su uso no está indicado de forma rutinaria para monitorizar la actividad de la enfermedad. No obstante, en algunos casos la RM de las articulaciones sacroilíacas y/o de columna puede emplearse para evaluar y monitorizar la actividad de la enfermedad en EspAax, aportando información adicional a las evaluaciones clínicas y bioquímicas. La decisión de cuándo repetir la RM en estos casos depende de las circunstancias clínicas48.
Evaluación de la función física y la calidad de vidaEl panel recomienda utilizar el cuestionario Bath Ankylosing Spondylitis Function Index (BASFI) como medida de capacidad funcional en pacientes con EspAax49. En situaciones especiales con predominio de la artritis periférica puede ser más adecuada la utilización del cuestionario de discapacidad Health Assessment Questionnaire (HAQ).
Para evaluar la calidad de vida en pacientes con EspAax, tradicionalmente se ha empleado el cuestionario Ankylosing Spondylitis Quality of Life (ASQoL). Actualmente, el grupo ASAS está desarrollando un nuevo índice de salud, el ASAS Health Indez (ASAS-HI), que consta de 17 preguntas y también ha sido traducido al español; no obstante, los puntos de corte para definir los diferentes estados de salud aún están por establecer50.
Definición de enfermedad activaA la hora de indicar una TB en pacientes con EspAax, se entiende como enfermedad activa aquella definida como BASDAI ≥4 o como alternativa un ASDAS-PCR ≥2,1 junto a una valoración global del médico de que la enfermedad está activa (≥4 en EVA de 0-10cm) en base a la experiencia de este, la anamnesis, la exploración física y las pruebas complementarias.
Definición de respuesta terapéuticaSe considera que un paciente con EspAax responde a TB si tras 3meses de tratamiento se consigue: a)una disminución del BASDAI del 50% o una disminución absoluta de más de 2puntos respecto a los valores previos37, o b)disminución del ASDAS ≥1,1 (mejoría clínicamente importante)41. En pacientes refractarios a TB y en ausencia de alternativa terapéutica se considerará una respuesta mínimamente aceptable para mantener el fármaco una mejora del 20% respecto a la situación basal previa a iniciar el tratamiento biológico. En cualquier caso y en todas las situaciones, la opinión del médico basada en su experiencia y los datos clínicos de paciente es clave para decidir continuar o no con el tratamiento.
Recomendación general 4
Se recomienda a la hora de establecer un régimen terapéutico tener en cuenta la eficacia, la opinión del paciente, la seguridad y las comorbilidades (GR: D; NE: 5; GA: 100%).
No existen datos comparativos directos que demuestren diferencias en términos de eficacia y seguridad entre los diferentes anti-TNF ni entre los anti-TNF y el secukinumab13,27. En este sentido, la elección de uno u otro fármaco se valorará en consonancia con las recomendaciones de la mayoría de guías3,14, en función de otros factores asociados a las características y las particularidades de administración de cada fármaco tales como la disponibilidad de hospital de día y la facilidad de canalización vía intravenosa, la actividad laboral del paciente (que puede repercutir en la posibilidad de recibir tratamiento en régimen hospitalario) y las preferencias personales del paciente. Finalmente, es importante a la hora de prescribir un fármaco tener en cuenta la presencia de manifestaciones extraarticulares y comorbilidades.
El AINE se considera la piedra angular y el tratamiento de inicio en pacientes con EspAax; sin embargo, su uso continuado se ha asociado a mayor dificultad en el control de la presión arterial y de la insuficiencia cardíaca, deterioro de la función renal y el incremento de mortalidad a largo plazo51,52. Por este motivo, se considera importante evaluar el perfil de riesgo cardiovascular y valorar alternativas terapéuticas a la hora de prescribir y mantener de forma crónica un AINE en estos pacientes, especialmente cuando existe evidencia que el tratamiento anti-TNF parece reducir la disfunción endotelial y podría estabilizar la aterosclerosis subclínica en pacientes con EA53,54.
Recomendaciones específicas1. Se recomienda iniciar TB en aquellos pacientes con EspAax persistentemente activa a pesar de tratamiento con AINE (GR: A; NE: 1a, 1b; GA: 100%).
Comentarios derivados de esta recomendación:
En pacientes con EspAax no radiográfica se indicará cuando se acompañe además de PCR alta y/o signos de inflamación en RM (NE: 1b; GA: 100%).
No existen datos sólidos que apoyen la necesidad de combinar la TB con ningún FAME para mejorar la eficacia o alargar la supervivencia del fármaco en pacientes con EspAax (NE: 2b; GA: 89%).
Diversos estudios indican que las manifestaciones clínicas y la carga de la enfermedad son comparables en pacientes con EspAax-nr y en EA definida55,56. Por tanto, ambos fenotipos clínicos requieren tratamiento, independientemente de la presencia de daño estructural.
Los inhibidores del TNF y el secukinumab han demostrado ser eficaces en el tratamiento de la EA refractaria a AINE con reducción significativa de sintomatología clínica, actividad inflamatoria medida por PCR y/o RM, capacidad funcional y calidad de vida26,57-59, e incluso hay datos a favor de un posible efecto enlentecedor de la progresión radiográfica espinal asociado a la TB33,60,61.
Los inhibidores del TNF (adalimumab, certolizumab pegol, etanercept y golimumab) han demostrado ser eficaces en el tratamiento de la EspAax-nr refractaria a AINE, con reducción significativa de sintomatología clínica y mejoría de la capacidad funcional y de la calidad de vida, de una forma similar a la observada en los pacientes con EA16,62-64. En estos estudios se ha evidenciado, además, una mejor respuesta clínica en aquellos pacientes en que la sintomatología clínica se asociaba a la presencia de una PCR alta y/o inflamación en la RM de sacroilíacas. No todos los pacientes con EspAax-nr progresan a EA definida: diversos estudios han evidenciado que la presencia de PCR alta e inflamación sacroilíaca medida por RM son factores predictores de progresión de la enfermedad y de respuesta a la terapia anti-TNF63,65,66. En este sentido, es razonable que en pacientes con EspAax-nr se requiera que la actividad clínica de la enfermedad se acompañe de la presencia de una PCR alta y/o sacroilitis por RM antes de establecer la indicación de TB.
No existen datos a día de hoy de eficacia de infliximab ni de secukinumab en pacientes con EspAax-nr, por lo que estos fármacos no están aprobados en esta indicación. No existen datos, en pacientes con EspAax, que apoyen la necesidad de combinar la TB (anti-TNF y/o secukinumab) con ningún FAME para mejorar la eficacia12,13,26. Aunque los datos sobre supervivencia son más controvertidos, el grupo de panelistas de estas recomendaciones considera que, a día de hoy, son insuficientes para apoyar la combinación sistemática de la TB con un FAME67-70.
2. Se recomienda tener en cuenta la valoración de factores predictivos de respuesta a la hora de indicar TB, pero en ningún caso es obligatorio para la instauración del tratamiento (GR: D; NE: 5; GA: 89%).Comentario derivado de esta recomendación:
Los factores predictivos de respuesta identificados incluyen: la edad, el sexo, el tabaco, el peso, la actividad de la enfermedad (incluyendo RM), la capacidad funcional, el tiempo de evolución de la enfermedad y el HLA B27 (NE: 4; GA: 100%).
Numerosos estudios han asociado ciertas variables de la enfermedad con una mejor respuesta al tratamiento con fármacos anti-TNF. La menor edad al inicio del tratamiento y el menor tiempo de evolución se han asociado con mejor respuesta tanto en pacientes con EA37,71-74 como en pacientes con EspAax-nr63,75. La mayor actividad de la enfermedad al inicio del tratamiento constituye uno de los mayores factores predictivos de buena respuesta que aparece en la mayoría de estudios tanto en pacientes con EA como en pacientes con EspAax-nr63,75. Diversos estudios apuntan a que los individuos de sexo masculino presentarían una mejor respuesta terapéutica71,73,74. Por el contrario, el sexo femenino76 y una mayor discapacidad al inicio del tratamiento (BASFI inicial elevado) se asociarían a menor respuesta terapéutica37,72,74. El sobrepeso expresado como índice de masa corporal (IMC) elevado se ha asociado en algunos estudios con menor respuesta al tratamiento, y se ha descrito además una asociación independiente entre IMC>30 y fallo al tratamiento76. Los fumadores presentan menor reducción de la actividad de la enfermedad (BASDAI, ASDAS), especialmente cuando la PCR es alta, y peor respuesta al tratamiento, incluso si son exfumadores77. Con respecto al HLA B27, existen datos contradictorios, si bien la mayoría de estudios apuntan a una mejor respuesta terapéutica en los individuos B27 positivos74. En un reciente estudio se sugiere que una respuesta precoz a la terapia anti-TNF es uno de los factores que más se asocia con buena respuesta a largo plazo78.
No se dispone por el momento de factores predictivos contrastados de respuesta a la terapia con secukinumab.
Numerosos estudios evalúan la utilidad de nuevos biomarcadores para mejorar la predicción de respuesta a la terapia con anti-TNF. La calprotectina es uno de los que presenta mejores resultados, si bien hasta la fecha ninguno de ellos ha demostrado resultados concluyentes79.
Existen numerosos factores asociados a la respuesta a la terapia anti-TNF. Ninguno de ellos, de forma aislada o en combinación, permite predecir con seguridad la respuesta final observada, por lo que su ausencia no debe impedir la instauración de la TB. Sin embargo, y en base a los resultados expuestos, parece importante, a la hora de mejorar la respuesta terapéutica a la TB, no retrasar el tratamiento en los pacientes activos pese al tratamiento con AINE, y mantener unos hábitos de vida saludables (evitar tabaco y sobrepeso).
3. Se recomienda valorar los factores predictivos de progresión de daño estructural en la indicación de TB (GR: D; NE: 5; GA: 100%).
Comentarios derivados de esta recomendación:
La TB es eficaz en reducir la inflamación ósea espinal y de sacroilíacas. Datos recientes sugieren que la TB es también eficaz en reducir la progresión radiográfica en EA (NE: 1b, 4; GA: 78%).
Entre los factores predictivos de daño estructural se incluyen: el daño radiográfico basal, la afectación en RM, el sexo, el tabaco y la actividad de la enfermedad (NE: 2b, 4; GA: 100%).
En pacientes con TB es aconsejable disponer de una radiografía basal y realizar una monitorización del daño estructural, especialmente en aquellos con mayor riesgo de progresión (NE: 5; GA: 100%).
La presencia de lesión radiográfica basal (sindesmofitos en la radiografía de columna vertebral) es el factor predictivo de progresión más importante80,81. Otros factores que se han asociado a una mayor progresión de la lesión radiográfica son el sexo masculino, el tabaco y especialmente la persistencia de actividad inflamatoria de la enfermedad (valorada clínicamente por niveles séricos de PCR y/o presencia edema óseo en la RM)81,82.
La TB ha demostrado un efecto precoz de inhibición de la inflamación ósea espinal y de SI valorada por RM ya objetivable desde las 6semanas del inicio del tratamiento. Este efecto es claramente superior al obtenido con el uso de AINE o sulfasalazina (SSZ)62,83-85. Existe una «ventana de oportunidad terapéutica» en las fases más precoces de la enfermedad (EspAax-nr) donde la TB parece ser especialmente eficaz en la inhibición de los focos de osteítis a nivel de SI o a nivel espinal86. La reducción del edema óseo tras TB se correlaciona con el control de la actividad clínica de la enfermedad y la PCR, especialmente en EspAax-nr. Sin embargo, en los primeros estudios a 2años la desaparición del edema óseo tras la TB con anti-TNF, especialmente en pacientes con enfermedad más evolucionada, no demostró frenar la aparición de focos de degeneración grasa y la progresión del daño estructural (sindesmofitos)87-89. En este sentido existen datos que apoyan que la asociación de inflamación más degeneración grasa, o la degeneración grasa sin inflamación previa, se asocian significativamente con la formación de sindesmofitos tras 5años de tratamiento con infliximab90. Datos recientes, sin embargo, apuntan a que el tratamiento con fármacos anti-TNF de forma continuada durante periodos de más de 4años se asocia a una reducción significativa de la progresión del daño estructural espinal valorado por radiografía simple (mSASSS)33,60. La progresión del daño estructural fue menor cuanto más precoz fue el inicio del tratamiento, especialmente en aquellos casos de <5años de evolución de la enfermedad, y cuanto mayor fue el tiempo de mantenimiento del tratamiento con terapia anti-TNF33.
Los datos de los ensayos principales de secukinumab valorados a los 2años parecen indicar que la reducción de la lesión osteítica se asocia a no progresión de las lesiones grasas y a una reducción de la progresión del daño estructural a nivel espinal. Los pacientes con factores de riesgo mayores de progresión radiográfica (sindesmofitos basales previos y PCR alta) fueron los que presentaron mayor reducción en la progresión61. Los datos, esperanzadores, son aún preliminares y precisan confirmarse en la práctica clínica y en periodos más prolongados para valorar posibles diferencias con los anti-TNF.
Existe poca información al respecto de la progresión radiográfica y la TB combinada con AINE. En un único estudio con 40 pacientes con EA la progresión radiográfica a los 2años valorada por mSASSS fue menor en el grupo de tratamiento combinado con anti-TNF +AINE que en el grupo tratado solo con anti-TNF91. Pero los datos de que disponemos son aún preliminares y escasos para poder apoyar esta actitud terapéutica de forma sistemática.
Dado que la progresión del daño estructural es uno de los factores clave para determinar el grado de discapacidad a largo plazo92, en pacientes con TB es aconsejable disponer de una radiografía basal y realizar una monitorización radiológica del daño estructural, especialmente en aquellos con mayor riesgo de progresión radiográfica. No existe un consenso sobre la frecuencia en realizar el control radiográfico, pues este depende del grado de actividad de la enfermedad entre otros múltiples factores, por lo que se suele dejar a criterio médico. Sin embargo, en pacientes activos y en la línea de las recientes recomendaciones EULAR48 parece razonable su realización en periodos de 2SASSaños.
4. Se recomienda que, después del fracaso a un primer anti-TNF, el paciente sea tratado con otro anti-TNF o anti-IL17 (GR D; NE: 4; GA: 100%).
El tratamiento con un segundo anti-TNF o secukinumab en pacientes con EA que han fallado a un anti-TNF previo es eficaz en un porcentaje elevado de pacientes, aunque la experiencia con secukinumab es aún limitada. No obstante, la respuesta clínica observada es menor a la que experimentan los pacientes que reciben un primer biológico93-99. No hay datos sobre diferencias en eficacia ni en supervivencia entre el cambio de anti-TNF o el cambio de diana terapéutica (secukinumab). La eficacia disminuye con el uso de sucesivos tratamientos biológicos, pero sigue encontrándose respuesta tras el tercer biológico93-99. Hay datos que sugieren una mejor respuesta en los pacientes que cambian a un segundo anti-TNF por ineficacia secundaria o toxicidad del primero frente a los pacientes que presentan falta primaria de respuesta a anti-TNF.
La supervivencia del fármaco fue menor en los sucesivos cambios de anti-TNF93,97; no obstante, las diferencias no llegan a alcanzar significación estadística, posiblemente por falta de tamaño muestral. Aunque sí parece que hay diferencias de supervivencia en favor de los que cambian por ineficacia secundaria y toxicidad frente a ineficacia primaria100. En estas situaciones de ineficacia primaria del anti-TNF sería razonable valorar el cambio de diana terapéutica y usar secukinumab.
No existe todavía evidencia sobre la eficacia del cambio a anti-TNF tras fracaso a secukinumab, pero el grupo de panelistas considera razonable utilizar un anti-TNF en estas situaciones. La recomendación se podía quizá haber formulado cambiando el término «primer anti-TNF» por «primer fármaco biológico», pero en el momento de realizar este documento no había evidencia ni experiencia sobre el fracaso a anti-IL-17A y la utilización posterior de un anti-TNF.
No existen datos sobre el cambio de terapia anti-TNF en EspAax-nr, pero se asume que la respuesta no diferiría de la de los pacientes con EA.
No se han encontrado evidencias de eficacia de otros fármacos biológicos, como rituximab o abatacept, tras el fracaso a terapia anti-TNF. En el caso de ustekinumab no se han publicado datos al respecto.
5. Se recomienda valorar la posibilidad de reducir la dosis del fármaco anti-TNF en los pacientes que hayan alcanzado remisión o baja actividad de la enfermedad de forma mantenida (GR D; NE: 2b, 4; GA: 100%).
6. Se recomienda que, ante un aumento de la actividad de la enfermedad, en aquellos pacientes en los que se ha reducido la dosis de anti-TNF se considere el aumento de las dosis, volviendo a las dosis previas o a dosis estándar (GR: D; NE: 5; GA: 100%).
En la revisión sistemática de la literatura sobre este tema encontramos 13estudios101-113. De ellos, pocos especifican el tiempo en remisión de la enfermedad antes de realizar la optimización; sin embargo, en la mayoría de ellos el periodo previo oscila entre 6meses y un año105,111-114, por lo que en la práctica clínica parece razonable esperar al menos 6meses de remisión de la enfermedad antes de considerar la optimización.
La tasa de recaídas en pacientes con EA a los que se aplicaron estrategias de reducción de las dosis osciló entre el 0 y el 47%101,102,104-106,108,109,111-113. Además, un estudio reciente comunicado en el congreso ACR de 2016115 demostró que en pacientes con EA en remisión clínica (BASDAI≤2, sin artritis o entesitis y PCR normal) mantenida un mínimo de 6meses, la pauta de tratamiento con dosis reducidas de anti-TNF (aproximadamente un 40% de la dosis estándar) no fue significativamente inferior, ni en eficacia ni en seguridad, a la pauta con dosis estándar.
No hay ningún estudio dirigido específicamente a evaluar factores que predigan el desenlace tras la reducción de dosis de la TB. Algunos apuntan que la menor duración de la remisión antes de la reducción de dosis, la menor duración del tratamiento y la menor duración de la enfermedad son factores asociados a la presencia de recaídas111. Por el contrario, un mayor ASQoL antes de la optimización, el sexo masculino y no haber recibido previamente anti-TNF se asociaron con buena respuesta a la optimización109,112. No se considera una opción razonable reducir la TB en pacientes con EspAax que no han conseguido el objetivo terapéutico (remisión o baja actividad), pues la persistencia de la actividad de la enfermedad es el factor más importante para el rebrote clínico.
Hasta la fecha solo disponemos de resultados de optimización con fármacos anti-TNF. Se desconocen los efectos a largo plazo de la reducción de dosis de TB sobre la supervivencia del fármaco o el daño estructural. Datos recientes sugieren que los pacientes con lesión radiográfica vertebral previa que van con dosis reducida progresarían más que los que reciben dosis plenas116.
Los datos respecto a la respuesta a la optimización en pacientes con EspAax-nr son demasiado escasos como para formular una recomendación basada en la evidencia. Sin embargo, la misma carga de enfermedad de ambas poblaciones55,56 y la tasa de respuesta observada a la TB similar en ambas poblaciones16,62-64 aconsejan en pacientes EspAax-nr seguir la misma pauta que en los pacientes con EA.
En la mayoría de estudios en los que, tras la recaída, se volvió a las dosis previas a la optimización o a dosis estándar, se recuperaba la respuesta clínica con unas tasas de respuesta por encima del 75%104,106,109,112.
No existe una definición de recaída establecida, y se han usado diferentes medidas para considerar brote de actividad de la enfermedad. El panel de expertos ha considerado rebrote clínico cualquier situación que suponga una pérdida del objetivo terapéutico fijado al inicio del tratamiento, ya sea por incremento del BASDAI y la PCR o por un aumento del ASDAS. El panel considera también fundamental tener en cuenta a la hora de decidir el manejo de este rebrote, bien sea reajustando el tratamiento con AINE y/o reinstaurando la TB (volviendo a las dosis previas a la optimización o a dosis estándar), la valoración global que el médico haga del mismo y de sus circunstancias (gravedad del rebrote, persistencia en el tiempo y/o asociación a otras manifestaciones), así como la opinión del paciente.
Si la reducción del tratamiento es una opción a considerar en pacientes que han alcanzado el objetivo terapéutico y que lo mantienen durante un cierto tiempo, la interrupción del tratamiento no es un objetivo en sí mismo y no hay datos que avalen de forma sistemática esta actitud. En base a algunas series y casos aislados se ha sugerido la posibilidad de valorar suspender el tratamiento de forma individualizada en pacientes que han alcanzado el objetivo terapéutico y que lo mantienen después de reducir al máximo el tratamiento biológico117. Sin embargo, los datos disponibles son muy escasos y no permiten actualmente apoyar esta actitud terapéutica.
7. Se recomienda, en pacientes con EspAax que presenten manifestaciones periféricas activas, valorar la utilización de sulfasalazina y/o infiltraciones locales con glucocorticoides previamente a la TB (GR: B; NE: 2b; GA: 100%).
Entre un 30 y un 50% de los pacientes con EspAax presentan también afectación periférica en forma de artritis, entesitis o dactilitis, con una frecuencia similar entre pacientes con EA y EspAax-nr118. En los pacientes con EspAax con síntomas axiales estables pero que presentan manifestaciones periféricas activas, en especial de artritis y dactilitis, debe valorarse inicialmente el tratamiento con AINE y las infiltraciones locales con glucocorticoides. En los pacientes con entesitis, en caso de realizar infiltraciones locales, se debe evitar la inyección directa sobre el tendón, sobre todo en los de gran tamaño, como el tendón de Aquiles, el rotuliano o el del cuádriceps.
Los FAME no han demostrado su eficacia para tratar los síntomas de enfermedad axial, ni tampoco existe evidencia que apoye su uso en entesitis. Pueden estar indicados en pacientes con artritis activa que han presentado intolerancia o ausencia de respuesta a los tratamientos anteriores. La sulfasalazina ha mostrado, en estudios controlados, que es efectiva, aunque de forma modesta, sobre las manifestaciones articulares a dosis de 2-3g al día119,120. No existen recomendaciones basadas en la evidencia para apoyar el tratamiento con otros FAME como metotrexato o leflunomida, y por este motivo su elección dependerá de las comorbilidades, de la experiencia del clínico y de las preferencias del paciente. En cualquier caso, el tratamiento con FAME se debe mantener un mínimo de 3meses antes de considerar su ineficacia.
La TB estará indicada en pacientes con EspAax con manifestaciones periféricas activas que no responden al tratamiento convencional. La eficacia de los anti-TNF y el secukinumab no solo se ha demostrado en pacientes con EspAax con o sin manifestaciones periféricas asociadas26,121-123, sino también en otras formas de EspA en donde la artritis periférica es una manifestación clínica predominante, como la artritis psoriásica124,125 y la artritis relacionada con la enfermedad inflamatoria intestinal126.
8. Se recomienda, en pacientes con EspA periférica persistentemente activa sin respuesta a tratamiento convencional (AINE, FAME, infiltraciones locales), valorar el tratamiento con fármacos anti-TNF (GR: D; NE: 5; GA: 78%).
Los pacientes con EspA de predominio exclusivamente periférico constituyen un subgrupo particular, pero si se excluye a los pacientes con artritis psoriásica, el resto, al ser un grupo de mayor heterogeneidad clínica, no suelen incluirse en ensayos clínicos controlados para la valoración de nuevos tratamientos. Por este motivo, son escasos los estudios que valoran el tratamiento de estos pacientes; en su mayoría no son ensayos clínicos controlados y están realizados con un número pequeño de pacientes. Aunque no existen estudios específicos con FAME, los resultados en pacientes con artritis psoriásica con afectación periférica, así como la práctica clínica, sugieren su utilidad. Varios estudios con adalimumab y golimumab, dos de ellos controlados, demuestran una clara eficacia de la terapia con anti-TNF en estas situaciones, aunque todos ellos presentan ciertas limitaciones metodológicas127-129. También se ha observado la eficacia del tratamiento con anti-TNF en varios estudios observacionales realizados en pacientes con artritis reactiva130,131 que incluso permitió suspender el tratamiento por remisión clínica en un tercio de los pacientes131.
No existen ensayos controlados aleatorizados (ECA) en los que se utilicen otras TB, ni tampoco estudios a largo plazo para confirmar la eficacia y seguridad de los anti-TNF en pacientes con EspA periféricas. Sin embargo, existen numerosos ECA en pacientes con EspAax y artritis psoriásica donde se demuestra que los distintos anti-TNF existentes son eficaces en el tratamiento de la artritis periférica, la entesitis y la dactilitis121-124. Por este motivo se aconseja el tratamiento con anti-TNF en pacientes con EspA periféricas activos y refractarios a terapia convencional incluidos FAME, según se ha definido en apartados anteriores.
9. Se recomienda, en pacientes con EspAax y uveítis anterior recidivante grave o uveítis crónica refractaria a la terapia convencional, considerar el tratamiento con anticuerpos monoclonales anti-TNF (GR: D; NE: 5; GA: 100%).
Está fuera del objetivo de este documento dar recomendaciones sobre el tratamiento oftalmológico de las uveítis asociadas a EspA, pero hay que mencionar que, dada la eficacia mostrada en esta situación por las distintas terapias biológicas, estas deberían considerarse de conformidad con el oftalmólogo en pacientes con uveítis anteriores agudas refractarias a terapia convencional, o uveítis recidivantes graves refractarias a terapia convencional (muy recurrentes con más de 3 brotes al año o presencia de secuelas oculares que comprometan la visión del ojo).
Los datos publicados y comunicados de estudios y registros sugieren que la terapia con anticuerpos monoclonales anti-TNF reduce el número de nuevos episodios de uveítis en pacientes con EspAax de forma más intensa que el tratamiento con etanercept132-135. Sin embargo, no existe ninguna evidencia que etanercept aumente el número de episodios de uveítis en estos pacientes. Además, en un estudio controlado comparando etanercept frente a sulfasalazina, fármaco habitualmente empleado para reducir los brotes de uveítis en pacientes con EspAax, no se encontraron diferencias significativas en la tasa de aparición de uveítis entre ambos tratamientos136.
No existen evidencias suficientes de la eficacia de las nuevas terapias anti-IL-12/23 o anti-IL-17 en el tratamiento de la uveítis asociada a EspA. Sin embargo, los datos procedentes de los diferentes ensayos clínicos de secukinumab no apoyan que su administración se asocie a un aumento en la incidencia de los brotes de uveítis en estos pacientes26.
10. Se recomienda, en pacientes con EspAax y enfermedad inflamatoria intestinal activa o antecedentes de la misma, considerar el tratamiento con anticuerpos monoclonales anti-TNF (GR: D; NE: 5; GA: 100%).
Está también fuera del objetivo de este documento dar recomendaciones sobre el tratamiento específico de las EspA asociadas a enfermedades inflamatorias intestinales, pero hay que mencionar que, dada la eficacia mostrada en esta situación por los anticuerpos monoclonales anti-TNF, estos deberían considerarse, de conformidad con el especialista en aparato digestivo, en dichos pacientes, intentando coordinar el manejo de los diferentes dominios, articular y digestivo, de la enfermedad. Los fármacos biológicos actualmente indicados en España para la enfermedad de Crohn o la colitis ulcerosa son infliximab, adalimumab y vedolizumab (anticuerpo monoclonal humanizado de tipo IgG1 que se une a la integrina α4β7). Este último no tiene eficacia en la afectación articular, por lo que su uso está restringido a la actividad intestinal. Golimumab está indicado en colitis ulcerosa pero no en enfermedad de Crohn, certolizumab no está aprobado por la EMA para ninguna enfermedad inflamatoria intestinal, pero sí lo está por la FDA para el tratamiento de la enfermedad de Crohn.
El receptor soluble, etanercept, no tiene indicación en la enfermedad inflamatoria intestinal, y no hay datos de que tenga eficacia en esta situación. Sin embargo, tampoco hay datos de que su uso agrave o aumente el número de episodios de enfermedad inflamatoria intestinal en pacientes con EA137.
Ustekinumab ha sido aprobado recientemente por la FDA para el tratamiento de la enfermedad de Crohn refractaria a anti-TNF, en base a la evidencia publicada138. Aunque ustekinumab tiene datos preliminares de eficacia en pacientes con EA30, no dispone aún de datos definitivos y, por tanto, no tiene la indicación aprobada para pacientes con EspAax.
No existen datos que apoyen la eficacia de secukinumab en el tratamiento de la enfermedad inflamatoria intestinal (Crohn y colitis ulcerosa) asociada a EspAax. En un estudio en pacientes con enfermedad de Crohn activa moderada/grave, el tratamiento con secukinumab no demostró ninguna eficacia y presentó una tasa de acontecimientos adversos superior al placebo29. Sin embargo, de los datos publicados en los estudios de registro con secukinumab en EA, y las extensiones de los mismos, no se evidencia que el fármaco aumente el número de episodios de enfermedad inflamatoria intestinal en estos pacientes139.
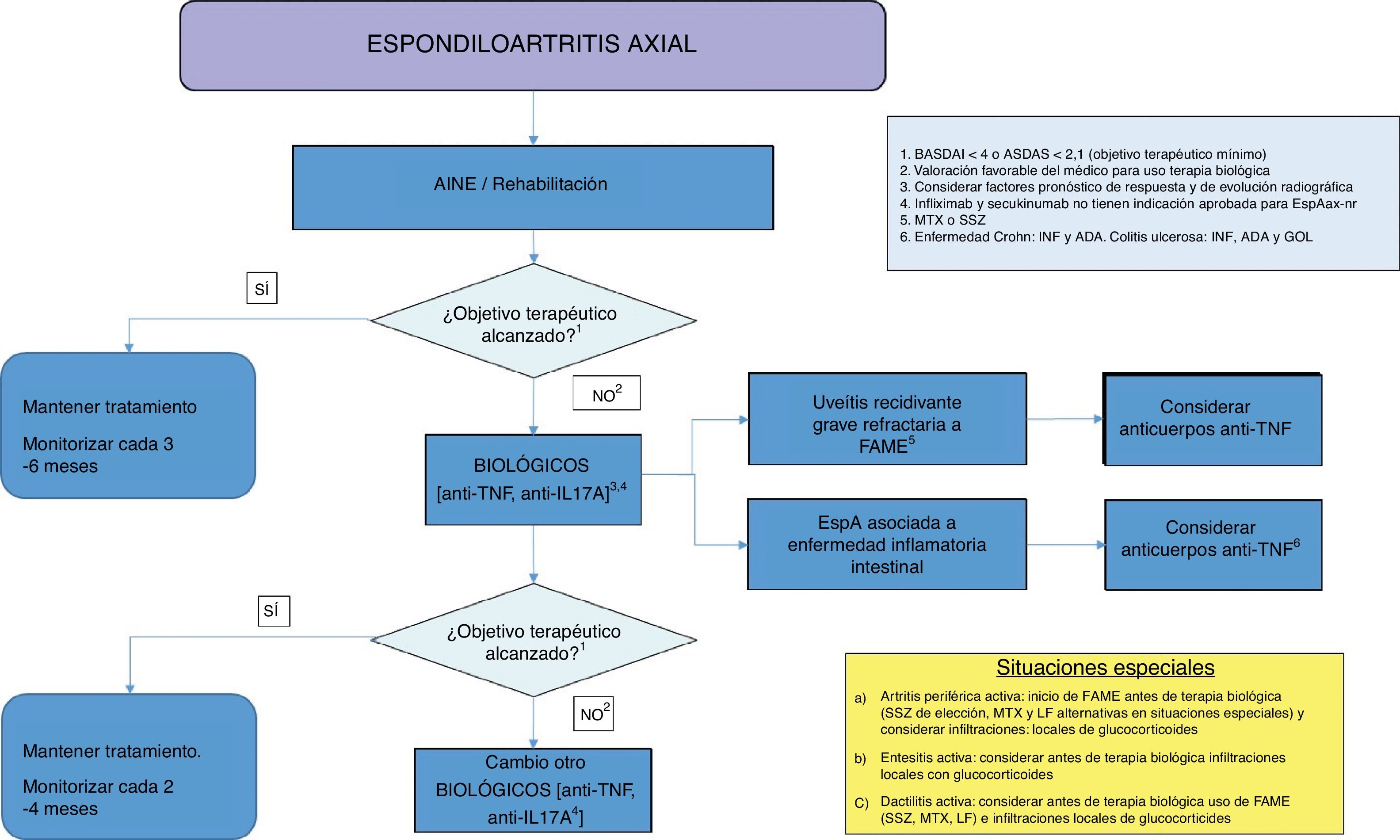
DiscusiónEl presente documento forma parte de la tercera actualización del Consenso de la SER sobre el uso de TB en las EspAax. El documento se apoya en las revisiones y recomendaciones de la actualización reciente de la ESPOGUÍA3 y en una revisión crítica del consenso previo14, y está basado en la mejor evidencia científica disponible y en la experiencia clínica de expertos. Con respecto al anterior consenso, destaca un cambio de estructura, basado en la elaboración de una serie de recomendaciones que se apoyan en evidencia científica y se exponen en una tabla. Algunas de las recomendaciones incorporan aclaraciones adicionales, con información relevante que los panelistas hemos creído necesario destacar. Finalmente, el texto incorpora también un algoritmo de tratamiento en base a las recomendaciones efectuadas (fig. 1). Creemos sinceramente que este formato va a facilitar la toma de decisiones por parte de nuestros compañeros dirigidas a los pacientes con EspAax que requieren TB.
Algoritmo de tratamiento de la espondiloartritis axial.
ADA: adalimumab; AINE: antiinflamatorios no esteroideos; anti-IL17: inhibidora de la interleucina 17; anti-TNF: inhibidor del factor de necrosis tumoral; ASDAS: ASAS-endorsed disease activity score; BASDAI: Bath Ankylosing Spondylitis Disease Activity Index; FAME: fármacos antirreumáticos modificadores de la enfermedad; GOL: golimumab; INF: infliximab; LF: leflunomida; MTX: metotrexato; SSZ: sulfasalazina.
En estas recomendaciones se ha querido destacar de forma explícita, ya en la introducción, la unidad que, a criterio de los panelistas, constituye la EspAax. Un grupo de procesos con características clínicas y carga de enfermedad similares y que, por tanto, con matices en su indicación, todos ellos pueden ser tributarios de TB.
En el apartado de nuevos fármacos biológicos disponibles se ha incluido certolizumab pegol, un nuevo anti-TNF, con un nivel de evidencia en el tratamiento de EspAax similar al de los otros fármacos anti-TNF disponibles. Se ha incorporado también el concepto de biosimilares, y sus indicaciones. Actualmente tenemos disponibles 3 biosimilares de infliximab y un biosimilar de etanercept. Finalmente, y posiblemente lo más novedoso, en el capítulo de fármacos se ha incorporado secukinumab (inhibidor de IL-17A), la primera molécula con una diana terapéutica diferente al TNF. La incorporación de secukinumab no solo es relevante porque amplía el espectro de posibles dianas terapéuticas, sino porque constituye la culminación de toda una serie de descubrimientos realizados en esta última década en torno a la barrera mucosa intestinal y el eje IL-23/IL-17, que han permitido entender mejor la fisiopatología de las EspA140.
Otra de las aportaciones incluida en el documento es, sin abandonar definitivamente el BASDAI, la incorporación de forma preferente del índice de actividad ASDAS para la valoración de la actividad de la enfermedad, así como para establecer los objetivos terapéuticos. Esta decisión está avalada por la apuesta decidida, por parte de los panelistas, de un régimen terapéutico basado en la consecución de objetivos (estrategias T2T, en la literatura anglosajona), con control estricto de la enfermedad, situación en la que ASDAS ha demostrado claramente ser superior a BASDAI para predecir la evolución de los pacientes45.
En el apartado de pacientes con EA refractaria a terapia convencional se ha decidido situar a los fármacos anti-TNF y secukinumab al mismo nivel. Esta decisión, plasmada también en el algoritmo terapéutico, es algo diferente a otras recomendaciones internacionales recientemente publicadas2, pero se basa, en nuestro criterio, en la ausencia de diferencias entre las diferentes moléculas, derivada de los resultados de los ensayos de registro12,13,26. Los panelistas son, sin embargo, conscientes de que los datos de eficacia y seguridad disponibles para los fármacos anti-TNF son mucho más numerosos y emanan de los ensayos clínicos y de la práctica clínica habitual durante más de dos décadas, lo que sitúa a estos fármacos en un lugar preeminente en el tratamiento de estos pacientes.
Los nuevos datos publicados en la literatura han permitido incorporar recomendaciones nuevas sobre factores predictivos de respuesta y de progresión del daño estructural que deben facilitar la toma de decisiones en determinadas circunstancias. Se han añadido también recomendaciones de tratamiento en pacientes refractarios a anti-TNF (en esta ocasión de especial interés, al disponer por primera vez de una molécula dirigida a una diana terapéutica diferente al TNF). Finalmente, recomendaciones para la optimización de la TB en pacientes que han alcanzado y mantenido durante un tiempo el objetivo terapéutico. Estas últimas, con una evidencia científica aún pobre, pero avaladas por la práctica clínica.
Las recomendaciones se han escrito en base a la evidencia clínica, y no incorporan voluntariamente ninguna referencia a aspectos farmacoeconómicos. Los panelistas consideran que estos aspectos son cambiantes en el tiempo y diferentes en los distintos territorios y hospitales del país, y por tanto un tema a considerar por cada reumatólogo, en base a sus condiciones particulares y específicas. Sin embargo, en situación de idéntica eficacia y seguridad, el coste debe ser un elemento a tener en cuenta a la hora de tomar la decisión compartida médico-paciente sobre la TB a prescribir. Finalmente, en este documento se incorporan también recomendaciones para el manejo con TB de pacientes con EspAax y artritis periférica, así como en pacientes con presencia de manifestaciones extraarticulares. Incluye el texto también un pequeño apartado para las EspA periféricas, pues si bien no forman parte del objetivo de estas recomendaciones, pueden ser de utilidad a nuestros compañeros y no se hallan incluidas en ningún otro consenso.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciaciónFundación Española de Reumatología.
Conflicto de interesesJordi Gratacós Masmitjà ha recibido financiación de UCB, MSD, Pfizer, Abbvie, Janssen, Celgene y Novartis para la asistencia a cursos/congresos y en concepto de ponencias; financiación de Abbvie, MSD y Pfizer para la realización de programas educativos o cursos y por participar en una investigación, y ha recibido ayuda económica de Pfizer, Abbvie, Janssen, Celgene y Novartis en concepto de consultoría para compañías farmacéuticas u otras tecnologías.
Cristina Fernández Carballido ha recibido financiación de Abbvie, Pfizer, MSD, Celgene y Novartis para la asistencia a cursos/congresos; honorarios de Abbvie, UCB, Celgene y Novartis en concepto de ponencias; financiación de Abbvie y MSD para la realización de programas educativos o cursos; financiación de Novartis por participar en una investigación, y ha recibido ayuda económica de Abbvie, Celgene y Novartis en concepto de consultoría para compañías farmacéuticas u otras tecnologías.
Xavier Juanola Roura ha recibido financiación de Abbvie, Pfizer y MSD para la asistencia a cursos/congresos; honorarios de Abbvie, Pfizer, UCB y MSD en concepto de ponencias; financiación de Abbvie por participar en una investigación, y ha recibido ayuda económica de Celgene, Novartis y Abbvie en concepto de consultoría para compañías farmacéuticas u otras tecnologías.
Luis Francisco Linares Ferrando ha recibido financiación de Abbvie, Pfizer, Novartis y MSD para la asistencia a cursos/congresos; honorarios de Abbvie, Pfizer, Grunenthal, Jansen y MSD en concepto de ponencias; financiación del Colegio Médico de Murcia para la realización de programas educativos o cursos; financiación de Abbvie y Novartis por participar en una investigación, y ha recibido ayuda económica de MSD en concepto de consultoría para compañías farmacéuticas u otras tecnologías.
Eugenio de Miguel Mendieta ha recibido financiación de Abbvie, Pfizer, Roche y MSD para la asistencia a cursos/congresos; honorarios de Abbvie, Janssen, Roche, UCB, Menarini, Celgene y MSD en concepto de ponencias; financiación de Abbvie y MSD para la realización de programas educativos o cursos; financiación de Pfizer por participar en una investigación, y ha recibido ayuda económica de Abbvie y Astra-Zeneca en concepto de consultoría para compañías farmacéuticas u otras tecnologías.
Santiago Muñoz Fernández ha recibido financiación de Abbvie, Pfizer, Bioibérica, UCB, Actelion, Roche, Lilly y MSD para la asistencia a cursos/congresos; honorarios de Janssen, Novartis, UCB, MSD, Abbvie y Pfizer en concepto de ponencias; financiación de UCB, Abbvie, Janssen, MSD, Celgene, Sanofi y Roche para la realización de programas educativos o cursos, y ha recibido ayuda económica de BMS, Abbvie, Novartis, Janssen, Pfizer, Sanofi y Roche en concepto de consultaría para compañías farmacéuticas u otras tecnologías.
Victoria Navarro Compán ha recibido financiación de Abbvie, Bristol, MSD, Pfizer y UCB para la asistencia a cursos/congresos; honorarios de Abbvie, BMS, Novartis y Roche en concepto de ponencias y asesoría, y financiación de Abbvie para proyectos de investigación.
Jose Luis Rosales Alexander ha recibido financiación de Pfizer, Roche, BMS, Novartis, Celgene y UCB para la asistencia a cursos/congresos; honorarios de UCB como asistente a mesa redonda y consultoría; financiación de FAES para la realización de programas educativos o cursos, y ha recibido ayuda económica de Grunenthal en concepto de consultoría.
Pedro Zarco Montejo ha recibido financiación de Abbvie, Pfizer y MSD para la asistencia a cursos/congresos; honorarios de Abbvie, Pfizer, UCB y MSD en concepto de ponencias, y de Pfizer y UCB en concepto de consultoría para compañías farmacéuticas u otras tecnologías.
El grupo de expertos del presente trabajo quiere manifestar su agradecimiento a los facultativos de reumatología que han participado en la fase de revisión de la evidencia: Miguel Ángel Abad Hernández, Gloria Candelas Rodríguez, María Betina Nishishniya Aquino, Claudia Pereda Testa y Ana Ortiz García. También quieren agradecer al Dr. Federico Díaz González, director de la Unidad de Investigación de la SER, por su participación en la revisión del manuscrito final y por contribuir a preservar la independencia de este documento, y a Daniel Seoane, metodólogo de la SER, por su colaboración en el presente trabajo.