El síndrome de Sjögren (SS) es una enfermedad autoinmune con un amplio espectro de manifestaciones clínicas que puede generar un importante impacto en la calidad de vida del paciente. Para hacer una evaluación objetiva de los componentes de la enfermedad se han diseñado herramientas clinimétricas como el ESSPRI. El objetivo de este estudio es hacer una adaptación de esta escala al idioma castellano.
Materiales y métodosEstudio transversal de validación de escalas clinimétricas llevado a cabo en Cali, Colombia. Se realizó una traducción de la versión original en inglés del ESSPRI al castellano y se aplicó a pacientes con SS, al igual que el PROFAD y el ESSDAI, como marcador de actividad. Se calculó el índice de confiabilidad del cuestionario en castellano con coeficiente de alfa de Cronbach, así como el coeficiente de correlación de Spearman para comparar las escalas. Se evaluaron también características demográficas, clínicas y de laboratorio.
ResultadosSe aplicó el ESSPRI, PROFAD y ESSDAI a 42 pacientes con SS; el 97,62% fueron mujeres. El resultado promedio del ESSPRI fue 5,8 (±4,6), con un coeficiente de confiabilidad de 0,8034 y una correlación con el PROFAD de 0,5800 (p=0,0001) y de −0,0848 (p=0,593) con el ESSDAI.
Discusión y conclusionesLa confiabilidad con la versión aplicada del ESSPRI en castellano fue adecuada. Se encontró una discordancia entre esta escala y el ESSDAI, lo cual remarca la importancia de aplicar ambas herramientas para asegurar un seguimiento objetivo del control de la enfermedad y su impacto en la calidad de vida de los pacientes con SS.
Sjögren's syndrome (SS) is an autoimmune disease with a wide spectrum of clinical manifestations that can have an important impact on the patient's quality of life. To make an objective evaluation of the components of the disease, clinimetric tools such as the ESSPRI have been designed. The objective of this study is to adapt this scale to the Spanish language.
Materials and methodsThis is a cross-sectional study to validate clinimetric scales, carried out in Cali, Colombia. A translation of the original English version of ESSPRI into Spanish was made and applied to patients with SS, as well as PROFAD and ESSDAI, as an activity marker. The reliability index of the questionnaire in Spanish with Cronbach's alpha coefficient and Spearman's correlation coefficient were calculated to compare the scales. Demographic, clinical and laboratory characteristics were also evaluated.
ResultsESSPRI, PROFAD and ESSDAI were applied to 42 patients with SS, 97.62% were women. The average result of the ESSPRI was 5.8 (±4.6), with a reliability coefficient of .8034 and a correlation with PROFAD of .5800 (P=.0001), and of −.0848 (P=.593) with ESSDAI.
Discussion and conclusionsReliability with the applied version of ESSPRI in Spanish was adequate. A discrepancy was found between this scale and ESSDAI, which highlights the importance of applying both tools to ensure objective monitoring of disease control and its impact on the quality of life of patients with SS.
El síndrome de Sjögren (SS) es una enfermedad autoinmune sistémica de carácter crónico que se caracteriza por generar una afectación de las glándulas exocrinas y por presentar lo que se conoce como «síndrome seco», lo cual se traduce principalmente en la aparición de xeroftalmía y xerostomía. Hasta un 50% de los pacientes con SS pueden presentar otras manifestaciones extraglandulares, como son a nivel musculoesquelético, pulmonar, gastrointestinal, hepático, hematológico, vascular, dermatológico, renal y neurológico1. El SS se puede asociar a otras enfermedades autoinmunes, como por ejemplo artritis reumatoide en un 20-32%, lupus eritematoso sistémico en un 15-36% y esclerosis sistémica en un 20-32%, entre otras2-4.
El SS afecta la calidad de vida de los pacientes en aspectos físicos, psicológicos y sociales5. Por ejemplo, los síntomas como ojo seco, boca seca, fatiga y dolor articular son algunos de los muchos síntomas que tienen impacto en la funcionalidad y que se pueden tornar incapacitantes6.
Se han creado a través del tiempo múltiples herramientas clinimétricas que permiten al clínico evaluar, a través de escalas, la actividad, la severidad, el daño de una enfermedad, así como el impacto en la calidad de vida los pacientes7. En el caso del SS, se han desarrollado cuestionarios como el Sicca Symptoms Inventory (SSI), para evaluar los síntomas de sequedad producidos por el SS8; el Profile of Fatigue and Discomfort (PROFAD), enfocado en la presencia o no de fatiga9; el Sjögren's Systemic Clinical Activity Index’ (SCAI), que incluye manifestaciones sistémicas10, entre otros. Recientemente se validaron el EULAR Sjögren's Syndrome Disease Activity Index (ESSDAI) y el EULAR Sjögren's Syndrome Patient Reported Index (ESSPRI)11. El ESSDAI es actualmente considerado como el estándar de oro para medir la actividad de la enfermedad12, mientras que el ESSPRI cuantifica la severidad de los síntomas incapacitantes del SS: dolor, sequedad y fatiga13. El ESSPRI fue diseñado en el año 2011, con adecuada correlación con escalas como el PROFAD, con la diferencia de que es considerablemente más sencillo y menos exhaustivo que este9,14.
En la actualidad el ESSPRI se encuentra en inglés y ya ha sido traducido y validado al portugués15. El presente estudio pretende realizar una adaptación del ESSPRI en su versión original al castellano para facilitar su aplicabilidad en todos los pacientes con SS en estudios clínicos y en la práctica clínica diaria en países de habla hispana.
MétodosSe realizó un estudio transversal de validación de escalas clinimétricas en un centro de referencia de enfermedades autoinmunes como lo es la Fundación Clínica Valle del Lili, en Cali, Colombia. Se seleccionaron pacientes mayores de 18años con clasificación de SS según los criterios del Consenso Americano-Europeo del 201616, independientemente de la coexistencia o no de otra enfermedad autoinmune (poliautoinmunidad) o del tratamiento recibido, que asistieron a consulta de control de su enfermedad al servicio de Reumatología entre abril de 2018 y marzo de 2019, en una única evaluación. Los criterios de exclusión correspondieron a los mencionados en los criterios de clasificación de SS (historia de radiación en cabeza y cuello, infección por virus de la hepatitisC activa, infección por VIH, sarcoidosis, amiloidosis, enfermedad injerto vs. huésped y enfermedad relacionada por IgG4).
Se realizó una adaptación cultural de la versión original en inglés de la escala ESSPRI a través de la realización de traducción-retrotraducción, y las versiones de la escala fueron evaluadas por un comité de revisión constituido por médicos especialistas con experiencia en el manejo de la enfermedad y/o en el manejo de escalas. El proceso de traducción se llevó a cabo enfatizando en el sentido conceptual de cada uno de los ítems. Después de la traducción se compararon las dos versiones en relación con el significado de los ítems17,18. La versión aprobada (fig. 1) por el grupo investigador consta de los tres enunciados relacionados con dolor, fatiga y sequedad en las últimas dos semanas, cada uno con una puntuación posible entre 0 y 10.
El ESSPRI y el PROFAD se aplicaron a cada paciente a manera de autorreporte, en compañía de un médico investigador.
Se tomaron datos demográficos, clínicos y de laboratorio a partir de la historia clínica de la consulta. Se tuvieron en cuenta comorbilidades que implicaran compromiso sistémico y/o con posibilidad de causar dolor o fatigabilidad. Se calculó el ESSDAI para cada paciente con la información allí registrada.
El tamaño de la muestra se definió a partir del criterio recomendado en la literatura17,18: 5 individuos por cada ítem del instrumento a evaluar, es decir, 15 sujetos como mínimo en total para el estudio; sin embargo, nuestra muestra fue de 42 pacientes.
Análisis estadísticoSe elaboró una base de datos con control de ingreso a través de reglas de validación de los valores introducidos en el formulario para garantizar la confiabilidad de los datos (programa Excel); posteriormente se llevó al programa Stata versión 14.0 (StataCorp, College Station, Texas, EE.UU.), en el que finalmente se realizó el análisis de la información.
Se efectuó un análisis exploratorio de los datos, se evaluó la normalidad de su distribución, se identificaron valores extremos que pudieran incidir en el resultado, al igual que valores perdidos. Posteriormente se llevó a cabo un análisis descriptivo de la población sujeto de estudio de acuerdo con las variables previamente definidas, y se calcularon medias o medianas según la distribución encontrada.
Para establecer la consistencia interna se calculó el coeficiente de alfa de Cronbach para los ítems de la escala. Para evaluar la validez del constructo se calculó el coeficiente de correlación de Spearman para el ESSPRI con el PROFAD y para el ESSPRI con el ESSDAI.
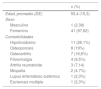
ResultadosSe incluyeron 42 pacientes con diagnóstico de SS. La edad promedio fue de 55,4años (±15,3), con una mediana de duración de la enfermedad de 36 (RIC 5,5-84) meses; 41 (97,62%) pacientes fueron mujeres. Se encontraron diferentes comorbilidades, siendo el hipotiroidismo la más frecuente (n=11, 26,19%), seguido de la osteoporosis (n=8, 19%) y la osteoartrosis (n=7, 16,6%), entre otras; 18 (42,8%) pacientes presentaron solo una comorbilidad, 6 presentaron dos (14,2%) y uno presentó tres (2,3%) (tabla 1).
Características demográficas
| n (%) | |
|---|---|
| Edad, promedio (DE) | 55,4 (15,3) |
| Sexo | |
| Masculino | 1 (2,38) |
| Femenino | 41 (97,62) |
| Comorbilidades | |
| Hipotiroidismo | 11 (26,1%) |
| Osteoporosis | 8 (19%) |
| Osteoartritis | 7 (16,6%) |
| Fibromialgia | 4 (9,5%) |
| Artritis reumatoide | 3 (7,14) |
| Miopatía | 2 (4,7%) |
| Lupus eritematoso sistémico | 1 (2,3%) |
| Esclerosis múltiple | 1 (2,3%) |
El resultado del ESSPRI para todos los pacientes fue en promedio de 5,8 (±4,6) y para el PROFAD de 2,8 (±1,7). Por otro lado, para el ESSDAI se encontró que 30 pacientes (71,43%) tenían actividad baja de la enfermedad (mediana 0, RIC 0-0,75), 4 pacientes (9,52%) tenían actividad moderada (mediana 8,5, RIC 6,5-9) y 8 pacientes (19,05%) tenían actividad severa (promedio 33,1±15,30).
El coeficiente de confiabilidad estandarizado (alfa de Cronbach) del ESSPRI fue de 0,8034 y el alfa de Cronbach del PROFAD fue de 0,9623. La correlación entre las escalas ESSPRI y PROFAD fue de 0,5800 (p=0,0001), mientras que entre el ESSPRI y el ESSDAI fue de −0,0848 (p=0,593) (tabla 2).
Correlación entre escalas
| Correlacióna | p | |
|---|---|---|
| ESSPRI - PROFAD | 0,5800 | 0,0001 |
| ESSPRI - ESSDAI | −0,0848 | 0,593 |
El ESSPRI fue validado en su idioma original en el año 2015 para evaluar los síntomas percibidos por pacientes con diagnóstico de SS11,13. Al ser un índice basado en tres preguntas sencillas, es una herramienta útil y fácil de aplicar, por lo que se prefiere por encima de otras como el PROFAD o el SSI, con las que se ha reportado adecuada correlación13, y desde entonces se ha utilizado en diversos estudios clínicos19-21.
En este estudio se aplicó la escala ESSPRI con sus tres dominios traducidos al castellano en 42 pacientes con diagnóstico de SS. Comparado con estudios que incluyen únicamente pacientes con SS primario, nuestra cohorte contextualiza sobre escenarios que pueden presentarse fácilmente en una consulta reumatológica, como es la poliautoinmunidad, e incluso sobre asociaciones poco frecuentes, como nuestro caso de esclerosis múltiple y SS. Aparte de esta, se encontró que varios pacientes presentaban una o más comorbilidades; entre ellas, fibromialgia, artritis reumatoide e hipotiroidismo, patologías que pueden generar dolor y/o fatigabilidad independientemente del SS. Por lo tanto, diferenciar el causante directo de dichos síntomas puede ser difícil y deben ser tomados en cuenta al momento de interpretar este cuestionario, sin limitar su aplicación. Relacionado con esto, varios estudios han reportado una correlación entre trastornos de ansiedad y depresión en pacientes con SS primario, no solo con mayor actividad de la enfermedad, sino también con mayores puntajes del ESSPRI19,22.
La consistencia interna de la prueba fue alta, basada en el coeficiente de confiabilidad para el ESSPRI de 0,8034, comparado con 0,447 de adaptaciones a otros idiomas15. La correlación con el PROFAD fue de 0,58, similar a la obtenida en la validación realizada por el EULAR, de 0,6811. Contrario a esto, mientras en la validación inicial de la escala se encontró una correlación baja con el ESSDAI11, en nuestro caso no hubo correlación, dado el r: −0,0848, con un valor de p no significativo.
Dado que el ESSDAI es la herramienta de elección para discriminar entre enfermedad activa e inactiva por el clínico y el ESSPRI para evaluar la percepción de los síntomas por el paciente, tras demostrar que la correlación entre las dos es baja, se ha planteado que el ESSPRI sea complementario al ESSDAI11,23.
En efecto, la concordancia entre ambas escalas es variable según el contexto en que se aplique. Estudios que miden el comportamiento de las escalas antes y después de administrar un tratamiento en pacientes con SS han mostrado que los puntajes son concordantes al disminuir y, por ende, que hay adecuada sensibilidad de estas escalas para cambiar tras una intervención24,25. En la serie de Olsson et al.26 el ESSPRI resultó asociado a mayor consumo acumulado de tabaco, mientras que el ESSDAI no mostró ninguna relación; aun así, al medirlos según el estado de tabaquismo de los pacientes, las dos se comportaron de forma similar. En nuestra cohorte pudimos ver que varios pacientes tuvieron puntajes bajos en el ESSDAI y puntajes altos en el ESSPRI, lo cual habla de una discrepancia entre el punto de vista del clínico y del paciente sobre la enfermedad en un determinado momento, comparable con otros reportes en que se han encontrado discordancias entre las dos escalas21.
Adicionalmente, aunque la aplicación del ESSPRI va dirigida a la evaluación subjetiva de los síntomas, varios estudios han descrito una correlación con variables biológicas como niveles séricos de beta-2-microglobulina y velocidad de eritrosedimentación20,27.
A pesar de que el ESSPRI se ha incorporado como marcador de desenlaces y demás en estudios de investigación, poco se encuentra en la literatura sobre el uso dado por reumatólogos en la práctica clínica diaria. El objetivo del manejo en el SS es mantener la enfermedad controlada con el mínimo de actividad y garantizar calidad de vida al paciente; por esto, idealmente se debe aplicar de forma conjunta con el ESSDAI para tener un reflejo más acertado de todos los espectros de la enfermedad, y más aún por ser las escalas clinimétricas actualmente catalogadas como las más prácticas y confiables en el SS28.
Si bien esta adaptación al castellano se llevó a cabo con pacientes colombianos y su aplicación en otros países de habla hispana requiere una evaluación cuidadosa, se espera que sea de gran utilidad para su implementación, seguimiento y toma de decisiones en estos países.
Limitaciones del estudioNo se realizó una prueba de reproducibilidad intraobservador, a diferencia de otros estudios que evalúan escalas clinimétricas. No se hizo una valoración estricta de las posibles dificultades de los pacientes al aplicarse y/o diligenciarse las pruebas, lo cual debe ser tenido en cuenta en su implementación.
FinanciaciónNo se recibió ningún apoyo financiero para el desarrollo de este estudio.
Conflicto de interesesLos autores declaran no tener conflicto de intereses.