El virus SARS-CoV-2 es un nuevo virus RNA causante de la enfermedad COVID-19, declarada como pandemia por la Organización Mundial de la Salud (OMS). Produce un cuadro de neumonía atípica que puede desembocar en un fallo multiorgánico. La desregulación del sistema inmune secundaria a la infección produce un cuadro similar al síndrome de linfohistiocitosis hemofagocítica (SLHH). Varios estudios han definido la importancia que los inhibidores de la IL-6 (tocilizumab) tienen en el tratamiento de la infección por SARS-CoV-2, sin embargo, la indicación de tratamiento con inhibidores de IL-1 (anakinra) no se encuentra establecida de forma clara.
Presentamos el caso de un paciente de 51 años con neumonía bilateral secundaria a infección por SARS-CoV-2 refractaria al tratamiento antiviral y anti-IL-6 que presentó mejoría clínica y analítica tras el tratamiento con anti-IL-1 (anakinra).
SARS-CoV-2 is a new RNA virus which causes coronavirus disease 2019 (COVID-19), declared a pandemic by the World Health Organization (WHO). It triggers an atypical pneumonia that can progress to multiorgan failure. COVID-19 can cause dysregulation of the immune system, triggering an inflammatory response, and simulate haemophagocytic lymphohistiocytosis. Several studies have proposed that anti-IL-6 receptor antibodies, such as tocilizumab, play an important role in the treatment of severe acute respiratory infection associated with SARS-CoV-2. However, the role of anti-IL-1 receptor antibodies, such as anakinra, in the treatment of COVID-19 has not been established.
We present a case report of a 51-year-old man diagnosed with severe respiratory infection associated with SARS-CoV-2 that was refractory to antiviral and anti-IL-6 treatment, with a favourable clinical outcome and analytical improvement after treatment with anti-IL-1 (anakinra).
El virus SARS-CoV-2 es un nuevo virus RNA que fue identificado por primera vez en diciembre de 2019 en la ciudad de Wuhan, China1. SARS-CoV-2 produce un cuadro de neumonía atípica que puede desembocar en un fallo multiorgánico2. La desregulación del sistema inmune secundaria a la infección produce un cuadro similar al síndrome de linfohistiocitosis hemofagocítica (SLHH)3. Las diferentes vías de activación inmune culminan en una disfunción citotóxica cuyo principal desencadenante es una «tormenta de citocinas». Varios estudios han definido la importancia que los inhibidores de la IL-6 (tocilizumab) tienen en el tratamiento de la infección por SARS-CoV-24. Sin embargo, la indicación de tratamiento con inhibidores de IL-1 (anakinra) no se encuentra establecida de forma clara.
Presentamos el caso de un paciente de 51 años con neumonía bilateral secundaria a infección por SARS-CoV-2 refractaria al tratamiento con tocilizumab que presentó mejoría tras el tratamiento con anakinra.
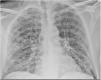
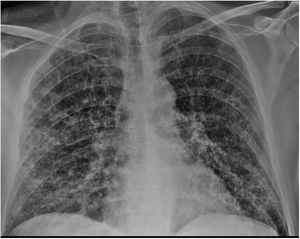
Caso clínicoVarón de 51 años que acudió a urgencias por cuadro de fiebre (>38°C) y disnea de una semana de evolución. El paciente presentaba antecedentes de EPOC, cirrosis hepática de origen no filiado y adenocarcinoma de recto (pT4N1M0). En el examen físico destacaba la presencia de hipoventilación generalizada con crepitantes finos bibasales. En la radiografía de tórax (fig. 1) se objetivaron infiltrados bilaterales con patrón en vidrio deslustrado. La analítica de sangre mostraba los valores descritos en la tabla 1. Los cultivos de sangre y orina fueron negativos. Se realizó detección de virus SARS-CoV-2 por reacción en cadena de polimerasa en exudado faríngeo, que fue positiva.
Valores analíticos del paciente durante el ingreso hospitalario
| Valores analíticos | Valores al ingreso | Valores al inicio de anakinra | Tras 48h de inicio de anakinra | Valores al alta | Rango de valores |
|---|---|---|---|---|---|
| Leucocitos (/μL) | 9,81 | 4,42 | 8,11 | 6,81 | (4,50-10,80) |
| Linfocitos (/μL) | 0,71 | 0,87 | 5,60 | 1,28 | (1,20-6,50) |
| Fibrinógeno (mg/dL) | 720 | - | 436 | 248 | (130-400) |
| Dímero-D (μg/mL) | 0,8 | 1,9 | 1,3 | 1,1 | (0,0-0,5) |
| Ferritina (ng/mL) | 477 | 406 | 322 | 502 | (30-400) |
| Proteína C reactiva (mg/dL) | 19,68 | 10,01 | 1,60 | ≤0,1 | (0,00-0,50) |
| Procalcitonina (ng/mL) | 0,42 | 0,23 | - | - | (0,00-0,50) |
| IL-6 (pg/mL) | - | >1.000 | - | - | (0,00-3,40) |
-: no disponible.
Ante el diagnóstico de neumonía bilateral secundaria a infección por SARS-CoV-2 se procedió al ingreso hospitalario del paciente y se inició tratamiento con antibioterapia de amplio espectro (ceftriaxona, azitromicina y posteriormente escalada a piperacilina-tazobactam), hidroxicloroquina (HCQ) y lopinavir/ritonavir (LPV/r). Ante la necesidad de soporte respiratorio se inició tratamiento con tocilizumab (8mg/kg cada 12h, 2 dosis subcutáneas). Dada la ausencia de mejoría respiratoria y analítica (tabla 1) transcurridas 48h de la administración de tocilizumab, se decidió la administración de anakinra (100mg dosis total única, subcutánea). Posteriormente el paciente experimentó buena evolución clínica, pudiendo retirar el soporte ventilatorio y recibiendo el alta hospitalaria a los 14 días del ingreso.
DiscusiónLa «tormenta de citocinas» secundaria a la infección por SARS-CoV-2 condiciona cuadros graves de enfermedad COVID-19. La activación desmesurada del sistema inmune produce un cuadro similar al SLHH3. El uso de anticuerpos anti-IL-6 en el tratamiento de la infección por SARS-CoV-2 se encuentra actualmente en estudio, siendo uno de los pilares actuales del tratamiento de la enfermedad COVID-19. En el estudio de Le et al.5, tocilizumab demostró respuesta clínica tras una o dos dosis de fármaco en el 69% de los pacientes con síndrome de activación de citocinas. El uso de moléculas inhibidoras de otras interleucinas se encuentra actualmente en estudio, siendo anakinra la molécula antiinterleucina más estudiada actualmente tras el tocilizumab en el tratamiento de COVID-196.
En el caso de nuestro paciente, el tratamiento con tocilizumab no aportó mejoría clínica o analítica, mientras que el uso de anakinra permitió obtener una clara mejoría en 48h. Aunque no se puede descartar un posible beneficio debido al efecto tardío del tocilizumab. Si bien la dosis de anakinra administrada a nuestro paciente fue única, existen estudios como el de Monteagudo et al., que muestran la eficacia de este fármaco en infusión continua a dosis mayores de 2.400mg/día para el tratamiento del síndrome de activación macrofágica (SAM)7.
En conclusión, el bloqueo de la IL-1 de forma específica podría ser una alternativa eficaz en el manejo de pacientes con infección por SARS-CoV-2 que no se hayan beneficiado de otros tratamientos.
Conflicto de interesesLF-P: Ninguno que declarar.
AO-H: Ninguno que declarar.
RAE-C: Ninguno que declarar.
ET-B: Ninguno que declarar.
AL-G: Ninguno que declarar.
JJC-H: Consulting or Advisory Role: MSD Oncology, Bristol-Myers Squibb, Merck Speakers’ Bureau: MSD Oncology, Bristol-Myers Squibb, Merck, Roche, Janssen Oncology, AstraZeneca Travel, Accommodations, Expenses: MSD Oncology.