Las prevalencia de las alteraciones nutricionales en pacientes con enfermedades reumatológicas varía entre un 4 y un 95%, dependiendo del método empleado para su detección. Inicialmente agrupadas bajo el término de caquexia reumatológica, en la actualidad es posible ampliar el concepto de desnutrición conforme los mecanismos fisiopatológicos que participan, sea desnutrición asociada a procesos inflamatorios crónicos (caquexia), desnutrición asociada a procesos inflamatorios agudos (desnutrición proteico-calórica) y desnutrición asociada a baja ingesta alimentaria. El espectro clínico de la desnutrición asociada a enfermedades reumatológicas varía desde el paciente con bajo peso hasta el paciente con sobrepeso u obesidad, con disminución en la cantidad de masa magra, repercusión funcional, en calidad de vida y pronóstico, como común denominador. Adicionalmente, el incremento asociado en masa grasa aumenta el riesgo para el desarrollo de enfermedad cardiovascular. El manejo integral de las enfermedades reumatológicas debe de incluir aspectos para la prevención, la identificación y el manejo oportunos de las alteraciones nutricionales.
The prevalence of nutritional alterations in rheumatologic diseases ranges from 4 to 95%, depending on the detection method used. Formerly described as the single term rheumatoid cachexia, nutritional alterations can currently be grouped and subdivided based on the physiopathological mechanisms involved: chronic disease-related inflammatory conditions (cachexia), malnutrition associated to acute malnutrition inflammatory conditions (protein-caloric malnutrition) and starvation-related malnutrition. Clinical manifestations of malnutrition associated to rheumatic diseases vary from the patient with low weight or overweight and obesity; with lean body mass depletion as well as functional repercussions, and impact of quality of life as a common denominator. Additionally, the associated increase in body fat mass increases the risk for cardiovascular morbidity. A multidisciplinary approach towards rheumatic diseases should include aspects oriented towards prevention, early identification, diagnosis and correction of nutritional alterations.
El impacto nutricional de las enfermedades reumatológicas fue reconocido desde 1873 por sir James Paget bajo el término de caquexia reumatológica1,2, se asoció a padecimientos con sustrato inflamatorio1 y comprendía los efectos que las alteraciones nutricionales tienen sobre la función sensitiva y motora, y que se manifiestan como la combinación de debilidad, atrofia muscular y su repercusión en pérdida de la funcionalidad1,3.
A pesar de que algunos autores plantean que las alteraciones en la condición nutricional de los pacientes con enfermedades reumatológicas se constituyen como marcadores de gravedad de la enfermedad3, en la actualidad aún resultan aspectos poco atendidos.
Relevancia del problemaEn las últimas décadas, el concepto de caquexia reumatológica ha recobrado vigencia2 a partir del entendimiento de los efectos que las alteraciones nutricionales ejercen sobre la calidad de vida de los pacientes, la evolución y el pronóstico de los padecimientos reumatológicos3, de los avances en el conocimiento de los mecanismos fisiopatológicos que median el impacto nutricional de las enfermedades de tipo inflamatorio (sean de evolución aguda y/o crónica)4,5 y de la mayor precisión de las herramientas disponibles para la evaluación de la composición corporal. Lo anterior ha permitido identificar de una manera más apropiada los efectos que los padecimientos inflamatorios tienen sobre la masa magra, la masa grasa y el gasto energético6.
Desde el punto de vista fisiopatológico, la importancia de prevenir la pérdida de masa magra deriva de que está conformada en su mayor proporción por lo que se denomina masa celular corporal (body cell mass, por su acepción más difundida en inglés) y que representa el sitio de la economía corporal en donde ocurre el 95% de la actividad metabólica del organismo2,6-8.
La masa magra se constituye por músculo, tejido funcional de los órganos, el sistema inmunitario y el sistema óseo con sus implicaciones funcionales en términos estructurales, metabólicas, inmunológicas, motoras o de sostén2,6-8, por lo que cualquier alteración a nivel de la masa magra se traducirá en la pérdida o limitación de funciones corporales y potencial morbimortalidad6,8,9.
Se reconoce que pacientes reumatológicos que presentan alteraciones en su condición nutricional tienen expectativas de vida hasta 18 años menores en comparación con pacientes con enfermedades reumatológicas sin desnutrición y de 3 a 5 veces mayor riesgo de morbilidad en relación con la población general3, con causas de mortalidad asociadas a desnutrición (procesos infecciosos, enfermedades cardiovasculares y pulmonares) por encima incluso de la propia morbilidad asociada las enfermedades reumatológicas3,6.
El concepto de desnutrición en los pacientes con padecimientos inflamatorios de curso crónico comprende el espectro clínico desde pacientes con bajo peso y disminución de masa magra, hasta aquellos pacientes que por índice de masa corporal (IMC) se encuentran en rangos de sobrepeso y obesidad pero que cursan con disminución de masa magra asociada al proceso inflamatorio de curso crónico4,5,8. A su vez, el incremento en masa grasa representa un factor de riesgo para el desarrollo de síndrome metabólico y enfermedades cardiovasculares, entidades ampliamente prevalentes en los pacientes con enfermedades reumatológicas2-10.
PrevalenciaLa incidencia de caquexia reumatológica es variable, dependiendo directamente de la sensibilidad y la especificidad de los instrumentos empleados para su detección11,12. La prevalencia de alteraciones nutricionales oscila desde un 4% hasta valores del 26 al 52%, particularmente en poblaciones con artritis reumatoide11,13.
En un estudio publicado por Bravo-Ramírez et al.14 hasta un 37,5% de la población mexicana con lupus eritematoso sistémico (LES) presentaron disminución de masa magra cuando fueron evaluados mediante análisis vectorial de bioimpedancia eléctrica, a pesar de que la mitad de la muestra tenía índices de masa corporal en rangos de sobrepeso u obesidad.
En otro estudio, también en pacientes mexicanos con diagnóstico de artritis reumatoide (AR)13, el 48% de los pacientes presentaron disminución de masa magra aun y cuando el 94% de los mismos tenían incremento en el porcentaje de grasa corporal. De ahí que resulta evidente que la prevalencia de desnutrición, conforme el criterio de disminución de masa magra, frecuentemente es subestimada.
La prevalencia de desnutrición también varía de acuerdo con el género de la población estudiada en el caso de mujeres con AR puede alcanzar hasta un 52% y para varones un 30%11.
PresentaciónEn los pacientes con desnutrición, la disminución de masa magra subyacente no siempre resulta fácilmente evidente, ya que si existe preservación o incremento en la cantidad de masa grasa el peso corporal no se modifica2,3,11,12, manteniendo el IMC en intervalos de normalidad, sobrepeso u obesidad, por lo que erróneamente se les consideraría como no desnutridos2,11-14.
En una población de mujeres mexicanas con diagnóstico de LES, evaluados mediante IMC, el 20,5% y el 29,2% se encontraron en intervalos de sobrepeso y obesidad, respectivamente; sin embargo, cuando se utilizó una herramienta de evaluación de mayor sensibilidad para la estimación de masa magra, como lo es el análisis vectorial de bioimpedancia eléctrica, el 37% de esta misma población presentó disminución de masa magra y cumplió el criterio de desnutrición (caquexia), condición que hubiera pasado inadvertida si solo se hubieran evaluado mediante el IMC14.
Es por ello que se establece que los pacientes con enfermedades de curso inflamatorio crónico deban de ser evaluados desde el punto de vista nutricional en forma sistemática y periódica, mediante la combinación de instrumentos y herramientas con alta sensibilidad para la detección de alteraciones en la composición corporal, aun y cuando los pacientes no manifiesten cambios en el peso corporal o estos sean apenas sutiles2,3,11,12. Dentro de los recursos disponibles para el abordaje del estado nutricional en pacientes con enfermedades reumatológicas, se encuentran las escalas de tamiz nutricional, medidas antropométricas, historia dietaria, interpretación de parámetros bioquímicos, evaluación funcional y determinación de la composición corporal, esta última mediante bioimpedancia eléctrica, densitometría, tomografía computarizada, resonancia magnética y ultrasonido muscular, entre otros6.
Para ampliar la capacidad diagnóstica de desnutrición en pacientes reumatológicos, se recomienda en la actualidad el empleo de recursos de mayor sensibilidad, en comparación con la antropometría y el IMC, que permitan una oportuna detección de las alteraciones nutricionales, particularmente a nivel de la masa magra y la función1-8, aun y cuando presenten IMC en intervalos de normalidad, sobrepeso e incluso obesidad4,6.
FisiopatologíaEn la actualidad, la desnutrición se categoriza en 3 entidades clínicas, de acuerdo con mecanismos fisiopatológicos implicados en su desarrollo, lo que permite una mayor comprensión e integración de sus aspectos clínico-fisiopatológicos y facilita la posibilidad de incidir puntualmente en su prevención, identificación, diagnóstico y manejo4,5,8.
Síndrome de caquexiaEl término caquexia, derivado de griego kachexía (significado, mal estado), también descrito como emaciación, síndrome de desgaste o síndrome consuntivo4,5, se refiere a la desnutrición asociada a procesos inflamatorios de curso crónico, en donde la presencia de inflamación, en diversos grados y amplitudes, se encuentra perennemente presente9.
En el caso de padecimientos de curso crónico, la participación de procesos inflamatorios de manera sostenida y a largo plazo implica la activación en cascada de mediadores como los son el factor de necrosis tumoral α, la interleucina-1, la interleucina-6, la proteína C reactiva, el factor transformante-β, las catecolaminas, los corticoides endógenos y la activación del factor nuclear κβ, entre otros8,15,16, los que en su conjunto ejercen efectos deletéreos sobre la composición corporal y el metabolismo energético, y que se presentan en forma de incremento en el gasto energético basal, la proteólisis muscular y en la gluconeogénesis, movilización de aminoácidos de origen muscular, resistencia a la insulina, hiperglucemia, disminución de la síntesis proteica muscular, incremento en movilización de ácidos grados libres del tejido adiposo, anemia de la enfermedad crónica, desmineralización ósea, disfunción endotelial, activación y agregación plaquetaria, dislipidemia, aterogénesis, hiperfibrinogenemia, hiperuricemia, vasoconstricción, trombogénesis y síndrome metabólico2-5.
En términos nutricionales, el efecto combinado de los mediadores inflamatorios, se traduce en anorexia, pérdida de peso no intencional (> 5% en un lapso de los últimos 6 meses), disminución de la masa muscular (valores menores al percentil 10)8 y del tejido adiposo, con disminución de la fuerza y de la movilidad, debilidad, limitación funcional, pérdida de la autonomía, fatiga, disfunción inmune, mayor susceptibilidad a procesos infecciosos, alteración en procesos de cicatrización y reparación tisular, depresión, pobre calidad de vida y disminución en la sobrevida2,3,8,10,17,18. A todas estas condiciones se pueden agregar los potenciales efectos secundarios de los medicamentos empleados en la terapéutica de las enfermedades reumatológicas (inmunosupresores y glucocorticoides) y su influencia negativa en la composición corporal19.
La disminución de masa magra asociada a caquexia no es completamente reversible con la provisión óptima de sustratos energéticos y proteicos, ya que es el resultado del efecto multisistémico de los mediadores inflamatorios y no susceptible de ser revertido en su totalidad mediante la regularización u optimización del aporte proteico-calórico y de micronutrimentos4,5,18. Se ha explorado la posibilidad de modular la amplitud de la inflamación mediante del uso selectivo de ciertos nutrimentos (ácidos grasos omega-3, β-hidroximetilbutirato, leucina), con propiedades regulatorias sobre la respuesta inflamatoria e inmunitaria, y que podrían modificar su curso hacia perfiles más favorables y menos deletéreos para el estado nutricional4,18.
Una entidad clínico-patológica que frecuentemente coexiste con la desnutrición asociada a procesos inflamatorios crónicos, y particularmente en poblaciones de edad avanzada, es la presencia de sarcopenia8, entidad asociada al proceso de envejecimiento y de causa multifactorial que se acompaña de disminución de masa magra (< 2 desviaciones estándar conforme el valor de referencia)8 y de la fuerza muscular (medida por dinamometría o velocidad de la marcha y su referente correspondiente para la población estudiada)8, incremento del tejido adiposo e infiltración grasa a nivel muscular6, con repercusión en términos de disminución de la fuerza muscular, debilidad, postración, pérdida de la autonomía y eventualmente discapacidad8.
La presencia de sarcopenia e incremento en la cantidad de masa grasa se denomina síndrome de obesidad sarcopénica6, con comportamiento metabólico y nutricional propio del paciente desnutrido, intervalos de IMC de sobrepeso y obesidad, e incremento en el riesgo de morbimortalidad cardiovascular, esta última causa de un número importante de muertes en pacientes reumatológicos, algunas de estas prematuras20-25.
La asociación del incremento en masa grasa corporal y desnutrición es prevalente. En una población mexicana de pacientes con AR, el 35% presenta obesidad central y está expuesto a morbilidad por desnutrición, enfermedades cardiovasculares y síndrome metabólico13.
Desnutrición asociada a procesos inflamatorios agudosLa característica de la desnutrición asociada a procesos inflamatorios agudos (también conocida como desnutrición proteico-calórica o kwashiorkor)4,5 es la amplificación significativa (habitualmente en intervalos suprafisiológicos) de la cascada de activación inflamatoria e inmunológica4,5,15,18, y que se traduce en una desnutrición de curso acelerado, con disminución significativa de masa magra en un reducido intervalo (transcurso de días o semanas), acompañada de incremento en la permeabilidad capilar, retención hídrica y formación de edemas4,5. Su presencia en los pacientes con enfermedades reumatológicas se deriva de los episodios de exacerbación de la enfermedad de base y/o la concurrencia de otro tipo de procesos inflamatorios agudos, por lo general de tipo infeccioso4,5,18.
Sin una evaluación instrumentada que permita conocer la cantidad de masa magra y su traducción funcional, erróneamente se pasa por alto el diagnóstico de desnutrición, ya que la presencia de edemas enmascara la pérdida ponderal en sus fases iniciales4,5,15,18.
Los efectos del curso rápidamente progresivo de la desnutrición secundaria a procesos inflamatorios agudos se agregan a los preexistentes y secundarios a la evolución crónica de las enfermedades reumatológicas, lo que potencia la disfunción inmunitaria y muscular, la debilidad, el dismetabolismo, las alteraciones en la calidad de vida, el pronóstico y la discapacidad a largo plazo, ya que, aunque el evento inflamatorio agudo se resuelva, las limitaciones impuestas por el deterioro agudo en su condición nutricional no siempre revierten en un corto plazo2,3.
De manera similar a los procesos inflamatorios de curso crónico, las intervenciones nutricionales en presencia de procesos de tipo agudo no revierten toda la cascada inflamatoria subyacente ni sus efectos sobre la condición nutricional, sino que solo contribuyen evitar que la condición nutricional del paciente presente un mayor deterioro2,18. Las alteraciones nutricionales asociadas a procesos inflamatorios de curso agudo y crónico solo serán reversibles una vez lograda la remisión del proceso fisiopatológico, condición que no siempre es posible en la gran mayoría de las enfermedades reumatológicas y en donde, aun con la remisión total del proceso inflamatorio subyacente, las alteraciones metabólicas y en la composición corporal persisten en el tiempo26.
Desnutrición asociada a baja ingesta o inadecuación nutricionalDescrita con el término de marasmo, la desnutrición asociada a baja ingesta o inadecuación nutricional es una entidad frecuente, particularmente en poblaciones de adultos ancianos o con discapacidad. Su fisiopatología radica en la inadecuación o el desbalance entre la demanda energética y los aportes de nutrientes4,5. Cuando se conjuntan desnutrición asociada a procesos inflamatorios agudos y crónicos y desnutrición asociada a baja ingesta calórica-proteica, su impacto en la funcionalidad se torna aditivo4,5,8,26,27.
La disminución en el aporte de sustratos energéticos conlleva a la implementación de mecanismos adaptativos con fines de preservar, temporalmente, las funciones corporales vitales. Cuando esta capacidad adaptativa se ve superada, se establece la entidad fisiopatológica de desnutrición asociada a baja ingesta, con sus consecuentes efectos sobre la función4,5. Su coparticipación en el escenario de procesos inflamatorios de curso crónico no es rara y su presencia generalmente obedece a una etiología multifactorial4,5.
La importancia de la identificación temprana y oportuna de la desnutrición asociada a baja ingesta dietaria radica en que es frecuente que los pacientes con enfermedades reumatológicas mantengan patrones inadecuado de consumo dietario que impiden cubrir los requerimientos nutricional de base, los que derivan de los procesos fisiopatológicos de las enfermedades reumatológicas y de los efectos de los medicamentos empleados13, además de que este tipo de desnutrición es reversible mediante la óptima provisión de sustratos nutricionales4,5.
Las etiología de la desnutrición asociada a baja ingesta dietaria en los pacientes con enfermedades reumatológicas obedece a múltiples factores, como lo son el impacto negativo del padecimiento en la calidad de vida, independencia, autonomía, suficiencia, funcionalidad, factores sociales y económicos adversos, la presencia de depresión, curso clínico con agudizaciones y remisiones, hospitalizaciones frecuentes, efectos secundarios de medicamentos, y los efectos anorexigénicos de los diversos mediadores inflamatorios que participan en las enfermedades reumatológicas (particularmente el factor de necrosis tumoral α)13. Por ello, como parte integral del manejo del paciente con enfermedades reumatológicas, la historia de consumo dietético representa un elemento de importante valor predictivo para la prevención, identificación, detección oportuna y pronta corrección de las alteraciones nutricionales asociadas a esta categoría28.
La prevalencia de inadecuación nutricional en pacientes con enfermedades reumatológicas es alta; en un estudio realizado por Puente-Torres et al., en una población mexicana de pacientes con AR, se demostró que el 90% de los pacientes estudiados presentaban inconsistencias para cubrir los criterios de una dieta completa, equilibrada, suficiente y variada13.
Manejo nutricional de los pacientes con enfermedades reumatológicasEl enfoque conceptual de la desnutrición sobre la base de los procesos fisiopatológicos que la condicionan, y no solo del grado de correspondencia con puntos de corte establecidos para medidas antropométricas o cantidad de masa magra y masa grasa, se considera en la actualidad como una propuesta innovadora para la comprensión, la prevención y el abordaje de la desnutrición4,5,18,29-31, ya que a partir de dicho razonamiento es posible implementar estrategias específicas para su manejo, cuyos como objetivos principales son:
- –
Incorporación del abordaje nutricional como parte integral e interdisciplinario del manejo médico de los pacientes con enfermedades reumatológicas6,13.
- –
Incorporación de metodologías de evaluación de la composición corporal que permitan una mayor definición del efecto que las enfermedades reumatológicas ejercen en los diferentes compartimentos corporales (masa magra y masa grasa) y, de esta forma, ampliar la comprensión, el conocimiento, la prevención y el manejo de las alteraciones nutricionales, para con ello reducir su impacto en el curso-pronóstico de la enfermedad, la calidad de vida y la funcionalidad6.
- –
Preservación de la composición corporal, particularmente mediante la conservación de masa magra y la consecuente funcionalidad que de esta deriva2,9,10,13,26.
- –
Prevención del incremento en masa grasa y de su traducción en sobrepeso, obesidad y síndrome metabólico, y su participación como factor de riesgo para el desarrollo de enfermedades cardiovasculares13,20-25.
- –
Disminución de la incidencia y la prevalencia de alteraciones nutricionales asociadas al sustrato fisiopatológico propio de las enfermedades reumatológicas, mediante un óptimo control de la enfermedad de base; prevención, identificación y manejo oportuno de los procesos agudos intercurrentes, así como minimizar al máximo posible los potenciales efectos secundarios que la terapéutica empleada tiene sobre la condición nutricional2,18.
- –
Preservación de la funcionalidad, la independencia, la autonomía, la suficiencia y la calidad de vida, con mejoría en el curso pronóstico y sobrevida6,9,10,26.
- –
El empleo potencial de farmaconutrición para modular selectivamente la respuesta inflamatoria subyacente a las enfermedades reumatológicas y de esta forma incidir en su curso pronóstico, aun y cuando en la actualidad esta modalidad de manejo todavía resulta debatible28,32.
Para ello, las intervenciones nutricionales propuestas son:
- –
Tamiz y evaluación nutricional a los pacientes con enfermedades reumatológicas para la prevención, la identificación, el diagnóstico y el abordaje oportuno de las alteraciones nutricionales que acompañan a los padecimientos reumatológicos33.
- –
Prescripción, vigilancia y seguimiento dietario para mantener la adecuación de macro y micronutrientes que permita cubrir el requerimiento nutricional de base más los derivados del curso crónico de la enfermedad, de los procesos agudos intercurrentes y de los que se asocian a los potenciales efectos secundarios de los fármacos empleados para el manejo de las enfermedades reumatológicas13,33.
- –
Incorporación de programas de rehabilitación que permitan preservar la densidad mineral ósea, la masa y la fuerza muscular, con su consecuente traducción en mantener la funcionalidad, la independencia, la autonomía, la prevención de discapacidad y la mejoría en calidad de vida de los pacientes con enfermedades reumatológicas34-38.
- –
Modulación selectiva de procesos inflamatorios que permita atenuar la respuesta metabólica que acompaña a las enfermedades reumatológicas y sus efectos en el estado nutricional y la composición corporal39-43.
Paciente femenino de 47 años de edad, diabética tipo 2, hipertensa, con hipercolesterolemia e hipertrigliceridemia. Diagnóstico de AR desde hace 6 años. Actualmente, con evidencia de actividad inflamatoria articular con flogosis a nivel de codos y rodillas. Ingresa en el hospital con diagnóstico de neumonía adquirida en la comunidad.
Manejo farmacológico para las enfermedades de base en forma irregular sobre la base de metformina, enalapril, prednisona, metotrexato y cloroquina. Peso habitual 78,5kg. Peso actual 65,5kg. Descenso ponderal de 13 kg en los últimos 12 meses. IMC 26,2kg/m2, sobrepeso. Con presencia de edema a nivel bimaleolar.
Evaluación de su ingesta dietaria con alto consumo de hidratos de carbono complejos, baja ingesta proteica.
Antropometría: circunferencia media de brazo 26,8cm (menor a percentil 1044). Perímetro abdominal 97cm (aumentado conforme el punto de referencia para población hispana45).
Composición corporal por análisis de bioimpedancia por vectores, índice de masa magra disminuido (percentil 1046), índice de masa grasa aumentado (percentil 9546).
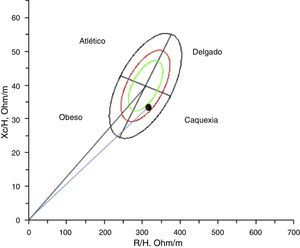
Comportamiento de composición corporal de acuerdo con el comportamiento de la masa magra mediante análisis vectorial de bioimpedancia eléctrica, paciente caquéctica47 (fig. 1), se integra adicionalmente la presencia de obesidad sarcopénica (incremento en masa grasa y disminución de masa magra)6,48.
Evaluación funcional con fuerza muscular por dinamometría de 14kg (percentil 1049).
Consideraciones nutricionales:
- 1.
Paciente con morbilidades condicionantes de desnutrición, estado inflamatorio crónico, empleo de glucocorticoides, síndrome metabólico y proceso inflamatorio infeccioso agudo.
- 2.
A pesar de presentar IMC en el intervalo de sobrepeso, la paciente se encuentra desnutrida, ya que cursa con pérdida del 16,5% de su peso habitual en transcurso de últimos 12 meses.
- 3.
Existe disminución de masa magra (circunferencia media de brazo en percentil 1044 e índice de masa libre de grasa en percentil 1046).
- 4.
Conforme el comportamiento de composición corporal por análisis de bioimpedancia por vectores, la paciente se encuentra en categoría de paciente caquéctica (disminución de masa magra y sobrehidratación)47.
- 5.
Traducción funcional de la disminución de masa magra, con disminución de fuerza prensil (dinapenia, por su acepción en inglés)49.
- 6.
Aunado a la disminución de masa magra, existe incremento de masa grasa (índice de masa grasa en percentil 9546), con lo que adicionalmente se integra la entidad de obesidad sarcopénica6,48.
- 7.
Existe compartamentalización de masa grasa a nivel abdominal con perímetro abdominal mayor al punto de corte para género y grupo poblacional45.
- 8.
Etiología de la desnutrición, multifactorial2,8,9:
- –
Desnutrición asociada a proceso inflamatorio crónico (caquexia reumatológica): AR y síndrome metabólico, no se descarta efecto aditivo de fármacos empleados (glucocorticoides).
- –
Desnutrición asociada a procesos inflamatorios agudos, exacerbación de la enfermedad de base, con actividad inflamatoria a nivel articular y proceso inflamatorio infeccioso pulmonar.
- –
Desnutrición asociada a baja ingesta proteica e incremento en consumo calórico a partir de hidratos de carbono.
- 9.
Paciente con morbilidad asociada a desnutrición y, a su vez, con incremento en riesgo cardiovascular derivado de la presencia de incremento en grasa corporal, particularmente con localización a nivel abdominal, y síndrome metabólico45.
- 10.
Estrategia de manejo médico-nutricio propuesta:
- –
Resolución de proceso inflamatorio infeccioso agudo.
- –
Manejo farmacológico óptimo de la enfermedad reumatológica de base, control metabólico (diabetes mellitus y dislipidemia) e hipertensivo.
- –
Prescripción dietaria para adecuación nutricia.
- –
En resumen, las alteraciones nutricionales son prevalentes en los pacientes con enfermedades reumatológicas.
Su diagnóstico dependerá de las herramientas de evaluación nutricional empleadas; se sugiere la preferencia de instrumentos que permitan la evaluación objetiva de la composición corporal, particularmente aquellas mediante las que resulte posible estimar o medir la cantidad de masa magra.
La etiología de las alteraciones nutricionales en las enfermedades reumatológicas es multifactorial, pudiendo encontrarse una combinación en grado variable de desnutrición asociada a procesos inflamatorios crónicos (caquexia reumatológica), desnutrición asociada procesos inflamatorios y desnutrición asociada a inadecuación nutricional.
La presencia de desnutrición en pacientes con enfermedades reumatológicas impacta en términos de pronóstico, calidad de vida, autonomía, independencia e incluso mortalidad.
Es frecuente la coexistencia de desnutrición con disminución de masa magra a la vez que aumento en la masa grasa (obesidad sarcopénica), lo que a su vez incrementa el riesgo de morbilidad cardiovascular.
Se requieren estrategias interdisciplinarias para la prevención, la identificación, el diagnóstico y el manejo oportuno de las alteraciones nutricionales asociadas a enfermedades reumatológicas.
El abordaje nutricional debe de formar parte del manejo integral de los pacientes con enfermedades reumatológicas.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciaciónNinguna.
Conflicto de interesesNo declarado.