El síndrome anserino es una causa frecuente de dolor de rodilla. La infiltración con glucocorticoides ha sido evaluada en estudios con bajo nivel de evidencia y no se han publicado ensayos clínicos para determinar su utilidad. El objetivo del estudio es determinar la eficacia y la seguridad de la infiltración de metilprednisolona para el tratamiento del síndrome anserino.
MétodosEfectuamos un ensayo clínico en 58 pacientes adultos con síndrome anserino, a los que se les descartó patología intraarticular que reflejara dolor en la cara medial de la rodilla. Se evaluó la escala WOMAC basal y se aleatorizaron a recibir una infiltración de xilocaína más 40mg de acetato de metilprednisolona (grupo 1) versus xilocaína más agua destilada (grupo 2). Ambos grupos recibieron 100mg de diclofenaco sódico durante 10 días. Se realizó la escala WOMAC a las 4 semanas y el registro de eventos adversos.
ResultadosSe demostró equivalencia en ambos grupos para las variables demográficas y en la evaluación clínica inicial. No hubo diferencias estadísticas en los tres dominios de evaluación de la escala WOMAC basal. La mediana del WOMAC basal en el grupo 1 fue de 32 y en el grupo 2 de 25,5 puntos. A las 4 semanas fue de 8 y 6,5 puntos, que correspondió a una mejoría del 61,6 y 62,8%, respectivamente.
ConclusiónLa infiltración con metilprednisolona en el síndrome anserino no es superior al placebo en pacientes que toman diclofenaco medidos por la escala WOMAC a las 4 semanas. La incidencia de eventos adversos tampoco difirió.
The anserine syndrome is a common cause of knee pain. Infiltration with glucocorticoids has been evaluated in studies with low level of evidence and there are no published clinical trials to determine its usefulness. The objective of this study was to determine the efficacy and safety of the infiltration of methylprednisolone in the treatment of Anserin Syndrome.
MethodsWe conducted a clinical trial in 58 adult patients with anserin syndrome, which presented intra-articular pathology ruled that reflected pain in the medial aspect of the knee. The WOMAC scale was assessed at baseline and patients were randomized to receive an infiltration of lidocaine plus 40mg methylprednisolone acetate (group 1) versus xylocaine plus distilled water (group 2). Both groups received 100mg of diclofenac sodium for 10 days. The WOMAC scale was applied at 4 weeks and adverse events were recorded.
ResultsEquivalence was demonstrated in both groups for demographic variables and initial clinical evaluation. There was no statistical difference in the three domains of assessment of the baseline WOMAC score. The median baseline WOMAC in group 1 was 32 and in group 2 was 25.5 points. At 4 weeks it was 8 and 6.5 points, which corresponded to an improvement of 61.6 and 62.8% respectively.
ConclusionThe infiltration with methylprednisolone in anserin syndrome is not superior to placebo in patients taking diclofenac measured by the WOMAC scale at 4 weeks. The incidence of adverse events did not show any differences either.
El síndrome anserino (SA), también conocido como bursitis anserina o tendinobursitis anserina, es una causa frecuente de dolor medial de rodilla. Existe controversia acerca de la estructura que produce el SA. La prevalencia en México es del 0,34% (IC del 95%, 0,24-0,45), por debajo del dolor plantar, entre las afecciones de dolor regional en el miembro inferior, como fue reportado en un estudio transversal, multietápico, estratificado y aleatorizado de tres regiones del país con la metodología utilizada en el programa COPCORD (Community Oriented Program in the Rheumatic Diseases)1.
Dada la falta de evidencia de la estructura involucrada en este síndrome y su diagnóstico clínico sencillo, este último se establece sobre la base del dolor medial de la rodilla con la palpación dolorosa en la cara inferomedial de esta. No se requieren estudios de imagen. El punto clave del dolor se sitúa en la cara medial de la tibia, 3 a 5 cm distal de la línea articular de la rodilla. No existen criterios validados para esta alteración y la utilidad diagnóstica de las maniobras arriba descritas no se ha evaluado2.
Para su manejo, se utilizan la fisioterapia, los antiinflamatorios no esteroideos orales y la corrección de los factores predisponentes (p. ej., el sobrepeso). En caso de que no responder, se efectúa la infiltración de glucocorticoides3. De esta última modalidad de tratamiento, no se han publicado ensayos clínicos y las publicaciones existentes carecen de rigor metodológico4,5.
El objetivo de este estudio fue determinar la eficacia y la seguridad de la infiltración de metilprednisolona para el tratamiento del SA, así como la incidencia de eventos adversos.
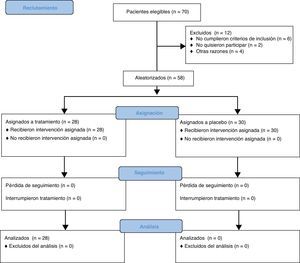
Métodos y materialesSe realizó un ensayo clínico aleatorizado, doble ciego, controlado con placebo, en la clínica de reumatología de la consulta de especialidades de Medicina Interna del Hospital Universitario Dr. José Eleuterio González. En la Figura 1 se observa el diagrama de flujo de reclutamiento, inclusión seguimiento y análisis de los participantes. Se reclutó a pacientes de ambos sexos, de 18 a 90 años de edad, con el diagnóstico clínico prevalente de SA. Se excluyó a los pacientes que fueron portadores de alguna patología intraarticular que reflejara dolor en la cara medial de la rodilla, como meniscopatía, ligamentos colaterales, o plica medial, además de aquellos que utilizaron glucocorticoides, fueron alérgicos al diclofenaco o a la metilprednisolona, o que tuvieron una coagulopatía que impidiera la realización del procedimiento. También se excluyó, a criterio del investigador, a los pacientes con una enfermedad no controlada, incluida la presencia de infección local o sistémica. Se eliminó a los pacientes que no cumplieron con el seguimiento, utilizaron algún tratamiento no especificado durante el estudio y aquellos que presentaron efectos adversos.
El estudio fue previamente aprobado por el comité de ética de la subdirección de investigación de la Facultad de Medicina y Hospital Universitario Dr. José Eleuterio González de la Universidad Autónoma de Nuevo León y registrado en ClinicalTrials.gov. Todos los pacientes firmaron un consentimiento informado por escrito de acuerdo a la Ley General de Salud de México.
Para establecer el diagnóstico del SA, el investigador principal (VM), primero preguntaba al paciente: ¿tiene dolor al subir las escaleras?, ¿el dolor es en la cara medial de la rodilla? Si la respuesta era afirmativa, se realizaba una palpación en el sitio afectado y se establecía el diagnóstico. Durante la exploración física se realizaron maniobras para descartar patología intraarticular y periarticular que se manifiestan con dolor medial de rodilla (menisco, plica, ligamentos colaterales). Una vez obtenido el consentimiento informado se llenaba el cuestionario Western Ontario and McMaster Universities Arthritis Index (WOMAC)6. Posteriormente, en base a una tabla de números aleatorios de 2 grupos del programa Research Randomizer7, se asignaron al grupo 1 para recibir una sola infiltración de metilprednisolona 40mg/1ml+2ml de xilocaína simple al 2% o al grupo 2 para recibir una sola infiltración de 1ml de agua destilada+2ml de xilocaína simple al 2% en el sitio de mayor dolor. Ambos grupos recibieron 100mg de diclofenaco sódico por vía oral cada 24 h durante 10 días. La técnica de infiltración se efectuó de manera radial al punto de más dolor4,8,9 con técnica aséptica y de manera cegada (jeringas cubiertas), por un médico reumatólogo certificado (NL) diferente del evaluador. Se citó a los participantes a las 4 semanas para el llenado de un nuevo cuestionario WOMAC, una escala visual análoga (EVA) de satisfacción del procedimiento y el reporte de eventos adversos. Se estableció como remisión completa una calificación de WOMAC igual a 0 a la semana 4, además de cuantificar el porcentaje de mejoría con respecto a la primera medición.
El número de pacientes reclutados obedeció al cálculo del tamaño de muestra para una diferencia de proporciones, donde la proporción de pacientes con remisión completa a la infiltración con metilprednisolona (P1) vs. la proporción de pacientes con respuesta completa a la infiltración de placebo (P2) eran comparados. P1: 30%, P2: 5% con un alfa de 0,05 bilateral y una significación estadística del 95%. Se determinó una beta de 0,20 para una potencia de 80%, obteniendo una muestra de 27 participantes por grupo. Una p < 0,05 fue estadísticamente significativa.
Se realizó una estadística descriptiva de las variables clínico-epidemiológicas numéricas para determinar su distribución y así determinar su análisis comparativo paramétrico (t de Student) o no parámetrico (U de Mann-Whitney). Para las variables categóricas se utilizó la prueba de la chi al cuadrado y la prueba exacta de Fisher si se requería. Se evaluó la aleatorización de los participantes con pruebas estadísticas de diferencia según la distribución de variable. Se compararon los índices WOMAC basal y a las 4 semanas intragrupo con la prueba de rangos de Wilcoxon. Para establecer los objetivos primario de eficacia y secundario de seguridad de la infiltración se utilizaron las pruebas de la U de Mann-Whitney y exacta de Fisher, respectivamente.
ResultadosSe reclutó a 58 participantes: 28 fueron infiltrados con xilocaína y metilprednisolona (grupo 1) y 30 con xilocaína y agua destilada (grupo 2). En la tabla 1 se observan las características clínico-epidemiológicas junto a la demostración de homogeneidad de cada variable por grupo. El promedio de edad fue de 54,3 y 54,4 años, respectivamente. Eran mujeres el 75% y el 80% de los incluidos en ambos grupos. El promedio del IMC se situó en 30,9 y 30,6kg/cm2. No se encontró diferencia entre la ocupación de los participantes. En la mayoría de los casos el dolor se localizaba en la rodilla izquierda y la mediana de duración de la afección fue de 52 y 50 semanas en cada uno de los grupos. La mediana del WOMAC inicial en el grupo 1 fue de 32, mientras que en el grupo 2 fue de 25,5, sin una diferencia estadística.
Características clínico-epidemiológicas basales
| Grupo 1 (n=28) | Grupo 2 (n=30) | p | |
| Edad, años | 53,4 (12,5) | 54,4 (10) | 0,75 |
| Mujeres (%) | 21 (75) | 24 (80) | 0,65 |
| Peso, kg | 76,6 (14,1) | 73,3 (11,2) | 0,32 |
| Talla, cm | 158,5 (8,2) | 158,7 (9) | 0,94 |
| IMC, kg/cm2 | 30,9 (4,1) | 30,6 (4,5) | 0,80 |
| Ocupación (%) | 0,26b | ||
| Hogar | 18 (64,3) | 17 (56,7) | |
| Empleado | 1 (3,6) | 4 (13,3) | |
| Comerciante | 7 (25) | 9 (30) | |
| Jubilado | 2 (7,1) | 0 | |
| Síndrome anserino en rodilla derecha (%) | 10 (35,7) | 14 (46,7) | 0,39b |
| Evolución semanasa | 52 (72) | 50 (187) | 0,74c |
| WOMAC iniciala | 32 (24,8) | 25,5 (30,5) | 0,40c |
| Dolor | 7 (2,9) | 7,1 (3,07) | 0,89 |
| Rigideza | 3 (4,75) | 3 (6) | 0,78c |
| Funcionalidad | 22,5 (20,5) | 16 (25,3) | 0,31 |
Valores expresados en media y desviación estándar.
Estadístico de prueba: t de Student.
IMC: índice de masa corporal; WOMAC: Western Ontario and McMaster Universities Arthritis Index.
A las 4 semanas, la mediana del WOMAC fue de 8 puntos y de 6,5, respectivamente. El porcentaje de remisión completa fue 21% para el grupo 1 y del 30% para el grupo 2. Ambos grupos mejoraron un 62 y un 63% (diferencia estadísticamente significativa respecto a la medición basal intragrupo). La mediana de la EVA de satisfacción fue de 87,5 y 70, respectivamente. En las tablas 2 y 3 se presentan el resto de las variables evaluadas y la frecuencia de eventos adversos; en ninguno de los dos hubo una diferencia estadísticamente significativa.
Evaluación de la eficacia a las 4 semanas
| Grupo 1 | Grupo 2 | p | |
| WOMAC final | 8 (17) | 6,5 (17) | 0,77 |
| Dolor | 2,5 (3) | 2 (5,5) | 0,78 |
| Rigidez | 0 (1) | 0 (1) | 0,21 |
| Funcionalidad | 4,5 (14) | 4 (17) | 0,74 |
| EVA satisfacción | 87,5 (50) | 70 (65) | 0,32 |
| Remisión completa (%) | 6 (21) | 9 (30) | 0,45c |
| Porcentaje de mejoríaa | 61,6 (37) | 62,8 (33) | 0,89b |
Valores expresados en mediana y rango intercuartílico.
EVA: escala visual análoga; WOMAC: Western Ontario and McMaster Universities Arthritis Index.
Se presenta el primer ensayo clínico que permite la exploración de la eficacia y seguridad de la infiltración de glucocorticoide en pacientes con SA. Se demuestra la eficacia equiparable al placebo de la infiltración de metilprednisolona en un grupo de pacientes que recibe diclofenaco de manera concomitante. La mejoría se encuentra en el 60% de los casos y la remisión a las 4 semanas en el 30%, aproximadamente.
Dentro de las ventajas de este estudio se encuentran las siguientes: el diseño controlado con placebo, el cegamiento de la infiltración y las escalas utilizadas en las evaluaciones, que le proveen mayor rigor metodológico. La evaluación de la eficacia no se redujo a una EVA, como en reportes previos4, sino que evaluó en tres dominios la afectación del SA en el paciente (dolor, rigidez y función).
A pesar de que el uso de la herramienta WOMAC es una de las fortalezas del estudio, también podría ser una de sus debilidades. Esta escala fue diseñada para pacientes con artrosis en rodilla y podría tener poca sensibilidad para medir el dolor, la rigidez y la función solo asociadas al SA, ya que existen ítems que no reflejan necesariamente estrés sobre la estructura en estudio (p. ej., funcionalidad al estar de pie o rigidez matutina). Aun así, la evaluación individual de la escala de dolor medida por WOMAC no demostró diferencia en ambos grupos.
Al comparar nuestros resultados con otros estudios previos, encontramos que Calvo-Alén et al. reportaron los resultados de 44 pacientes con SA que fueron asignados a recibir 500mg de naproxeno sódico 2 veces al día o la infiltración con glucocorticoide. El desenlace principal fue el dolor evaluado usando una escala verbal de intensidad al mes de seguimiento. El 58% del grupo de naproxeno tuvo una «mejoría significativa» y en el 5% la afección se resolvió. En los pacientes con infiltración, el 70% tuvo «mejoría significativa» y la afección se resolvió en el 30% (p<0,05)4. El porcentaje de resolución es similar a lo encontrado en nuestro ensayo en ambos grupos infiltrados.
Asimismo, en una revisión retrospectiva de 29 pacientes con SA, la remisión clínica se observó de 11 de 12 pacientes que recibieron infiltración, comparada con 7 de 17 que no la recibieron5.
Finalmente, Yoon y Kim9 evaluaron con ultrasonido a 26 pacientes con diagnóstico de artrosis de la rodilla y SA. A 17 de ellos se realizó infiltración con acetónido de triamcinolona en la bursa. La respuesta terapéutica fue valuada por las escalas EVA y WOMAC y por una evaluación global del paciente y del investigador usando la escala de Likert. En solo 2 pacientes (8,7%) se demostró la presencia de bursitis/tendinitis anserina por ultrasonido. Los parámetros de la EVA, el índice de dolor y la capacidad funcional del WOMAC demostraron una mejoría estadísticamente significativa después de la infiltración. La evaluación global de los pacientes reveló una respuesta excelente en 2 casos, buena en 6 y moderada en uno; en 8 casos hubo ausencia de mejoría y ninguno empeoró. El WOMAC basal de la cohorte correspondió a 47 puntos y el posterior al tratamiento fue de 37. En los 2 pacientes que reportaron una respuesta excelente, se evidenció mediante ultrasonografía la bursitis. Aunque en ese estudio se infiltró otro esteroide diferente del nuestro y se hizo el esfuerzo por documentar con ultrasonido la lesión, el procedimiento no fue controlado y se observó una satisfacción similar a la que presentaron nuestros pacientes en ambos grupos.
En cuanto a las características demográficas, el promedio de edad de los participantes fue de 63 años y el índice de masa corporal de 26kg/m2. Presentaron una duración promedio de la enfermedad de 93 meses. Por el contrario, en el presente estudio la población incluida tuvo un promedio de edad 10 años inferior, la mayoría eran obesos y la mediana de la duración de los síntomas fue de 12 meses.
En nuestra serie, no fue posible realizar la confirmación ultrasonográfica de la lesión y, a diferencia del estudio de Yoon y Kim, nosotros utilizamos acetato de metilprednisolona como glucocorticoide y no triamcinolona, dado que en nuestro medio es más utilizada para la infiltración.
Otra de las posibles desventajas es que la aplicación de los resultados de este estudio en la práctica clínica obedecería solo a pacientes dentro del rango de edad establecido y que usen antiinflamatorios no esteroideos orales, que se utilizaron de manera compasiva y por fines éticos para el grupo 2. En los pacientes en los cuales el uso de diclofenaco no es posible, se recomienda la infiltración con metilprednisolona. Este escenario clínico no fue abordado en nuestro trabajo.
Se decidió indicar diclofenaco ya que es un antiinflamatorio eficaz y seguro para la mayoría de los participantes y nos permitió controlar el uso de otros medicamentos por parte del paciente, lo que se reflejó en un mejor control de las condiciones del estudio. No consideramos que el uso del antiinflamatorio modificara la respuesta que se observó en el estudio, solo tal vez la magnitud de la mejoría, pero sin modificar la diferencia obtenida.
Cuando los resultados de un ensayo comparativo como este no demuestran la diferencia entre las variables de desenlace, es menester realizar una prueba de poder estadístico. En nuestro estudio se ubicó entre el 90 y el 95% y nos permitió establecer con más seguridad la igualdad de los resultados obtenidos en el ensayo. Aun así, debemos considerar que posiblemente el tamaño de la muestra fue deficiente y no nos permitió encontrar la diferencia en las intervenciones, ya que fue calculada en base a las diferencias encontradas en un ensayo clínico no cegado4. En un diseño ulterior se podría considerar la diferencia porcentual que se obtuvo en este ensayo y probablemente permitiría encontrar la diferencia clínica esperada por el tratamiento activo.
Se han sugerido en reportes previos la utilización de un placebo completo para este grupo, que corresponde a la infiltración de agua destilada sin xilocaína, para sustraer el efecto de la xilocaína en la evaluación y de esta manera tener una medición más limpia del efecto del glucocorticoide. Sin embargo, consideramos que es poco ético. Por otra parte, hay que puntualizar que la absorción de la xilocaína es de 30 min10 y es poco probable que el efecto a largo plazo sea provisto por este. Sin embargo, reconocemos que el efecto del uso de la xilocaína pudo ser determinante para la mejoría del 63% intragrupo en el grupo 2, pero no fue suficiente para mostrar diferencia entre los grupos de comparación. En un ensayo posterior sería adecuado evaluar la infiltración solo de xilocaína contra una infiltración de placebo de agua destilada.
Se sugiere también el uso de técnicas de imagen, principalmente ultrasonido e imagen por resonancia magnética, para la localización de la estructura afectada en el SA y reportar qué y en dónde se está infiltrando. Esto también permitiría descartar, de manera objetiva, cualquier patología intraarticular, que reduciría aún más el sesgo en la evaluación del dolor11. Sin embargo, la prevalencia del SA en estudios que lo buscan intencionadamente no es muy ilustrativa; además de que en los estudios descriptivos sobre lesiones de rodilla las alteraciones en la bursa son más prevalentes y hasta están presentes en las rodillas asintomáticas, por lo que el papel de los estudios de imagen aun no está definido12,13.
De la misma manera, es importante realizar un seguimiento a largo plazo para definir la tasa de recurrencia del SA por grupo y así investigar sí existe alguna superioridad por utilizar metilprednisolona.
Aun tomando en cuenta las consideraciones anteriores, podemos concluir que el uso de la infiltración de metilprednisolona no supera al placebo en la obtención de mejoría a las 4 semanas en pacientes con SA que toman diclofenaco.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.