El rhupus es una entidad poco común en la que se superponen datos de lupus eritematoso generalizado y artritis reumatoide, predominando con frecuencia las manifestaciones articulares. En muchos casos el tratamiento con fármacos modificadores de la enfermedad no biológicos es insatisfactorio, por lo que se ha intentado el uso de inmunosupresores y fármacos biológicos.
Se realizó un estudio prospectivo y abierto para evaluar la eficacia y la tolerabilidad de rituximab en pacientes con rhupus. El objetivo principal fue el cambio en el DAS28 a los 6 meses; fueron objetivos secundarios el cambio en MEX-SLEDAI a los 6 meses, el cambio en DAS28 y MEX-SLEDAI durante el seguimiento, el requerimiento de esteroides y el registro de eventos adversos.
Se incluyó a 9 pacientes, todas mujeres, con edad promedio de 43 años y tiempo de evolución de 10 años. Se observó un descenso en la puntuación basal de DAS28 de 5,73 a 3,02 a los 6 meses (p < 0,001). La mejoría en el DAS28 se mantuvo durante el periodo de seguimiento. A los 6 meses, 3 pacientes presentaban remisión por DAS28 y 3 actividad baja. La calificación de MEX-SLEDAI disminuyó de 5 puntos a nivel basal a 1,22 a los 6 meses (p < 0,001) y mantuvo esta mejoría. Se observó una correlación negativa entre la mejoría clínica y los niveles de anti-CCP (r = –0,794; p = 0,011). La dosis de prednisona disminuyó de 11,66mg/día basal a 0,55 y 1,11mg/día a los 12 y 24 meses, respectivamente. En general, el tratamiento con rituximab fue bien tolerado durante el estudio.
En los pacientes de nuestro estudio, el tratamiento con rituximab mostró ser eficaz tanto en las manifestaciones articulares, con reducción significativa del DAS28, como en otras manifestaciones de lupus, con mejoría del MEX-SLEDAI. Consideramos que esta puede ser una buena opción terapéutica para pacientes con rhupus.
Rhupus in an infrequent disease in which an overlap between lupus eritematosus and rheumatoid arthritis exists. Joint manifestations are prominent and treatment with non biological DMARDs is not always satisfactory, so immunosupressors and biological agents have been tried.
A prospective, open clinical study was done to evaluate efficacy and tolerability of rituximab in patients with Rhupus. The main objective was a change in DAS28 at 6 months and secondary objectives were a change in MEX-SLEDAI at 6 months, change in DAS28 and MEX-SLEDAI during follow up, steroid requirements and detection of adverse events.
We included 9 women with a mean age of 43 years and disease duration of 10 years. A significant reduction in DAS28 was observed (from 5.73 at baseline to 3.02 at 6 months, P<.001). Improvement in DAS28 was maintained during follow up. At 6 months, 3 patients were in remission and 3 had low disease activity. MEX-SLEDAI diminished from 5 points at baseline to 1.22 at 6 months (P<.001). There was a negative correlation between clinical improvement and anti-CCP levels (r=-0,794, P=.011). Mean prednisone dose was reduced from 11.66mg/day at baseline to 0,55 and 1.11mg/day at 12 and 24 months. Treatment was well tolerated.
In this study rituximab was effective not only for joint affection but also for other manifestations of the disease. We consider that this biological agent can be a good therapeutic option for patients with rhupus.
El rhupus se ha definido como la superposición de lupus eritematoso generalizado (LES) y artritis reumatoide (AR). Es una entidad muy poco frecuente, ya que existen menos de 150 casos publicados en la literatura. En un estudio epidemiológico se observó que su prevalencia es de alrededor del 0,09%1. A pesar de que algunos autores sostienen que el rhupus representa un subgrupo de LES con manifestaciones articulares predominantes y características, las evidencias tanto clínicas como serológicas parecen suficientes para apoyar que se trata de un síndrome de superposición definido2.
En la mayoría de los casos descritos de rhupus el cuadro clínico inicia como una poliartritis simétrica y erosiva con factor reumatoide y/o anticuerpos antipéptido de citrulina (anti-CCP) positivos que permite clasificarlo como AR. A estos datos se agregan manifestaciones clínicas de LES y anticuerpos específicos para el mismo (anti-ADNds y/o anti-Sm). Además de la artropatía, las manifestaciones más comunes de lupus son de tipo mucocutáneo, hematológico y serositis; es infrecuente el compromiso renal o del sistema nervioso central. La artropatía suele ser la manifestación predominante en estos pacientes, con datos clínicos de inflamación, deformidades y erosiones características de AR e incluso formación de nódulos reumatoides1,3-5.
En muchos de los casos descritos no existe buena respuesta a fármacos modificadores de la enfermedad no biológicos (FARME) y se ha intentado el tratamiento con inmunosupresores (azatioprina, micofenolato de mofetilo) e incluso con fármacos biológicos (abatacept)2,6.
A pesar de la eficacia indudable de los fármacos antifactor de necrosis tumoral en los pacientes con AR, la experiencia previa en pacientes con LES, en los que se ha demostrado poca eficacia e incluso en algunos casos un empeoramiento de los síntomas, hace poco factible intentar el uso de estos medicamentos en los enfermos con rhupus7-9.
Rituximab es un anticuerpo monoclonal dirigido contra la molécula CD20 de los linfocitos B que ha demostrado en forma extensa ser eficaz en el tratamiento de la AR10,11. Además, aunque los reportes recientes de estudios clínicos controlados no han dado los resultados esperados12-14, existen múltiples reportes en la literatura de tratamiento exitoso con rituximab en pacientes con LES y diferentes tipos de manifestaciones, principalmente hematológicas, renales e incluso de sistema nervioso central15-17. No existe en la literatura en este momento ningún reporte específico respecto a la respuesta en manifestaciones articulares, aunque seguramente muchos de estos pacientes las presentaban.
El objetivo de este trabajo fue investigar la eficacia y la tolerabilidad de rituximab en un grupo de pacientes con rhupus.
Pacientes y métodosDiseño del estudioSe realizó un estudio prospectivo y abierto para evaluar la eficacia de rituximab en pacientes con diagnóstico de rhupus. El objetivo principal fue el cambio en el DAS28 a los 6 meses (definiendo mejoría como una disminución de por lo menos 0,618). Fueron objetivos secundarios el cambio en el MEX-SLEDAI a los 6 meses, durante el seguimiento y hasta el final de la evaluación, el cambio en el DAS28 durante el seguimiento y al final de la evaluación y el requerimiento de esteroides, así como el registro de eventos adversos durante el estudio. Se incluyó para el análisis sólo a los pacientes que hubieran cumplido por lo menos 24 meses de seguimiento.
Se registraron los datos demográficos, las características clínicas de la enfermedad y los criterios de clasificación para el LES y la AR, así como los datos de evolución y la respuesta previa a diferentes tratamientos. Todos los pacientes firmaron un consentimiento informado para recibir el tratamiento.
TratamientoLos pacientes recibieron rituximab 1 g en infusión intravenosa para 4 h, previa premedicación con hidroxicina, paracetamol y dexametasona 8mg por vía intravenosa los días 1 y 15 del estudio, con ciclos posteriores cada 9 a 12 meses, dependiendo de la actividad clínica evaluada por DAS2818. Los FARME no biológicos (metotrexato, leflunomida, azulfidina), así como los inmunosupresores (azatioprina, micofenolato de mofetilo, ciclofosfamida) fueron suspendidos un mes previo al inicio del estudio. Se permitió el uso concomitante de dosis bajas de esteroides (máximo 15mg de prednisona/día o su equivalente), así como de hidroxicloroquina, antiinflamatorios no esteroideos y analgésicos, así como terapia adyuvante (hipolipemiantes, antihipertensivos, etc.).
Sujetos de estudioLa población en estudio consistió en pacientes consecutivos mayores de 18 años, con diagnóstico de rhupus según los criterios propuestos por Simon et al.3,19: poliartritis simétrica, erosiva, signos y síntomas de LES y anticuerpos anti-ADNds y/o anti-Sm y enfermedad articular con actividad moderada a severa, definida como DAS28 > 3,218. Para los pacientes en edad fértil, se empleó un anticonceptivo confiable. En todos los pacientes se realizó escrutinio de tuberculosis y perfil viral de hepatitis previo al tratamiento. Los criterios de exclusión consistieron en la presencia de embarazo o lactancia, antecedente de hepatitis, necesidad de uso de otro inmunosupresor o FARME en forma concomitante (excepto antimaláricos) o infección activa al inicio del estudio.
EvaluacionesLos pacientes fueron evaluados en forma trimestral durante todo el seguimiento. En cada visita se interrogó acerca de los síntomas sugestivos de actividad, se realizó una exploración física completa por un reumatólogo y se determinó el puntaje de DAS28 y MEX-SLEDAI, registrando también medicamentos concomitantes y presencia de eventos adversos en forma intencionada. Además se realizaron estudios de laboratorio de rutina que incluyeron biometría hemática completa con diferencial, y recuento de plaquetas, química sanguínea, examen general de orina, depuración de creatinina, albúmina en orina de 24 h, reactantes de fase aguda (velocidad de eritrosedimentación, proteína C reactiva) y niveles de C3 y C4.
Análisis estadísticoSe empleó estadística descriptiva, prueba exacta de Fisher para variables cualitativas y t de Student para las cuantitativas. La comparación de diferencias se realizó con la prueba de rangos de Wilcoxon. Se empleó el programa SPSS versión 15 en español.
ResultadosCaracterísticas de los sujetos de estudio: se incluyó a 9 pacientes, todas fueron mujeres, con una media de edad de 43 años (rango de 38-57 años) y un tiempo de evolución de la enfermedad de 10,03 años (rango 1,8-22 años). En 6 pacientes el diagnóstico inicial fue AR y precedió a las manifestaciones de LES en 2,5 años como promedio; solo en 3 pacientes fue el LES el diagnóstico inicial. En la tabla 1 se describen los datos demográficos, las características clínicas y serológicas, y el tratamiento previo de las pacientes incluidas, así como los criterios con los que se hizo el diagnóstico de rhupus. Debe mencionarse que en todas las pacientes se empleó previamente tratamiento con antiinflamatorios no esteroideos, esteroides en dosis medias o bajas y FARME no biológicos en monoterapia o terapia combinada sin éxito.
Características clínicas y serológicas de los pacientes
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | Total | |
| Edad, años | 43 | 38 | 39 | 52 | 43 | 57 | 36 | 42 | 38 | 43 (38-57) |
| Sexo, F/M | F | F | F | F | F | F | F | F | F | 9 (100%) |
| Años diagnóstico | 18 | 22 | 12 | 5 | 10 | 13 | 6 | 1,8 | 2,5 | 10,03 (1,8-22) |
| Artritis | + | + | + | + | + | + | + | + | + | 9 (100%) |
| Fotosensibilidad | + | + | + | + | + | + | 6 (66,6%) | |||
| Eritema malar | + | + | + | + | + | + | + | + | 8 (88,8%) | |
| Úlceras orales | + | + | + | + | + | + | + | 7 (77,7%) | ||
| Lupus discoide | + | 1 (11,1%) | ||||||||
| Serositis | + | 1 (11,1%) | ||||||||
| Renal | iii | iia | v | ii | 4 (44,4%) | |||||
| Neurológico | 0 | |||||||||
| Hematológico | L-L | L-L | L-L-T | L-L | L-L | L-L | 6 (66,6%) | |||
| VSG/PCR + | + | + | + | + | + | + | + | + | + | 9 (100%) |
| FR | 72 | 410 | 752 | 681 | - | 212 | 74 | 4560 | 120 | 8 (88,8%) |
| Anti-CCP | 172 | 197 | 68 | 433 | 1260 | 311 | - | 300 | 224 | 8 (88,8%) |
| AAN | HD | MG | HD | HD | HD | HD | HD | HD | LP | 9 (100%) |
| Anti-ADNds | + | + | + | + | + | 5 (55,5%) | ||||
| Erosiones Rx | + | + | + | + | + | + | + | + | 8 (88,8%) | |
| Criterios | ||||||||||
| AR | + | + | + | + | + | + | + | + | + | 9 (100%) |
| LES | + | + | + | + | + | + | + | + | + | 9 (100%) |
| Tratamiento previo | ||||||||||
| Esteroides | + | + | + | + | + | + | + | + | + | 9 (100%) |
| Antimaláricos | + | + | + | + | + | + | + | 7 (77,7%) | ||
| Metotrexato | + | + | + | + | + | + | + | + | 8 (88,8%) | |
| Azulfidina | + | + | + | + | + | + | + | 7 (77,7%) | ||
| Azatioprina | + | + | + | 3 (33,3%) | ||||||
| Ciclofosfamida | + | 1 (11,1%) | ||||||||
| Micofenolato | + | + | 2 (22,2%) | |||||||
AAN: anticuerpos antinucleares; anti-ADNds: anticuerpos anti-ADN de doble cadena; anti-CCP: anticuerpos antipéptido de citrulina; AR: artritis reumatoide; F: femenino; FR: factor reumatoide; HD: homogéneo difuso; LES: lupus eritematoso sistémico; L-L: leucolinfopenia; L-L-T: leucolinfopenia y trombocitopenia; LP: lineal periférico; M: masculino; MG: moteado grueso.
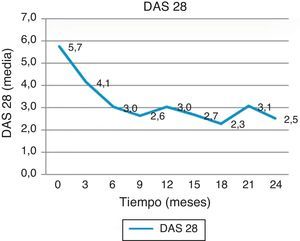
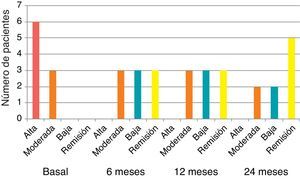
Eficacia clínica: se observó buena respuesta clínica, con descenso en la puntuación basal de DAS28 de 5,73 a 4,13 a los 3 meses y a 3,02 a los 6 meses, cambio estadísticamente significativo (p < 0,001). La mejoría en el DAS28 se mantuvo durante el periodo de seguimiento, con calificación DAS 28 de 3,04 a los 12 meses y 2,52 a los 24 meses, como lo muestra la figura 1. A los 6 meses 3, pacientes presentaban remisión por DAS28 y 3 actividad baja. La figura 2 muestra el porcentaje de pacientes con actividad alta, moderada, baja o remisión por DAS28 en forma basal y a los 6, 12 y 24 meses de seguimiento.
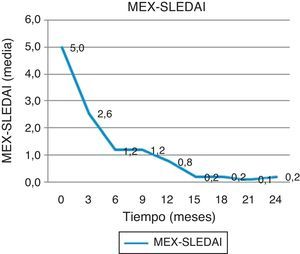
Respecto a la calificación de MEX-SLEDAI, esta disminuyó de 5 puntos a nivel basal a 2,56 a los 3 meses y 1,22 a los 6 meses (p < 0,001) y mantuvo esta mejoría a los 12 (0,78) y 24 (0,22) meses (fig. 3). Como ya se mencionó, la decisión de aplicar un segundo tratamiento de rituximab dependió de la actividad clínica. En 8 pacientes se observó un incremento en la actividad por DAS28 entre los 9 y 12 meses, por lo que se administró un segundo tratamiento de rituximab; solo en una paciente este fue necesario hasta los 15 meses. Al realizar un análisis multivariado, encontramos una correlación negativa entre la mejoría clínica evaluada por DAS28 a los 12 meses y los niveles de anti-CCP (r = –0,794, p = 0,011).
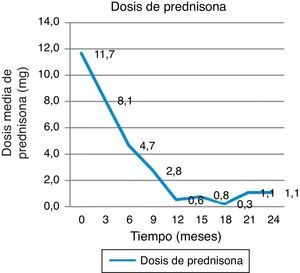
Una medida indirecta de eficacia clínica del tratamiento es la capacidad para disminuir la dosis de esteroide y/o descontinuarla durante el estudio. La dosis basal de prednisona en nuestro grupo de pacientes fue de 11,66mg de prednisona/día y logró disminuirse en forma progresiva a 4,72mg a los 6 meses y a 0,55 y 1,11mg/día a los 12 y 24 meses, respectivamente. La gran mayoría de los pacientes6 no requirió esteroides por vía oral desde los 12 meses de tratamiento (fig. 4).
Aspectos de seguridad: en general, el tratamiento con rituximab fue bien tolerado durante el estudio. Los eventos adversos se dividieron como reacciones inmediatas a la infusión, eventos infecciosos y eventos adversos serios. Ocurrieron 3 reacciones adversas en 2 pacientes durante la infusión de rituximab, que consistieron en eritema y prurito, cediendo en todas las ocasiones al suspender temporalmente la infusión y administrar esteroides y antihistamínicos por vía intravenosa. Ocurrieron 9 eventos infecciosos no serios en 6 pacientes, principalmente infecciones de las vías urinarias bajas (6 casos) e infección de las vías respiratorias altas (3 eventos), en ambos casos no complicados. Solo una paciente cursó con un evento de neumonía que se consideró serio por requerir manejo hospitalario, con adecuada recuperación clínica. No se presentaron muertes, neoplasias o infecciones oportunistas durante el periodo de seguimiento.
DiscusiónEn los pacientes de nuestro estudio el tratamiento con rituximab mostró ser eficaz tanto en las manifestaciones articulares, con reducción significativa del DAS28, como en otras manifestaciones de lupus, con mejoría del MEX-SLEDAI. La respuesta clínica fue evidente a los 6 meses; sin embargo, comenzó a ser manifiesta desde los 3 meses de evaluación y se mantuvo en todos los pacientes durante la fase de seguimiento con los ciclos repetidos de tratamiento en el momento en que se evidenció reactivación clínica.
Por lo general, las manifestaciones articulares en los pacientes con LES suelen responder en forma satisfactoria a FARME no biológicos o esteroides en dosis bajas; sin embargo, en los pacientes con rhupus un gran porcentaje de los casos no tiene buena respuesta, presentando en muchos casos artropatía poliarticular con daño estructural progresivo3,4,6,20,21. Dentro de las diferentes opciones de terapia biológica, el bloqueo de anti-CD20 con rituximab puede ser una buena elección. Existen múltiples reportes de series de casos que han demostrado la eficacia de este medicamento en pacientes con diversas manifestaciones de lupus15. En un metaanálisis reciente publicado por Ramos-Cassals se realizó una revisión sistemática de 188 pacientes con lupus tratados con rituximab entre 2002 y 2007, encontrando que la terapia fue eficaz en el 91% de los casos16. De los pocos estudios controlados y aleatorizados que existen a la fecha, en el estudio EXPLORER, que incluyó a 257 pacientes con lupus con actividad moderada a severa, no se observó diferencia significativa en el porcentaje de pacientes que alcanzaron respuesta importante (1,24 vs. 15.9) o parcial (17,2 vs. 12,5) en los grupos tratados con rituximab o placebo, respectivamente12,13. Un resultado semejante se observó en el estudio LUNAR, que incluyó a 144 pacientes con nefritis lúpica iii o iv y en el que tampoco pudo demostrarse una diferencia significativa entre rituximab y placebo14. Sin embargo, es importante mencionar que, en ambos estudios, la respuesta con rituximab pareció mejor en los grupos minoritarios y que además debe considerarse que en ambos estudios los pacientes recibían el tratamiento estándar del lupus, lo que dificulta detectar diferencia entre ambos grupos. Nosotros reportamos en 2010 un estudio abierto en pacientes con lupus y que recibieron ciclofosfamida o rituximab. Los resultados favorecieron a rituximab y, aunque todos los pacientes tenían manifestaciones graves de la enfermedad como criterio para ser incluidos, un porcentaje significativo tenía manifestaciones articulares, que mejoraron22.
Recientemente se publicaron los resultados del registro francés de pacientes con lupus tratados con rituximab. Los autores observaron una adecuada respuesta clínica en alrededor del 80% de los pacientes; específicamente, ocurrió mejoría de las manifestaciones articulares en el 72%17. En la actualidad, se desarrollan otros estudios clínicos controlados multicéntricos en pacientes con diferentes manifestaciones de lupus, como el estudio RING, que evaluará la eficacia de rituximab para lograr remisión en la nefritis lúpica y cuyos resultados sin duda serán de gran valor para definir cada vez mejor la utilidad de este fármaco biológico23.
En los pacientes con rhupus, si bien coexisten manifestaciones de ambas afecciones, lupus y AR, es característico el predominio durante la evolución de las manifestaciones articulares, que suelen dominar el cuadro clínico de la enfermedad, en ocasiones con manifestaciones mucocutáneas y con mucho menos frecuencia manifestaciones renales, hematológicas serias o del sistema nervioso1,3-5. Esto no fue diferente en nuestros pacientes, en los que la expresión de difícil manejo era la articular, con manifestaciones generales o mucocutáneas asociadas que explican calificaciones bajas de MEX-SLEDAI, que sin embargo, mejoraron durante el curso del estudio.
Se ha descrito también relación entre la severidad de las manifestaciones articulares en los pacientes con rhupus y la positividad a anticuerpos anti-CCP5,24-26, de ahí que la correlación negativa que encontramos entre los títulos de estos anticuerpos y la respuesta clínica sea del todo explicable.
Sin dejar de reconocer las limitaciones de nuestro trabajo, que incluyó un número pequeño de pacientes con rhupus, lo que se debe a la muy baja prevalencia de esta entidad1 y a que se trata de un estudio abierto no controlado, consideramos que los resultados obtenidos son alentadores y, hasta cierto punto, esperados, si consideramos la experiencia previa, que es muy amplia, en el tratamiento con rituximab de pacientes con AR y los reportes de mejoría en muy diversas manifestaciones de LES, que colocan al rituximab como un medicamento muy adecuado para el manejo de pacientes con rhupus e incluso con lupus y manifestaciones articulares prominentes.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesAndrade-Ortega: conferencista para Roche, Bristol, Pfizer, Merck.
Irazoque-Palazuelos: Advisory board y/o conferencista para Roche, Bristol, Pfizer, Jannsen, Merck.
Muñoz-López: conferencista para Sanofi, Pfizer.
Rosales-Don Pablo. Conferencista para Pfizer.