Analizar el efecto del secukinumab sobre las variables propias reportadas por el paciente diagnosticado de artritis psoriásica y/o espondilitis anquilosante en relación con su estado de salud, dolor, fatiga, sueño y calidad de vida.
MétodosSe realizó un estudio observacional, longitudinal, prospectivo y multicéntrico a 6meses con 39 pacientes que iniciaron tratamiento con secukinumab para la terapia de artritis psoriásica y/o espondilitis. Las variables principales fueron los cambios en las medidas reportadas por el paciente, evaluándolas por medio de los cuestionarios FACIT-fatiga, Índice de Gravedad del Insomnio, EuroQol-3L-5D y PsAQoL. Adicionalmente, y dependiendo del tipo de enfermedad (psoriásica periférica o espondiloartritis), se recogió el DAS28 con velocidad o el BASDAI, respectivamente.
ResultadosLos niveles de fatiga, insomnio moderado y grave presentan una reducción significativa tras el tratamiento de 6meses con secukinumab. Al mismo tiempo, la calidad de vida reportada por el paciente aumenta notablemente (p=0,006). Los datos referentes al dolor y a la incomodidad también presentan una notable mejoría tras el tratamiento.
ConclusionesLos pacientes de artritis psoriásica y/o espondilitis anquilosante que inician tratamiento con secukinumab presentan mejoría a los 6meses en todos los tamaños del efecto del tratamiento, particularmente en el sueño, la fatiga y la calidad de vida. Además, las medidas de desenlace reportadas por los pacientes son un valor clínico adicional y permiten realizar una valoración más exacta y aproximada de su estado real de salud y bienestar.
To analyse the effect of secukinumab on self-reported variables of patients diagnosed with psoriatic arthritis and/or ankylosing spondylitis in relation to their health status, pain, fatigue, sleep and quality of life.
MethodsA six-month, observational, longitudinal, prospective, multicentre study was conducted with 39 patients who initiated treatment with secukinumab as therapy for psoriatic arthritis and/or spondylitis. The main variables were changes in patient-reported measures and they were evaluated by means of the questionnaires: FACIT-fatigue, Insomnia Severity Index, EuroQol-3L-5D and PsAQoL. In addition, depending on the type of disease (peripheral psoriasis or spondyloarthritis) the DAS28 with ESR or the BASDAI were calculated, respectively.
ResultsLevels of fatigue, moderate and severe insomnia significantly reduced after 6months of treatment with secukinumab. At the same time, patient-reported quality of life increased significantly (P=.006). Data on pain and discomfort also show significant improvement after the treatment.
ConclusionsPatients with psoriatic arthritis and/or ankylosing spondylitis who start treatment with secukinumab show improvement at 6months in all effect sizes of the treatment, particularly in sleep, fatigue and quality of life. Furthermore, patient-reported outcome measures are of additional clinical value and allow more accurate and closer assessment of their real status of health and well-being.
La artritis psoriásica es una entidad inflamatoria articular que ocurre en el contexto de un paciente con psoriasis cutánea o que presenta un antecedente familiar de primer grado al respecto1,2. Tiene una prevalencia de 6-25 casos por cada 10.000 personas y afecta al 20-30% de los pacientes que presentan dicha afectación cutánea3,4. La artritis psoriásica puede presentarse como una forma de afectación periférica en forma de oligoartritis asimétrica o poliartritis simétrica y/o en forma de afectación axial correlacionándose con dolor lumbosacro inflamatorio y rigidez de espalda, lo que puede conducir a un deterioro funcional y a una reducción en la calidad de vida5,6.
Se sabe que el eje interleucina IL-23/IL-17A está implicado en una variedad de funciones biológicas tales como inflamación, daño y lesiones articulares, estando también presente en el mecanismo patogénico de la artritis psoriásica y espondilitis7. Estudios recientes han demostrado que la inhibición del receptor de IL-17A con secukinumab, un anticuerpo monoclonal anti IL-17A humano, mejora los signos y síntomas de la enfermedad7-9. Sin embargo, la naturaleza multifactorial de la patología dificulta la utilización de medios que reflejen cambios en la evolución del tratamiento y su impacto en la calidad de vida del paciente.
En los últimos años se han desarrollado una serie de cuestionarios10-12 destinados a evaluar la eficacia y la efectividad de las intervenciones sanitarias bajo la premisa de que incorporar el punto de vista del paciente debe contribuir de manera decisiva a evaluar los méritos relativos de los tratamientos en los ensayos clínicos13. Desde esta perspectiva, en nuestro estudio analizamos el efecto del secukinumab en cuanto a las variables reportadas por el paciente, concretamente la fatiga, el sueño y la calidad de vida en pacientes con artritis psoriásica y/o espondiloartritis.
Material y métodosSe realizó un estudio multicéntrico, observacional, longitudinal y prospectivo a 6meses en el que se seleccionaron 39 pacientes provenientes del área de Valencia y se llevó a cabo un muestreo consecutivo de todos aquellos que iniciaran tratamiento con secukinumab con cualquier indicación reumatológica.
Las variables principales fueron los cambios en las medidas reportadas por el paciente, evaluando de forma global la salud tanto en la visita inicial como transcurridos 6meses mediante una escala visual analógica (EVA). También se recogieron medidas de cada paciente referidas a la fatiga usando la escala FACIT-fatiga. Para la evaluación del sueño se empleó el Índice de Gravedad del Insomnio y para la calidad de vida del paciente los cuestionarios EuroQol-3L-5D y PsAQoL. Como criterios de confusión se estableció el método de administración de secukinumab (en monoterapia o con FAME), la administración de biológicos previos y la medicación con corticoides o AINE del paciente durante el estudio. Adicionalmente, y dependiendo del tipo de enfermedad (psoriásica periférica o espondiloartritis), se recogió el DAS28 con velocidad o el BASDAI, respectivamente.
- •
La Escala FACIT es un cuestionario que contiene 13ítems. Cada respuesta se evalúa por medio de una escala tipo Likert de 5 puntos, siendo 0 ausencia de problema y 4 la máxima cantidad, e incluye elementos como el cansancio, la debilidad, la apatía, la falta de energía y el impacto que estos sentimientos producen en el paciente. El rango global de la escala es de 0 a 52, y la suma de valores más bajos denota mayores niveles de fatiga4,11,14.
- •
El Índice de Gravedad del Insomnio (IGI) es un cuestionario que consta de 7 ítems en los que se evalúan la naturaleza, la gravedad y el impacto del insomnio. Las dimensiones evaluadas son: severidad del inicio del sueño y problemas para despertarse temprano en la mañana, insatisfacción del sueño, dificultades para dormir y la percepción externa del problema. Para calificar cada elemento cuenta con una escala Likert de 5 puntos, siendo 0 la ausencia de problemas y 4 la existencia de problemas graves. De esta manera genera una escala donde 0-7 se interpreta como ausencia de insomnio; 8-14 insomnio por debajo del umbral; 15-21 insomnio moderado; 22-28 insomnio severo15.
- •
El EuroQol-5D-3L (EQ-5D) es un instrumento genérico de medición de la calidad de vida mediante el cual el propio paciente valora su estado de salud por dimensiones referentes a la movilidad, el cuidado personal, las actividades cotidianas, el dolor y el malestar, la ansiedad y la depresión. Cada una de ellas está valorada en 3 niveles de gravedad y un EVA de evaluación general. Un tercer elemento del EQ-5D es el índice de valores sociales, que consta de 5 dimensiones (movilidad, cuidado personal, actividades cotidianas, dolor/malestar y ansiedad/depresión), cada una de las cuales es calificada de uno a tres, siendo 1 ausencia de problemas y 3 problemas graves. La segunda parte del EQ-5D es una EVA en la que el paciente indica la valoración de su estado general de salud en una escala de 0 a 100, donde 0 es el mejor estado de salud posible y 100 el peor, siendo la diferencia mínima significativa 1016.
- •
El cuestionario PsAQoL es un instrumento específico de evaluación de la calidad de vida. Consta de 20 preguntas sí/no derivadas directamente de entrevistas cualitativas realizadas a pacientes y se utiliza con éxito en enfermedades como la artritis reumatoide, la espondilitis y el lupus eritematoso. La puntuación total se calcula como el número de preguntas afirmativas y puede variar de 0 a 20, siendo los valores más altos indicativos de mala calidad de vida17.
El análisis estadístico de las muestras se realizó mediante medidas de tendencia central, analizando los cambios tras los 6meses mediante la prueba t de Student para los datos pareados en el caso de FACIT, EVA, PsAQoL e IGI y con la prueba chi-cuadrado para las dimensiones del cuestionario EQ-5D. Los cambios en las medidas reportadas por el paciente fueron analizados en modelos de regresión lineal múltiple con intervalos de confianza del 95%. El tamaño de efecto de cada una de las medidas fue calculado mediante la d de Cohen (diferencia de medias/desviación agregada). Los resultados fueron analizados por grupos de enfermedad y en global por medio del programa Stata v12 (College Station, Tx, EE.UU.).
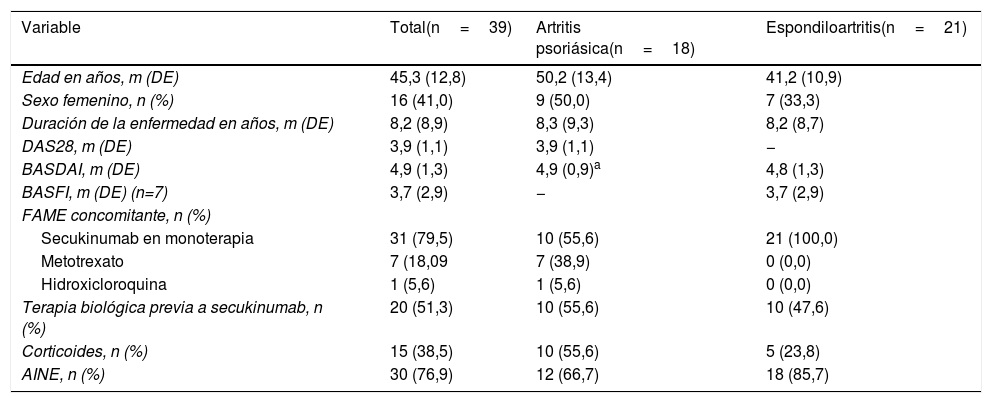
ResultadosLos 39 pacientes a los que se les realizó el estudio fueron clasificados en dos grupos dependiendo de si padecían artritis psoriásica o espondiloartritis, con una edad media de 50,2±13,4 y 41,2±10,9años, respectivamente. De todos ellos, el 54% presentaban un cuadro predominantemente axial y el 46% restante presentaban artritis periférica. En cuanto a los fármacos empleados como terapia, tanto el tratamiento en combinación con un fármaco modificador o con corticoides era más frecuente entre los pacientes con cuadros periféricos que entre los de predominio axial (tabla 1). Además, aproximadamente la mitad de los pacientes de cada grupo había sido tratados con algún biológico previo.
Descripción basal de los 39 pacientes del estudio
| Variable | Total(n=39) | Artritis psoriásica(n=18) | Espondiloartritis(n=21) |
|---|---|---|---|
| Edad en años, m (DE) | 45,3 (12,8) | 50,2 (13,4) | 41,2 (10,9) |
| Sexo femenino, n (%) | 16 (41,0) | 9 (50,0) | 7 (33,3) |
| Duración de la enfermedad en años, m (DE) | 8,2 (8,9) | 8,3 (9,3) | 8,2 (8,7) |
| DAS28, m (DE) | 3,9 (1,1) | 3,9 (1,1) | − |
| BASDAI, m (DE) | 4,9 (1,3) | 4,9 (0,9)a | 4,8 (1,3) |
| BASFI, m (DE) (n=7) | 3,7 (2,9) | − | 3,7 (2,9) |
| FAME concomitante, n (%) | |||
| Secukinumab en monoterapia | 31 (79,5) | 10 (55,6) | 21 (100,0) |
| Metotrexato | 7 (18,09 | 7 (38,9) | 0 (0,0) |
| Hidroxicloroquina | 1 (5,6) | 1 (5,6) | 0 (0,0) |
| Terapia biológica previa a secukinumab, n (%) | 20 (51,3) | 10 (55,6) | 10 (47,6) |
| Corticoides, n (%) | 15 (38,5) | 10 (55,6) | 5 (23,8) |
| AINE, n (%) | 30 (76,9) | 12 (66,7) | 18 (85,7) |
AINE: antiinflamatorios no esteroideos; BASDAI: Bath Ankylosing Spondylitis Disease Activity Index; BASFI: Bath Ankylosing SpondylitisFunctional Index; DAS28: Disease Activity Score de 28 articulaciones; DE: desviación estándar; FAME: fármacos modificadores de la enfermedad; m: media.
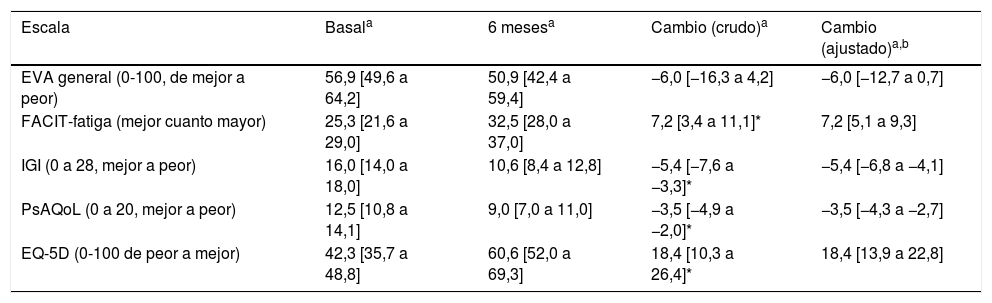
Para el análisis de las variables centradas en el paciente y la calidad de vida se llevaron a cabo cuestionarios en la consulta basal y tras 6meses de tratamiento con secukinumab. A excepción de la Escala Visual Analógica (EVA), en todas las variables de estudio se observan cambios significativos y relevantes tras el tratamiento con secukinumab. Tras los 6meses de tratamiento se observa una reducción notable en los niveles de fatiga (tabla 2). Así mismo, al analizar los cuestionarios referentes a la calidad de vida (PsAQoL y EQ-5D) se observa una notable mejoría tras el tratamiento.
Cambios en cada una de las variables centradas en el paciente tres 6 meses de terapia con secukinumab
| Escala | Basala | 6 mesesa | Cambio (crudo)a | Cambio (ajustado)a,b |
|---|---|---|---|---|
| EVA general (0-100, de mejor a peor) | 56,9 [49,6 a 64,2] | 50,9 [42,4 a 59,4] | −6,0 [−16,3 a 4,2] | −6,0 [−12,7 a 0,7] |
| FACIT-fatiga (mejor cuanto mayor) | 25,3 [21,6 a 29,0] | 32,5 [28,0 a 37,0] | 7,2 [3,4 a 11,1]* | 7,2 [5,1 a 9,3] |
| IGI (0 a 28, mejor a peor) | 16,0 [14,0 a 18,0] | 10,6 [8,4 a 12,8] | −5,4 [−7,6 a −3,3]* | −5,4 [−6,8 a −4,1] |
| PsAQoL (0 a 20, mejor a peor) | 12,5 [10,8 a 14,1] | 9,0 [7,0 a 11,0] | −3,5 [−4,9 a −2,0]* | −3,5 [−4,3 a −2,7] |
| EQ-5D (0-100 de peor a mejor) | 42,3 [35,7 a 48,8] | 60,6 [52,0 a 69,3] | 18,4 [10,3 a 26,4]* | 18,4 [13,9 a 22,8] |
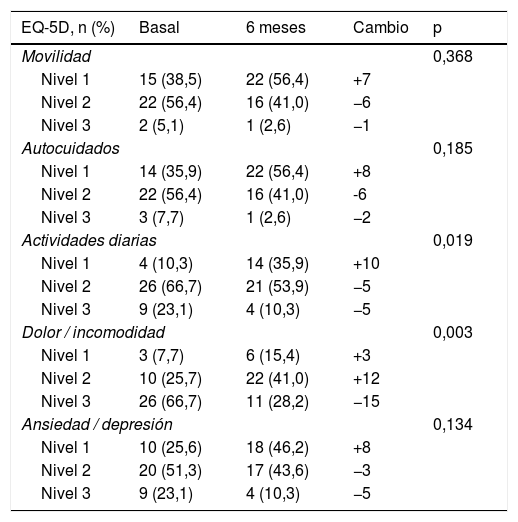
Los subítems donde se obtienen las mayores diferencias tras los 6meses de tratamiento con secukinumab se producen en las variables referentes al dolor y a la incomodidad (p=0,003). Por su parte, los indicadores referentes al conjunto de actividades diarias también presentan una mejoría significativa (p=0,019) (tabla 3). Por el contrario, no encontramos diferencias significativas en las variables referentes a la movilidad, los autocuidados y la ansiedad (p>0,05) (tabla 3).
Cambios en el EuroQuoL-5D tras seis meses de tratamiento con secukinumab
| EQ-5D, n (%) | Basal | 6 meses | Cambio | p |
|---|---|---|---|---|
| Movilidad | 0,368 | |||
| Nivel 1 | 15 (38,5) | 22 (56,4) | +7 | |
| Nivel 2 | 22 (56,4) | 16 (41,0) | −6 | |
| Nivel 3 | 2 (5,1) | 1 (2,6) | −1 | |
| Autocuidados | 0,185 | |||
| Nivel 1 | 14 (35,9) | 22 (56,4) | +8 | |
| Nivel 2 | 22 (56,4) | 16 (41,0) | -6 | |
| Nivel 3 | 3 (7,7) | 1 (2,6) | −2 | |
| Actividades diarias | 0,019 | |||
| Nivel 1 | 4 (10,3) | 14 (35,9) | +10 | |
| Nivel 2 | 26 (66,7) | 21 (53,9) | −5 | |
| Nivel 3 | 9 (23,1) | 4 (10,3) | −5 | |
| Dolor / incomodidad | 0,003 | |||
| Nivel 1 | 3 (7,7) | 6 (15,4) | +3 | |
| Nivel 2 | 10 (25,7) | 22 (41,0) | +12 | |
| Nivel 3 | 26 (66,7) | 11 (28,2) | −15 | |
| Ansiedad / depresión | 0,134 | |||
| Nivel 1 | 10 (25,6) | 18 (46,2) | +8 | |
| Nivel 2 | 20 (51,3) | 17 (43,6) | −3 | |
| Nivel 3 | 9 (23,1) | 4 (10,3) | −5 | |
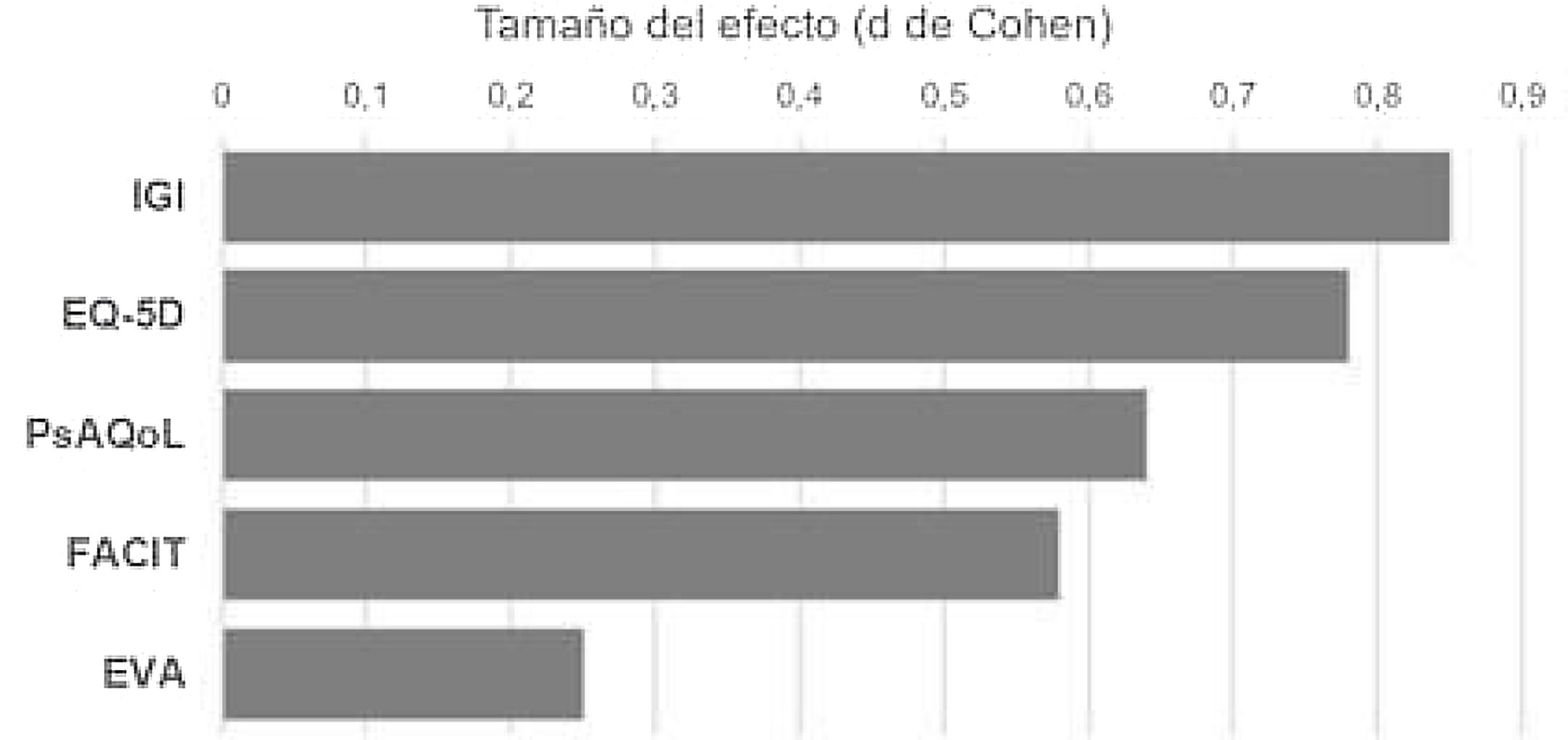
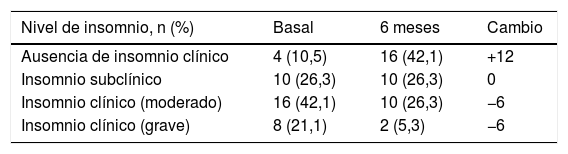
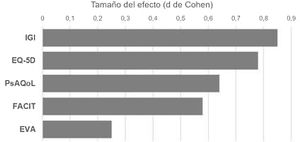
Por último, después de 6meses de terapia con secukinumab se observa un cambio significativo en las variables referentes al insomnio moderado y grave, con una notable reducción en ambos (p=0,006) (tabla 4). Esta es la variable sobre la que mayores diferencias se observan entre el estado basal y tras el tratamiento (fig. 1), seguida de la calidad de vida reportada por el propio paciente.
Cambios en los niveles de insomnio tras los 6 meses de tratamiento
| Nivel de insomnio, n (%) | Basal | 6 meses | Cambio |
|---|---|---|---|
| Ausencia de insomnio clínico | 4 (10,5) | 16 (42,1) | +12 |
| Insomnio subclínico | 10 (26,3) | 10 (26,3) | 0 |
| Insomnio clínico (moderado) | 16 (42,1) | 10 (26,3) | −6 |
| Insomnio clínico (grave) | 8 (21,1) | 2 (5,3) | −6 |
Nivel de significación: p=0,006.
El tratamiento con secukinumab durante el periodo de estudio de 6meses en pacientes con artritis psoriásica y espondiloartritis produjo una mejora notable en todas las variables de efecto del tratamiento sobre las distintas escalas estudiadas, siendo los cambios más notables sobre el sueño, la calidad de vida y la fatiga (fig. 1)18. Esta mejoría generalizada fue reportada tanto en los pacientes sometidos a tratamiento con secukinumab en monoterapia como en tratamiento combinado y tanto en pacientes naïve a tratamiento biológico como a refractarios a terapias biológicas previas. Cada una de las variables reportadas por el paciente fue analizada por medio de cuestionarios validados y con una gran fiabilidad y consistencia internas2,10. Estos datos son de una gran relevancia, puesto que la percepción de un cambio en la salud del propio enfermo es un importante indicador del éxito del tratamiento13,16.
El tratamiento actual para la artritis psoriásica incluye medicamentos antirreumáticos clásicos como el metotrexato19, así como una gran variedad de medicamentos biológicos como los agentes anti-TNF. Sin embargo, muchos de los pacientes no responden ni a los FAME clásicos ni a los antagonistas del TNF, y la mayoría de los que inicialmente responden no logran la remisión completa de la enfermedad20-22. Por lo tanto, sigue habiendo una necesidad insatisfecha para el tratamiento de las espondiloartritis y la necesidad de investigar y desarrollar alternativas a las terapias existentes23. Por esta razón, los resultados obtenidos en nuestro estudio son de una gran relevancia clínica, pues parecen sugerir que la terapia a 6meses con secukinumab (tanto en pacientes que habían recibido terapia anti-TNF previa como aquellos que no habían recibido dicha terapia), además de mejorar los datos objetivos clínicos de respuesta que utilizamos en nuestra práctica clínica habitual, mejora de manera significativa la calidad de vida percibida por los pacientes, así como los síntomas de fatiga, insomnio, dolor y malestar padecidos y referidos por el propio enfermo6,24-26.
Nuestro estudio ha demostrado una clara mejoría en la calidad de vida reportada por el paciente, así como una reducción de los niveles de insomnio, dolor y fatiga tras 6meses de tratamiento con secukinumab. Dado que la artritis psoriásica y la espondiloartritis pueden ser debilitantes en términos de su impacto sobre la calidad de vida del paciente y generar problemas psicosociales, los agentes biológicos como el secukinumab tienen el potencial de reemplazar las terapias actuales debido a las marcadas mejoras en la calidad de vida reportada por el propio paciente27.
Estos resultados son compatibles con los reportados en los estudios pivotales del secukinumab. En concreto, en el estudio Future1 el secukinumab demostró mejorías clínicamente significativas y sostenidas en el tiempo en los distintos medidas de desenlace reportadas por el paciente (PRO) estudiados, incluyendo los parámetros de enfermedad global, dolor, función física y fatiga en sujetos con artritis psoriásica activa18,28,29.
Entre las limitaciones del estudio, que necesitaría comprobaciones adicionales y aumentar la población, está que, si bien hemos diferenciado inicialmente los pacientes en función de la forma axial y periférica (tabla 1), a la hora de analizar los resultados del estudio no hemos podido tener en cuenta estas consideraciones debido al escaso tamaño muestral. Las mismas consideraciones se aplican al criterio monoterapia y terapia combinada. En cualquier caso, del estudio sí se desprende que el empleo de secukinumab mostró eficacia a los 6meses de tratamiento en los dominios clave del estudio, de manera que los pacientes experimentan menos fatiga e insomnio y una mejora global de la calidad de vida30. Adicionalmente, y considerando la cronicidad de la patología y del tratamiento prescrito, se podría valorar la realización a más largo plazo de este tipo de estudios con el objetivo de reevaluar en práctica clínica habitual la persistencia del efecto a corto plazo evidenciado en relación con las distintas medidas de desenlace referidas y reportadas por el paciente.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.