El lupus eritematoso sistémico es una enfermedad reumática sistémica enormemente heterogénea, con múltiples posibles manifestaciones de patogenia diversa, como se ilustra en esta revisión sobre las novedades más relevantes concernientes a esta compleja enfermedad autoinmune. Se revisan aspectos como la patogenia de la anemia crónica asociada al lupus eritematoso sistémico, la estimación del riesgo cardiovascular, el síndrome antifosfolipídico, la predicción del daño acumulado y los avances más recientes en el tratamiento, incluyendo los tolerógenos y las terapias biológicas. También se revisan las contribuciones más relevantes en torno a las terapias clásicas, como la optimización del uso de los glucocorticoides y los antipalúdicos, así como el papel que pueda desempeñar la vitamina D.
Systemic lupus erythematosus is a heterogeneous rheumatic systemic disease with extremely varied clinical manifestations and a diverse pathogenesis, as illustrated in this review on the most relevant new knowledge related to the disease. Topics such as anemia, pathogenesis, cardiovascular risk assessment, antiphospholipid syndrome, prediction of damage and recent advances in treatment, including tolerogenic and biological agents, are discussed. Relevant contributions regarding classical therapies such as corticosteroid and antimalarials and their optimal use, as well as the roll of vitamin D, are also referred.
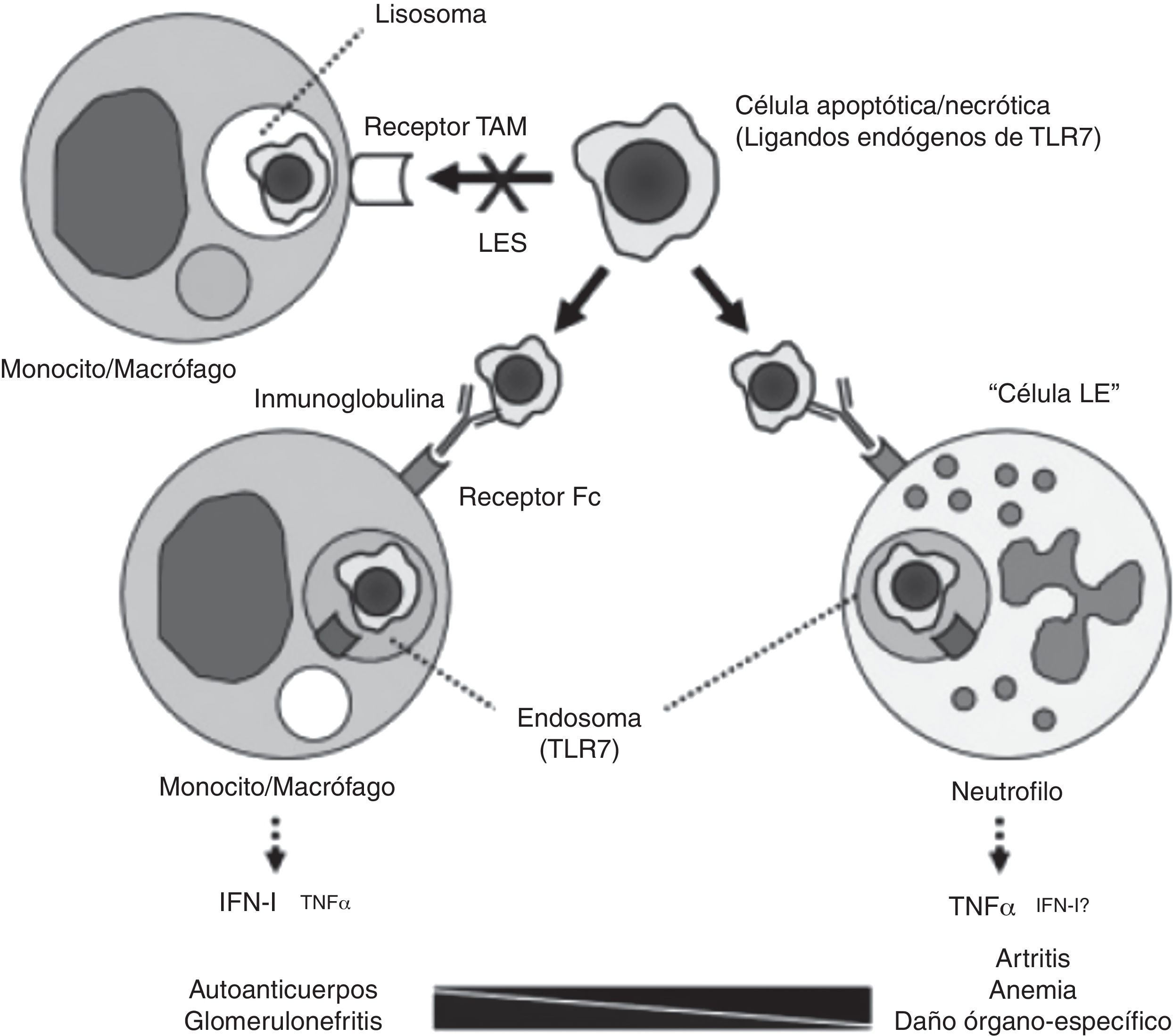
Si algo caracteriza al lupus eritematoso sistémico (LES) es la diversidad. Bajo tan amplia diversidad de manifestaciones clínicas a muy diferentes niveles subyacen diferentes mecanismos patogénicos. Un estudio llevado a cabo en la Universidad de Florida analiza la patogenia de la anemia crónica del LES que, siendo la más frecuente de las anemias del LES, es, sin embargo, la menos conocida1. Los autores revisan retrospectivamente las biopsias de médula ósea de 6 pacientes con LES y encuentran, replicando en su mayor parte hallazgos de estudios previos, una importante diseritropoyesis, con abundantes células «LE» y marcados fenómenos apoptóticos; demuestran también, mediante técnicas inmunohistoquímicas, presencia marcada de TNF y enzimas marcadoras de apoptosis, como es el caso de la caspasa 3 escindida. Los autores testan diferentes hipótesis en modelos murinos knockout de lupus inducido por pristane. Entre otros hallazgos, constataron que las anomalías patológicas mencionadas, que también se desarrollan en el ratón, no precisaban de la intervención del receptor de interferón alfa y, sin embargo, sí era imprescindible la indemnidad de la vía TLR-7/TNF-α. Una excesiva producción de TNF por parte de los neutrófilos parece crítica para el desarrollo de la anemia y también, posiblemente, de la artritis lúpica, tal y como proponen en su modelo explicativo (fig. 1). Este modelo cuestiona el paradigma de la mediación del INF de tipo i en todas las manifestaciones del LES, desempeñando un papel más relevante en aquellas donde la intervención de un autoanticuerpos resulta crítica, como es el caso de la glomerulonefritis lúpica (NL). Las posibles implicaciones terapéuticas de esta diversidad de mecanismos patogénicos resultan obvias. Es preciso señalar que estos pacientes fueron probablemente seleccionados por su gravedad y, por tanto, cabe la posibilidad que no representen a todos los pacientes lúpicos con anemia no hemolítica.
Modelo de patogenia de diferentes manifestaciones del LES. El procesamiento de los cuerpos apoptóticos no se produciría a través de los receptores tipo «TAM» (Tyro3, Axl, Mer), sino que, una vez opsonizados por las inmunoglobulinas, serían reconocidos por los receptores FC de los monocitos/macrófagos o de los neutrófilos, formando endosomas e interaccionando con TLR 7, dando lugar a la transcripción de IFN o TNF, dependiendo de la célula implicada.
Tomado de Zhuang et al.1
Es claro que existe un problema con la valoración individual del nivel de riesgo cardiovascular (RCV) en nuestros pacientes con LES. Los pacientes con LES tienen un RCV mayor que el de la población de similar edad y sexo, y ese exceso de riesgo relativo no se explica solo por un incremento en los factores de riesgo clásicos2. Por tanto, no es de extrañar que los instrumentos basados en los datos de Framingham, como el SCORE, no sean útiles en pacientes con LES, ya que no capturan adecuadamente el nivel de RCV de estos pacientes. El grupo de Bevra Hahn ha llevado a cabo un estudio observacional prospectivo con el propósito de identificar factores predictivos de desarrollo de placa de ateroma carotídeo y/o de su progresión. Incluyeron una serie de biomarcadores con alto sentido patogénico, implicados (de acuerdo con estudios previos) en el desarrollo de ateromatosis en el LES o en población general. Para el análisis, se valen de una herramienta informática poderosa con el objetivo de identificar predictores y puntos de corte de los biomarcadores: el análisis CART o clasificación y árboles de regresión3. Una serie de variables explicativas se asociaron a presencia de placa, con altas OR para niveles de leptina > 34 ng/dl (OR = 7,3; IC del 95%, 2,2-24,0; p=0,001), niveles de TNF-like weak apoptosis inductor (TWEAK) > 373 pg/ml (OR = 28,8; IC del 95%, 2,9-281,1; p=0,004) y HDL proinflamatoria ≥ 0,94 FU (OR = 9,1; IC del 95%, 3,3-24,6; p<0,001). La diabetes mellitus alcanzó una OR marcadamente alta (OR = 61,8; IC del 95%, 6,4-598,1; p<0,001). Los autores construyen un score, que denominan con el acrónimo «PREDICT», cuya capacidad predictiva de placa resultó superior a la de los factores de riesgo clásico en valor predictivo positivo (VPP) (63,5 vs. 53,6), valor predictivo negativo (VPN) (94,4 vs. 74,7) y área bajo curva (0,84 [0,78-0,90] vs. 0,58 [0,49-0,67])4. El estudio no estaba diseñado para predecir eventos y fueron excluidos pacientes en tratamiento con estatinas, limitando la generalización de los resultados. Además, los test para la determinación de varios de estos biomarcadores no están ampliamente disponibles y adolecen de estandarización suficiente como para su aplicación generalizada. En cualquier caso, lo que sí nos enseña este estudio es que es posible mejorar la predicción del RCV en nuestros pacientes con LES y que los biomarcadores, a diferencia de lo que acontece en la población general, probablemente terminen desempeñando un papel clave en los instrumentos de predicción.
Un estudio del grupo SLICC sobre su cohorte prospectiva de inicio ha encontrado un alto porcentaje de síndrome metabólico en pacientes con LES (en torno a un 35%), que se asoció a actividad y daño, así como a la edad y la etnia afroamericana o hispánica. Sin embargo, la aportación real de este hallazgo en la estimación del RCV es dudosa, dado que este conglomerado de factores que define al síndrome metabólico no ha terminado de demostrar ser más que la suma de los factores que lo componen5.
El síndrome antifosfolipídicoRecientemente, se han publicado los resultados a 10 años del Europhospholipid Projet, una cohorte multicéntrica europea constituida inicialmente por 1.000 pacientes con síndrome antifosfolipídico (SAF)6. El objetivo de este estudio observacional y prospectivo era analizar la morbimortalidad del síndrome, estando asociado a LES en un 36,2% de los casos. Solo el 40% de los pacientes permanecieron anticoagulados a lo largo del estudio y 135 no recibieron tratamiento antitrombótico alguno (antiagregante o anticoagulante), de los cuales un 93,3% estaban libres de trombosis a los 10 años, sugiriendo que las decisiones de sus médicos no resultaron del todo desacertadas. Llama la atención el predominio de las trombosis venosas a la entrada en la cohorte, siendo sin embargo predominantes las arteriales al final del período de observación. Los investigadores proponen, como explicación de este hallazgo, la posible mayor eficacia de las medidas antitrombóticas en prevenir la trombosis venosa vs. la arterial. Una explicación alternativa podría ser la dificultad de atribución, ya que un porcentaje importante de pacientes son LES y es conocida la predisposición de estos pacientes a desarrollar arteriosclerosis. En este sentido, no se informa en el artículo de ningún esfuerzo que se haya llevado a cabo para discriminar entre ictus puramente trombótico o arteriosclerótico. Otra limitación del estudio es la no aleatorización de la inclusión, así como el importante porcentaje de pérdidas de seguimiento que, excluyendo las muertes, resultó del 41,9%. La ratio de mortalidad estandarizada fue de 1,8 (IC del 95%, 1,5-2,1), ratio muy similar al que se ha venido comunicando últimamente en las cohortes europeas de LES7. Entre las causas más comunes de muerte, destaca como primera la trombosis: un 36,5% (3% del total). Quizá reflejo de la ya mencionada amplia representación de pacientes con LES en la cohorte, la infección resultó también frecuente como causa de muerte (26,9% de los casos) y, como llamada de atención, un 10,7% de los pacientes que fallecieron lo hicieron a consecuencia de una hemorragia. Claramente, son necesarios más estudios, con una cuidadosa evaluación del binomio riesgo-beneficio, que fundamente mejor las decisiones concernientes a la anticoagulación en el SAF.
Predictores de dañoEl daño acumulado, en su mayoría relacionado con el empleo a largo plazo de los glucocorticoides (GC)8, es un problema clínico mayor en el LES, aún sin buena solución. Varias cohortes han publicado recientemente datos prospectivos buscando predictores de daño y el grupo SLICC ha hecho lo propio en su amplia cohorte de inicio, multicéntrica y multinacional9. El estudio incluyó a 1.502 pacientes, con una media ± desviación estándar de 4,25 ± 2,7 visitas por paciente. Encuentran una serie de factores modificables asociados a progresión del daño, medido con el índice del propio grupo (SDI), como la actividad del LES (SLEDAI-2k), los GC y la hipertensión arterial, replicando resultados de otros estudios. Los autores hacen un especial esfuerzo en intentar eludir la colinealidad entre GC y actividad (esto es: a más actividad, más GC), demostrando un efecto independiente de los GC sobre el daño. En concreto, la relación entre actividad y transición a daño (desde no daño) fue mayor en pacientes sometidos a tratamiento esteroideo: 1,33 (IC del 95%, 1,02 a 1,74). De nuevo aparecen los antipalúdicos como protectores, con el problema habitual de la posible confusión por indicación a LES más leves. Como no podría ser de otro modo, el daño predijo mortalidad, con hazard ratio de 1,46 por punto de SDI. El estudio también aporta una tasa de daño en una cohorte de inicio, de indudable utilidad para la investigación en el futuro. Una debilidad mayor es que se recoge pobremente el efecto de los GC (no se calcula la dosis acumulada ni se menciona la dosis actual de los mismos), cuando la dosis de corticoides actual es un fuerte predictor de daño10.
Los tolerógenos, de nuevo a escenaLa búsqueda de agentes tolerógenos, es decir, de agentes capaces de restaurar la tolerancia frente a autoantígenos nucleares, ha sido, hasta la fecha, tan intensa como infructuosa para el LES. Fármacos inicialmente prometedores, como el edratide o el abetimus, con efectos serológicos favorables, no han conseguido, sin embargo, demostrar beneficios clínicos. La reciente aparición en escena del lupuzor, también llamado regerimod, podría cambiar esta tendencia. Este fármaco, desarrollado por una empresa europea de biotecnología, ImmuPharma, está constituido por un pequeño fragmento de ribonucleoproteína fosforilado en la posición 140 de la serina, lo que parece conferirle marcada capacidad moduladora sobre célula T. Con lupuzor se constata una expansión de los fenotipos reguladores en detrimento de los efectores, algo ya observado en otros agentes tolerógenos precedentes. Algunos efectos imprevistos sobre célula dendrítica, como es la interacción con las HSP-70 (o chaperonas, altamente expresadas en respuestas autoinmunes), pueden ser importantes en su mecanismo de acción, desestabilizando ciertas proteínas, como las moléculas de HLA de clase ii, con la consiguiente interferencia en la presentación antigénica. Sea cual sea su mecanismo de acción, aún no del todo esclarecido, el lupuzor ha mostrado datos prometedores en el ensayo controlado aleatorizado (ECA) fase iib, añadido al tratamiento estándar, con un porcentaje de respondedores SLE responder index (SRI), a las 24 semanas, de hasta el 84,2%, si se aplicaba solo a aquellos pacientes con un SLEDAI clínico (sin parámetros serológicos) ≥ 6. En este ensayo, doble ciego, llama la atención la fuerte respuesta a placebo (superior al 40%), circunstancia que los autores intentan explicar por la liberalización de los resultados favorables del análisis intermedio, que se llevó a cabo a las 12 semanas11. No surgieron alarmas de seguridad destacables y no se constataron efectos sobre las respuestas CD4 a patógenos. A pesar de que los grupos no resultaron bien balanceados tras la aleatorización y de que no se alcanzó el objetivo primario, estos resultados son prometedores y ya están en marcha los ensayos en fase iii, con un fast track (consideración de vía rápida) concedido por la Food and Drug Administration.
Los glucocorticoides en el punto de miraRecientemente, sobre todo en lo que a la NL se refiere, se ha venido cuestionando el papel de los GC, y particularmente de las dosis altas, en controlar la actividad de manifestaciones graves del LES, sobre la base de un balance riesgo/beneficio probablemente desfavorable a medio-largo plazo. Un régimen terapéutico libre de GC diarios, para inducción de remisión y mantenimiento en la NL, referido como «Rituxilup», ha adquirido cierta resonancia en la literatura y en diferentes foros. Esta novedosa propuesta consiste en una combinación de pulsos de metilprednisolona al inicio junto con rituximab y micofenolato, ajustado este último a niveles séricos. Con este protocolo, los autores comunican resultados muy favorables en un estudio observacional con casi 3 años de seguimiento, obteniendo una respuesta completa en un 72% de los tratados y una respuesta parcial o completa en un 92%12. Sin embargo, hasta un 33% presentó una recidiva durante el tiempo de observación. El estudio tiene numerosas limitaciones, entre las que destaca sobrerrepresentación de glomerulonefritis membranosas, que constituyeron nada menos que un 44% de la muestra. Es bien sabido que estos pacientes tienen mejor pronóstico que los afectados de formas proliferativas. Así, en un estudio observacional multicéntrico del grupo de Enfermedades Autoinmunes Sistémicas de la la Sociedad Española de Reumatología (EAS-SER), pudimos constatar que, tras 10 años de seguimiento, solo un 6% de los pacientes con NL membranosa (de un total de 150 pacientes) tenían una enfermedad renal crónica avanzada13. No es la primera vez que se propone un protocolo «sin esteroides» aparentemente exitoso, ya preconizado en otros centros, como el UCL por el grupo de David Isenberg14; pero los datos son demasiado preliminares y el seguimiento demasiado corto como para fundamentar un cambio tan radical.
La vitamina D en pacientes con lupus eritematoso sistémicoA la vitamina D se le atribuyen efectos moduladores a distintos niveles de la respuesta inmunitaria. Sabemos que su déficit se asocia a autorreactividad y que la corrección del mismo favorece la diferenciación del linfocito T a fenotipos reguladores, con disminución, por ejemplo, de las TH1715,16. Dado que la mayoría de las cohortes documentan un déficit de vitamina D en pacientes con LES17, cabría la posibilidad de que una corrección del mismo trajera efectos beneficiosos. Con ese propósito, la cohorte de Johns Hopkins inició un estudio observacional que incluyó a 1.006 de sus pacientes, suplementado a aquellos que se definieron como deficitarios, comprobando, en el análisis a 128 semanas, cambios paralelos de la actividad de la enfermedad (en términos de reducción, medida por PGA o por SELENA-SLEDAI) e incluso de la proteinuria, con el incremento de los niveles de vitamina D, siendo significativos estadísticamente (aunque modestos) en aquellos pacientes que partían de niveles < 40 ng/ml y para cambios en niveles plasmáticos > 20 ng/ml18. Dado que los suplementos de vitamina D podrían ofrecer otros beneficios a los pacientes con LES, como la reducción de incidencia de cáncer colorrectal o efectos favorables sobre el metabolismo óseo, algunos expertos aconsejan suplementar a los pacientes con niveles de vitamina por debajo de 30-40 ng/ml19. En cualquier caso, dado que la seguridad a largo plazo no está del todo establecida y que en ciertos modelos murinos de LES, como el NZW, la vitamina D puede empeorar la nefritis, es claro que necesitamos ensayos clínicos aleatorizados, que confirmen estos probables beneficios, antes de poder recomendar su uso generalizado en pacientes con LES.
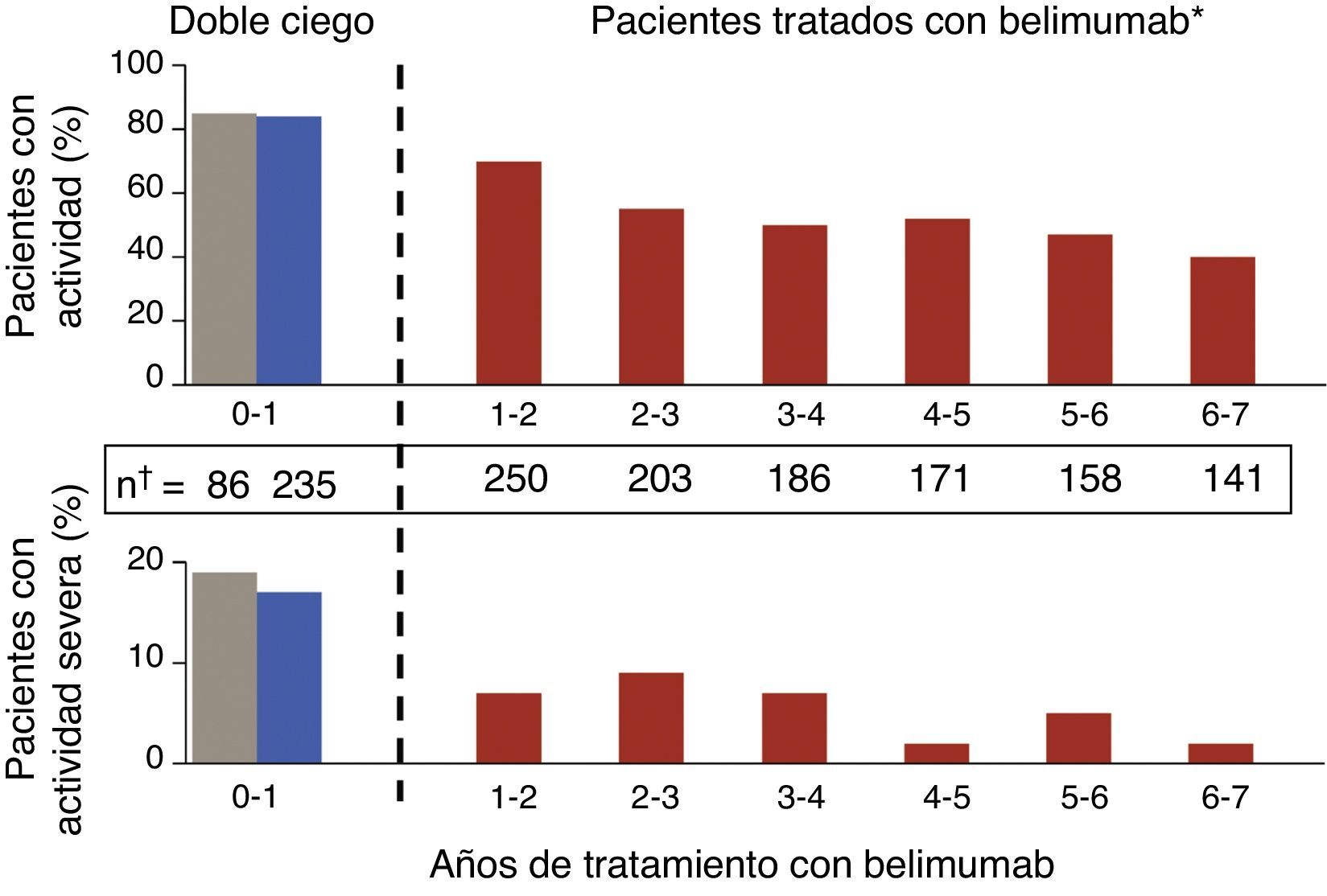
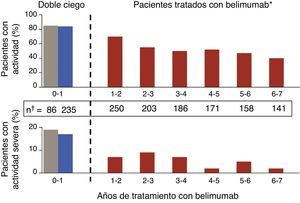
Novedades en terapias biológicasSe han publicado los resultados del estudio de extensión abierto del ensayo clínico en fase ii de belimumab20, con datos de seguimiento de 1.746 pacientes-año. En este estudio, que es el ensayo con un biológico en LES que cuenta con mayor seguimiento hasta la fecha, se incluyó a los pacientes que, a criterio del investigador, eran calificados como respondedores tras una fase abierta de 24 semanas. Se observó que el porcentaje de respondedores SRI se incrementaba discretamente y se produjo una disminución paulatina de los brotes (fig. 2), tanto graves como leves-moderados, medidos por SELENA-SLEDAI flare index (SFI). Además, se constató una disminución de las dosis medias de GC, en torno a un 50%, si bien pocos pacientes fueron capaces de prescindir de los mismos. Una limitación de este estudio es que se enriquece con respondedores; además, dado que la historia natural de la enfermedad supone la tendencia a la disminución de los brotes con el tiempo, resulta difícil extraer conclusiones firmes en lo que a grado de eficacia se refiere. Lo que sí es cierto es que alrededor de un 50% de los pacientes continuaban usando belimumab tras una media de 7 años de seguimiento, una cifra que resiste bien la comparación con la supervivencia de la terapia biológica en patologías reumáticas inflamatorias como la artritis reumatoide. Los datos más consistentes que este tipo de estudios pueden ofrecer son quizás los concernientes a la seguridad y, en este aspecto, los resultados se pueden calificar de buenos. La tasa de efectos adversos anuales permaneció estable, disminuyendo la de infección y, drásticamente tras el primer año, las reacciones infusionales. Solo un pequeño porcentaje desarrolló hipogammaglobulinemia de consideración (de grado iii-iv de 1,1 a 2,6%), sin que se observasen infecciones graves.
Disminución paulatina de los brotes en pacientes tratados con 10mg/kg de belimumab, tanto graves como leves-moderados, a lo largo del estudio de extensión del ensayo clínico fase ii en pacientes con LES.
Tomado de Ginzler et al.20
Otro agente biológico «en rampa de salida» para el LES es el epratuzumab. Se han publicado, por fin (tras una espera inusual, dados los resultados favorables que venían siendo comunicados en los diferentes foros), los datos completos del EMBLEM, un ECA en fase iib con epratuzumab21. Este monoclonal va dirigido contra CD22, una molécula presente en la membrana del linfocito B que guarda una estrecha relación con el B cell receptor, de tal manera que su bloqueo conduce a una regulación a la baja de la señalización generada por el receptor. Se trata de una terapia que también desencadena cierto grado de ablación de células B y modifica la expresión de determinadas moléculas de adhesión, interfiriendo la circulación del linfocito B, entre otros efectos sobre el sistema inmunitario22. EMBLEM es un ECA multicéntrico realizado en pacientes con LES leve o moderado, excluyendo NL o afectación grave del sistema nervioso central, cuyo objetivo era explorar superioridad sobre el tratamiento estándar y buscar la dosis más adecuada. La eficacia fue medida en términos de porcentaje de pacientes que obtuvieron respuesta BICLA, un nuevo índice compuesto, basado sobre fundamentalmente en BILAG y diseñado específicamente para el estudio. A las 24 semanas, el final del estudio, se encontró que existían diferencias favorables al brazo de epratuzumab en varias pero no en todas las dosificaciones. Si estas diferencias se confirman, se trata de un efecto intrigante, ya observado con otros biológicos en el LES, que demanda explicación del porqué con dosis altas se pueden perder los beneficios que se consiguen con dosis menores del fármaco. El programa de desarrollo clínico fase iii, denominado EMBODY, incluye 2 ECA pivotales y se encuentra en fase avanzada, esperando publicar resultados para el primer trimestre del 2015.
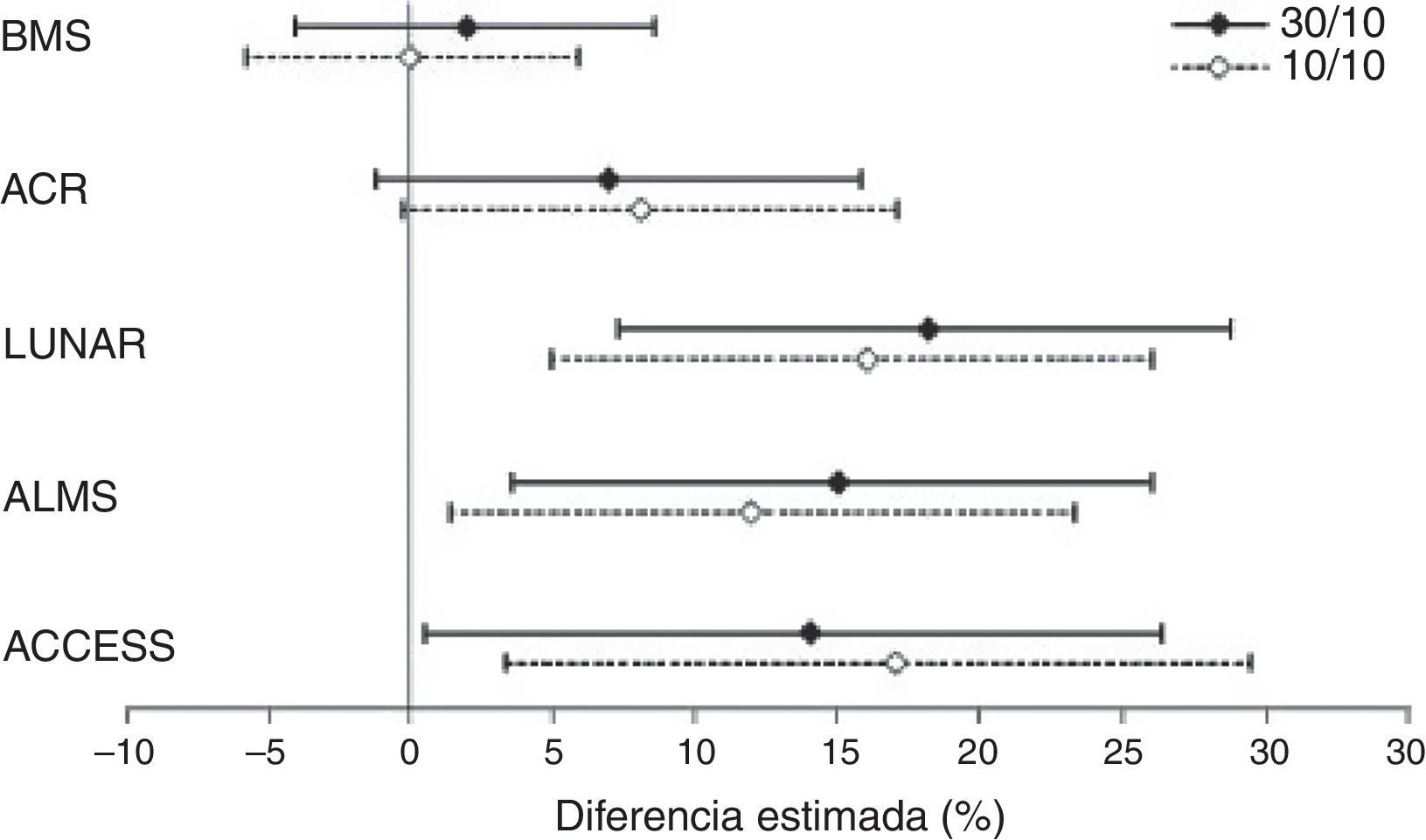
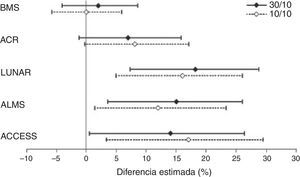
Un estudio con abatacept en NL, de entrada calificable de fallido, merece atención por varias razones, entre otras, porque ilustra las dificultades metodológicas que atañen al diseño de los ECA en el LES y sus implicaciones en la interpretación de los resultados. Este ECA, promovido por Bristol -Myers Squibb, trataba de demostrar la superioridad del abatacept sobre placebo añadido al tratamiento estándar, no consiguiendo el objetivo primario en ninguna de las 2 dosificaciones ensayadas23. Sin embargo, matizando estas conclusiones, Wofsy et al. proponen un ejercicio inteligente de análisis post hoc de los resultados, que consiste en utilizar diferentes índices de respuesta designados para otros ECA (LUNAR, ALMS, etc.) solo en aquellos pacientes que cumplieran los criterios de inclusión del ensayo original para el que fue diseñado el índice. Pues bien, con cualquiera de esos índices de respuesta se observaban diferencias significativas favorables al abatacept (fig. 3). Con el único índice con el que no se consiguió demostrar diferencias fue con el previsto para el estudio, sin duda el más exigente de todos ellos24. Este estudio ejemplifica lo que parece ser un escollo recurrente de muchos de los ECA llevados a cabo hasta la fecha en LES: los instrumentos de medida aparecen como poco sensibles al cambio y puede que nos estén mostrando como similares tratamientos que en realidad no lo son.
Diferencias en tasas de respuesta completa en cada grupo de tratamiento de abatacept, comparadas con tratamiento estándar usando diferentes definiciones de respuesta.
ACCESS: Abatacept and Cyclophosphamide Combination: Efficacy and Safety Study; ACR: recomendaciones del American College of Rheumatology; ALMS: Aspreva Lupus Management Study; LUNAR: Lupus Nephritis Assessment with Rituximab trial.
Tomado de Wofsy et al.24
Con el objetivo de facilitar el análisis crítico de la evidencia y tratar de guiar las decisiones clínicas en este complejo asunto de las terapias biológicas en el LES, la SER ha publicado recientemente un consenso de expertos25. El consenso se llevó a cabo siguiendo una metodología rigurosa de consenso de grupo (RAND-UCLA) e incluyó varias revisiones sistemáticas (algunas de ellas, como la realizada en clinimetría, inéditas), definición de enfermedad refractaria y córtico-dependencia. Además, como no podía ser de otro modo, trata de forma amplia el soporte científico del uso fuera de indicación, tan común en esta enfermedad.
La optimización de los antipalúdicosNadie parece ya dudar de la eficacia de los antipalúdicos en el LES y la necesidad de su uso universal para controlar esta patología, con beneficios potenciales a múltiples niveles26. Con el propósito de contribuir a optimizar su efectividad, el grupo de la doctora Costedoat-Chalumeau se plantea estudiar si una estrategia basada en ajustar la dosis de hidroxicloroquina (HCQ) a los niveles plasmáticos es mejor, en términos de eficacia, que el empleo tradicional de una dosis fija o ajustada a peso corporal27. La hipótesis, atractiva sin duda, se fundamenta en la conocida variabilidad en la absorción de la HCQ28 y en estudios previos del propio grupo, donde consiguieron demostrar una relación estrecha entre actividad y niveles de antipalúdicos29. Emplean una herramienta estandarizada y relativamente validada, para la captura de brote de enfermedad (SFI) pero, desafortunadamente, no encuentran diferencias en incidencia de brotes entre ambas modalidades de uso de la HCQ. La corta duración del ensayo (7 meses), en una población que no fue seleccionada según riesgo de brote, con una acumulación relativamente baja de los mismos, pudo ser una de las explicaciones de este aparente fracaso. En cualquier caso, y dado que la técnica de determinación de los niveles no está ampliamente disponible, por el momento no es aconsejable incluir en el «T2T» del tratamiento del LES el perseguir determinados niveles plasmáticos de HCQ.
Para finalizar, me gustaría disculparme por si no he incluido estudios que, a criterio de otros, han podido ser relevantes y también por el sesgo hacia estudios clínicos con evidente aplicabilidad, algo quizá inevitable dada mi condición de clínico práctico.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesEl Dr Rúa-Figueroa ha actuado como consultor para Lilly y GSK.