Mediante registro multicéntrico ambispectivo de 2.047 pacientes con diversas afecciones reumáticas bajo terapia biológica (TxB), incluyendo un grupo control de pacientes con artritis reumatoide (AR) sin TxB, se reporta la supervivencia en la terapia y eventos adversos asociados a su uso. Los diagnósticos más frecuentes son: AR 79,09%; espondilitis anquilosante (EA) 7,96%; artritis psoriásica (APso) 4,40%; lupus eritematoso sistémico (LES) 3,37% y artritis idiopática juvenil (AIJ) 1,17 por ciento. Un análisis de 1.514 casos de la muestra total reportó que la tasa de incidencia para cualquier evento adverso es de 178/1.000 pacientes-año en TxB vs. 109/1.000 pacientes-año en controles con un riesgo relativo (RR) de 1,6 (IC del 95%, 1,4-1,9); para eventos adversos graves un RR de 15,4 (IC del 95%, 3,7-63,0 p < 0,0001). La supervivencia global de TxB es del 80% a 12 meses, el 61% a 24 meses, el 52% a 36 meses y el 45% a 48 meses. La tasa de mortalidad estandarizada (TME) es de 0,23 (IC del 95%, 0,0-49,0) para TxB vs. 0,00 (IC del 95%, 0,0-0,2) para controles. Se concluye que la TxB se asocia a un mayor riesgo de presentar eventos adversos, especialmente infecciosos, en comparación con pacientes sin TxB. La mortalidad de los pacientes expuestos a TxB no es mayor que la esperada para la población general ajustada a edad y sexo.
This work reports patient treatment survival and adverse events related to Biologic Therapy (BT), identified by a multicenter ambispective registry of 2047 rheumatic patients undergoing BT and including a control group of Rheumatoid Arthritis (RA) patients not using BT. The most common diagnoses were: RA 79.09%, Ankylosing Spondilytis 7.96%, Psoriatic Arthritis 4.40%, Systemic Lupus Erythematosus 3.37%, Juvenile Idiopathic Arthritis 1.17%. A secondary analysis included 1514 cases from the total sample and was performed calculating an incidence rate of any adverse events of 178 × 1000/ BT patients per year vs. 1009 x 1000/control group patients per year with a 1.6 RR (IC95% 1.4-1.9). For serious adverse events the RR was: 15.4 (95% CI 3.7-63.0, P<.0001). Global BT survival was 80% at 12 months, 61% at 24 months, 52% at 36 months and 45% at 48 months. SMR: 0.23 (95%CI 0.0-49.0) for BT vs. 0.00 (95%CI 0.0-0.2) for the control group. In conclusion, BT was associated to a higher infection risk and adverse events, compared to other patients. Mortality using BT was not higher than expected for general population with same gender and age.
Las enfermedades reumáticas afectan a más del 10% de la población general1. En México se ha identificado una alta prevalencia de las principales enfermedades reumáticas: en particular, la prevalencia de artritis reumatoide estimada es del 1,60% (IC del 95%, 1,4-1,7]2; en nuestro medio, son una de las principales demandas de consulta en primer nivel de atención y condicionan un alto costo a los servicios de salud3.
El tratamiento de estas enfermedades es complejo, dado que requiere un manejo multidisciplinario y temprano en el que se deben incluir medidas no farmacológicas, como terapia física, ocupacional y psicológica, así como el tratamiento con fármacos de diferentes mecanismos de acción, como el uso crónico de analgésicos, antiinflamatorios no esteroides (AINE) e inclusive glucocorticoides. La piedra angular del manejo es la instauración temprana de fármacos modificadores de la enfermedad (FARME), tales como el metotrexato, los antimaláricos, la sulfasalazina y leflunomida4,5. Durante la última década se han multiplicado las opciones de los FARME con el desarrollo de nuevos y prometedores fármacos, en particular los agentes biológicos que en general consisten en anticuerpos monoclonales dirigidos a moléculas específicas, como el factor de necrosis tumoral (anti-TNF-α), a receptores de interleucinas (IL-1, IL-6), de linfocitos B y regulador de la coestimulación de células T6 y muchos más en desarrollo.
Numerosos ensayos clínicos han demostrado la eficacia y la seguridad de la terapia biológica7; sin embargo, el seguimiento de estos casos a largo y medio plazo ha sido limitado8. En consecuencia, se ha considerado necesario realizar evaluaciones en escenarios reales para conocer la eficacia y la seguridad de este grupo farmacológico en la práctica clínica; con este fin se han llevado a cabo diferentes registros9,10, la mayoría en países desarrollados; sin embargo, los resultados han sido muy variables, debido a las diferentes metodologías y análisis implementados, además de que se deberían considerar los aspectos demográficos, socioeconómicos y de atención médica particulares de cada sociedad, sobre todo en aquellas con economías emergentes, donde hay diferencias importantes con respecto a la terapia biológica, tales como el costo y acceso de estos medicamentos. Además, el escenario epidemiológico es diferente del reportado en sociedades desarrolladas respecto a un mayor riesgo de infecciones. Por tanto, el objetivo de este reporte es describir los eventos adversos registrados en una cohorte de pacientes mexicanos con enfermedades reumáticas tratadas con fármacos biológicos, así como identificar la tasa de sobrevida de los mismos y las causas de suspensión del tratamiento.
MétodosLa plataforma para el registro de terapia biológica conformada por la Sociedad Española de Reumatología (SER) desde 200011 fue considerada por PANLAR para desarrollar el proyecto Biobadamérica, cuyo principal objetivo es obtener registros locales relacionados con el uso de biológicos en America latina y en el que cada país adopta el registro con las modificaciones pertinentes.
El Colegio Mexicano de Reumatología (CMR) inicio un registro retrospectivo (RECOLBI) en 2007 de casos de pacientes con enfermedades reumáticas tratados con medicamentos biológicos por especialistas en reumatología, y a partir de 2008 se ha utilizado la plataforma de Biobadaser para el registro Biobadamex12,13, en el que también se incluye un grupo control de casos con el diagnóstico de artritis reumatoide (AR), tratados con FARME no biológicos. Esto fue posible debido a los diferentes sistemas de atención médica del país, ya que no todos los servicios tienen cobertura de terapia biológica, como es el caso de algunos hospitales de la Secretaría de Salud, así como a la atención privada, en donde el acceso depende de la compra directa del tratamiento por el paciente.
Los pacientes con cualquier enfermedad reumática que ameritaran el uso de terapia biológica fueron considerados como candidatos a ingresar al registro. El seguimiento mínimo para ser incorporados al registro de cada uno de los pacientes fue de un año a partir de la fecha de inicio del biológico. El protocolo fue autorizado y registrado (2009-785-103) en la Comisión Nacional de Investigación del Instituto Mexicano del Seguro Social.
Los reumatólogos certificados en el país fueron invitados a participar, para incluir en el registro un mínimo de 20 casos y sin límite máximo. Después de un entrenamiento remoto (por vía telefónica o a través de la red Internet) o bien presencial, a cada colaborador se le asignó una clave de acceso; de esta manera, cada especialista registró en línea los casos diagnosticados y tratados con biológicos durante su consulta de rutina (excepto los casos que estaban incluidos en protocolos terapéuticos o que formaban parte de algún ensayo clínico) con al menos un año de seguimiento. Para control de calidad se lleva a cabo una revisión en línea del 100% de los casos y posteriormente se realizó un monitoreo. Cada centro se supervisa localmente; un monitor visita el centro para verificar aleatoriamente una muestra de al menos el 25% de los expedientes. Si se identifica más del 25% de inconsistencias el caso es eliminado del registro.
Evaluación basal: el registro consiste en una plataforma electrónica en la que se ingresan como datos basales las características demográficas: edad, sexo, escolaridad, sistema de atención; parámetros clínicos acerca de la enfermedad: diagnóstico, tiempo de evolución, actividad en los casos de AR (DAS28) y espondilitis anquilosante (BASDAI), comorbilidad, tratamiento previo para la enfermedad reumática y tratamiento concomitante; así como la información relacionada con el fármaco biológico: tipo de fármaco (adalimumab, abatacept, etanercept, infliximab, rituximab), fármacos accesibles en México durante esta fase del registro; se incluye también la fecha del inicio y la descontinuación del tratamiento, así como la causa en caso de descontinuación. Cada paciente acudió a la cita programada con su reumatólogo tratante y fue seguido con una frecuencia individualizada de acuerdo el criterio de cada médico, sin seguir intervalos fijados previamente.
En este estudio se consideró evento adverso a toda reacción nociva o no deseada que se presentara tras la administración de un fármaco, a las dosis habitualmente utilizadas, para prevenir, diagnosticar o tratar una enfermedad, o para modificar cualquier función biológica. Se definió evento adverso grave a todo suceso desfavorable que, independientemente de la dosis, ponga en peligro la vida, precise de ingreso hospitalario o lo prolongue la internación, así como el que produzca una discapacidad persistente o importante, y evento adverso mortal a todo suceso desfavorable que, independientemente de la dosis, tenga desenlace fatal. Se utilizó la nomenclatura del MedDRA (Medical Dictionary for Drug Regulatory Activities) para clasificar cada uno de los eventos adversos.
Durante las evaluaciones de seguimiento se registraron los acontecimientos adversos asociados al uso de terapia biológica y, en caso de ocurrir, los cambios en los esquemas de tratamiento biológico. El seguimiento mínimo del paciente para reportar acontecimientos adversos o cambios en el fármaco biológico fue de un año. Debido a que la temporalidad del registro fue tanto retrospectivo como prospectivo, si un paciente contaba ya con un período de un año desde que se inició el biológico se podía considerar en el análisis, pero si al momento de incluir al paciente aún no cumplía ese intervalo con el tratamiento biológico, el seguimiento del paciente continuó por lo menos durante 12 meses más.
Análisis estadístico: este reporte incluye un primer análisis descriptivo basal de 2.047 pacientes registrados hasta febrero 2011, considerando su información demográfica, características clínicas y del tratamiento. En la segunda fase del análisis se consideraron 1.514 del total de 2.047 casos, que corresponden a los casos ya monitorizados, incluyendo en este un grupo que recibió terapia biológica (n = 1.114) vs. un grupo control de casos con AR tratados con FARME no biológicos (n = 400); analizando con la prueba de la t de Student, ANOVA para variables continua y prueba de la χ2 para variables cualitativas. Esta misma submuestra de 1.514 casos se utilizó para identificar el riesgo de presentar un evento adverso entre el grupo de biológicos vs. el grupo de AR solo tratado con FARME; se calculó la tasa de incidencia de eventos adversos por 100.000 pacientes-años (IC del 95%). Se calcularon las tasas estandarizadas ajustadas por edad y sexo en la población mexicana general. Finalmente, se identificó la sobrevida con el medicamento a través de curvas de Kaplan-Meier, incluyendo los casos tratados con anti-TNF, considerando como variable censada la fecha de descontinuación del biológico (independiente de la causa). El análisis se realizó con el programa estadístico STATA. La significación estadística se asumió con valores de p < 0,05.
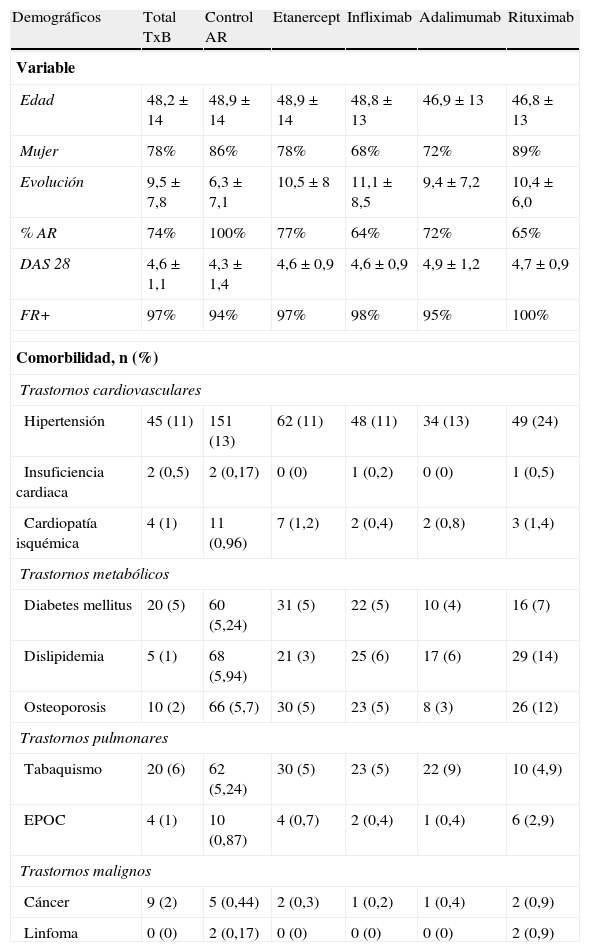
ResultadosEn Biobadamex 1.0 (febrero de 2009-febrero de 2011) participaron 25 centros y 46 reumatólogos; se registró a 2.047 pacientes, con una edad promedio de 49,5 ± 14 años; el 73% del total de los casos corresponde al sexo femenino; la duración media de la enfermedad de 10 ± 8 años. La mayoría son pacientes atendidos en alguno de los sistemas de seguridad social en México (IMSS, ISSSTE, PEMEX, ISSEMYM y Secretaría de Salud). Solo el 9,05% de ellos fueron casos registrados en atención privada. Entre el total de los 2.047 pacientes se registró un total de 2.651 tratamientos, distribuidos de la siguiente manera: 1.916 corresponden a terapia biológica y 735 (27,73%) a casos de AR tratados con FARME no biológicos, considerado como grupo control. Las características demográficas generales y la comorbilidad de la población total y por tratamiento recibido se encuentran en la tabla 1.
Características generales en el Registro Biobadamex 1.0
| Demográficos | Total TxB | Control AR | Etanercept | Infliximab | Adalimumab | Rituximab |
| Variable | ||||||
| Edad | 48,2 ± 14 | 48,9 ± 14 | 48,9 ± 14 | 48,8 ± 13 | 46,9 ± 13 | 46,8 ± 13 |
| Mujer | 78% | 86% | 78% | 68% | 72% | 89% |
| Evolución | 9,5 ± 7,8 | 6,3 ± 7,1 | 10,5 ± 8 | 11,1 ± 8,5 | 9,4 ± 7,2 | 10,4 ± 6,0 |
| % AR | 74% | 100% | 77% | 64% | 72% | 65% |
| DAS 28 | 4,6 ± 1,1 | 4,3 ± 1,4 | 4,6 ± 0,9 | 4,6 ± 0,9 | 4,9 ± 1,2 | 4,7 ± 0,9 |
| FR+ | 97% | 94% | 97% | 98% | 95% | 100% |
| Comorbilidad, n (%) | ||||||
| Trastornos cardiovasculares | ||||||
| Hipertensión | 45 (11) | 151 (13) | 62 (11) | 48 (11) | 34 (13) | 49 (24) |
| Insuficiencia cardiaca | 2 (0,5) | 2 (0,17) | 0 (0) | 1 (0,2) | 0 (0) | 1 (0,5) |
| Cardiopatía isquémica | 4 (1) | 11 (0,96) | 7 (1,2) | 2 (0,4) | 2 (0,8) | 3 (1,4) |
| Trastornos metabólicos | ||||||
| Diabetes mellitus | 20 (5) | 60 (5,24) | 31 (5) | 22 (5) | 10 (4) | 16 (7) |
| Dislipidemia | 5 (1) | 68 (5,94) | 21 (3) | 25 (6) | 17 (6) | 29 (14) |
| Osteoporosis | 10 (2) | 66 (5,7) | 30 (5) | 23 (5) | 8 (3) | 26 (12) |
| Trastornos pulmonares | ||||||
| Tabaquismo | 20 (6) | 62 (5,24) | 30 (5) | 23 (5) | 22 (9) | 10 (4,9) |
| EPOC | 4 (1) | 10 (0,87) | 4 (0,7) | 2 (0,4) | 1 (0,4) | 6 (2,9) |
| Trastornos malignos | ||||||
| Cáncer | 9 (2) | 5 (0,44) | 2 (0,3) | 1 (0,2) | 1 (0,4) | 2 (0,9) |
| Linfoma | 0 (0) | 2 (0,17) | 0 (0) | 0 (0) | 0 (0) | 2 (0,9) |
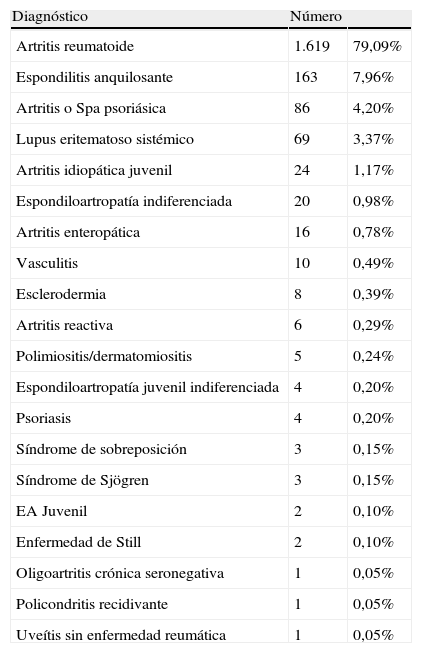
El diagnóstico más frecuente fue AR (79%) seguido por espondiloartropatías seronegativas (14,4%), incluyendo en estas las siguientes entidades: espondilitis anquilosante, artritis psoriásica, espondiloartropatía indiferenciada, artritis enteropática, espondiloartropatía de inicio juvenil y oligoartritis crónica seronegativa; los demás diagnósticos tratados con terapia biológica se enumeran en la tabla 2.
Diagnósticos de los pacientes del registro Biobadamex 1.0
| Diagnóstico | Número | |
| Artritis reumatoide | 1.619 | 79,09% |
| Espondilitis anquilosante | 163 | 7,96% |
| Artritis o Spa psoriásica | 86 | 4,20% |
| Lupus eritematoso sistémico | 69 | 3,37% |
| Artritis idiopática juvenil | 24 | 1,17% |
| Espondiloartropatía indiferenciada | 20 | 0,98% |
| Artritis enteropática | 16 | 0,78% |
| Vasculitis | 10 | 0,49% |
| Esclerodermia | 8 | 0,39% |
| Artritis reactiva | 6 | 0,29% |
| Polimiositis/dermatomiositis | 5 | 0,24% |
| Espondiloartropatía juvenil indiferenciada | 4 | 0,20% |
| Psoriasis | 4 | 0,20% |
| Síndrome de sobreposición | 3 | 0,15% |
| Síndrome de Sjögren | 3 | 0,15% |
| EA Juvenil | 2 | 0,10% |
| Enfermedad de Still | 2 | 0,10% |
| Oligoartritis crónica seronegativa | 1 | 0,05% |
| Policondritis recidivante | 1 | 0,05% |
| Uveítis sin enfermedad reumática | 1 | 0,05% |
El tratamiento registrado en el momento de iniciar la terapia biológica fue: el 77,29% metotrexato y el 42,29% glucocorticoides, seguidos por antimaláricos, el 26,59%, leflunomida, el 21,65%, la sulfasalazina, el 21,65%, y en menos del 5% de los casos azatioprina, ciclofosfamida, mesalazina y ciclosporina. El 40,36% de los pacientes reportó la presencia de comorbilidad, siendo las más frecuentes: la hipertensión arterial sistémica, 14,95% (n = 306); diabetes, 5,81% (n = 119); osteoporosis, 5,32% (n = 109), y tabaquismo, 5,18% (106). Además del FARME, los tratamientos concomitantes más frecuentemente registrados fueron: AINE 39,62% (n = 437), ácido fólico 31,82% (n = 351), paracetamol 7,89% (n = 87), omeprazol 6,89% (n = 76); otros medicamentos como calcio, vitamina D, bifosfonatos, antidiabéticos orales y antidepresivos se reportaron en menos del 3% de los casos.
Los fármacos biológicos más utilizados para el manejo de la enfermedad reumática en el registro Mexicano son los anti-TNF-α (60%), con la siguiente distribución: etanercept 25,61% (679) de los tratamientos, infliximab en el 19,80% (525) y adalimumab en el 14,56% (386). Otros agentes biológicos fueron el rituximab 10,60% (281) y abatacept 1,20% (34).
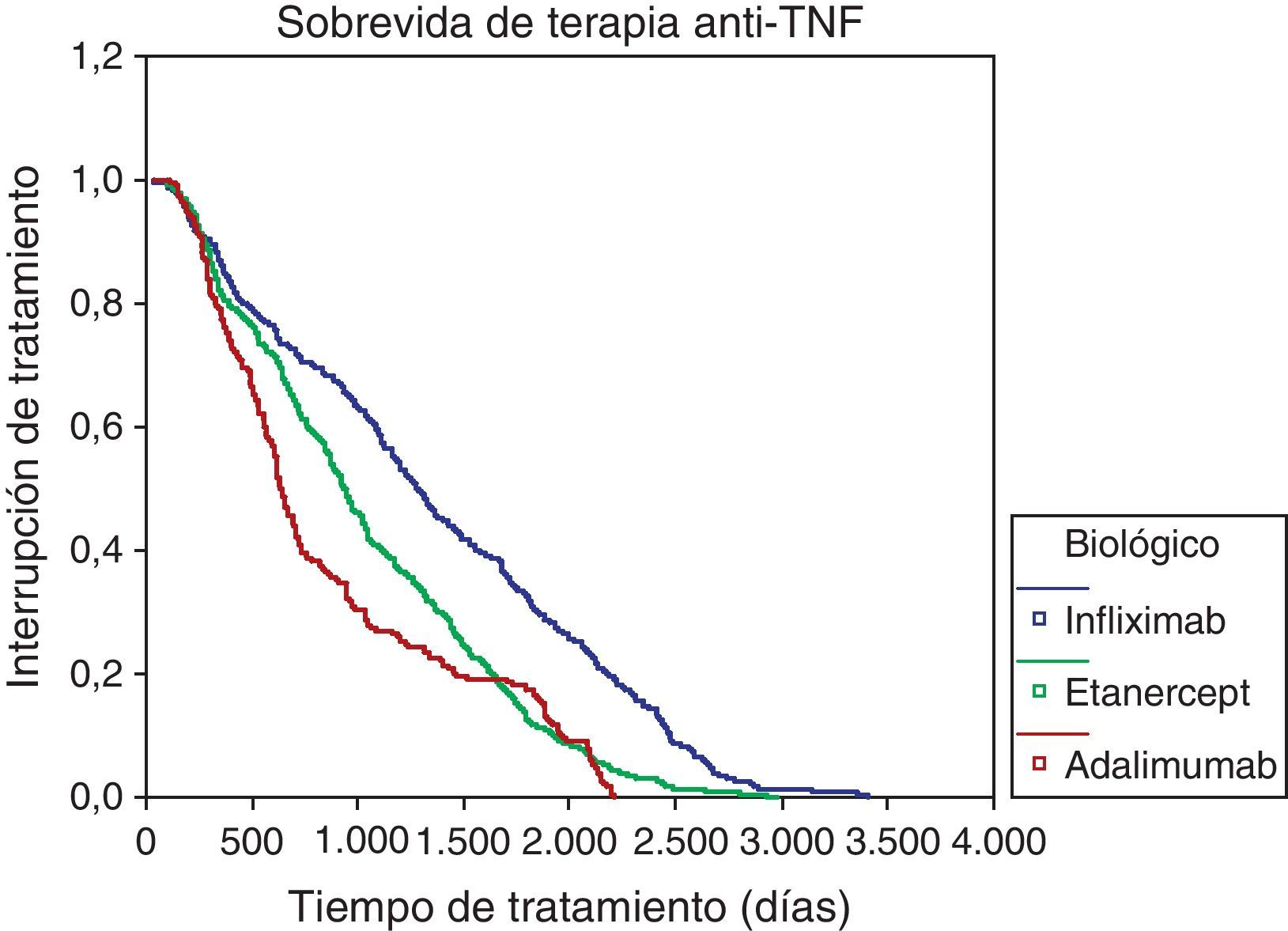
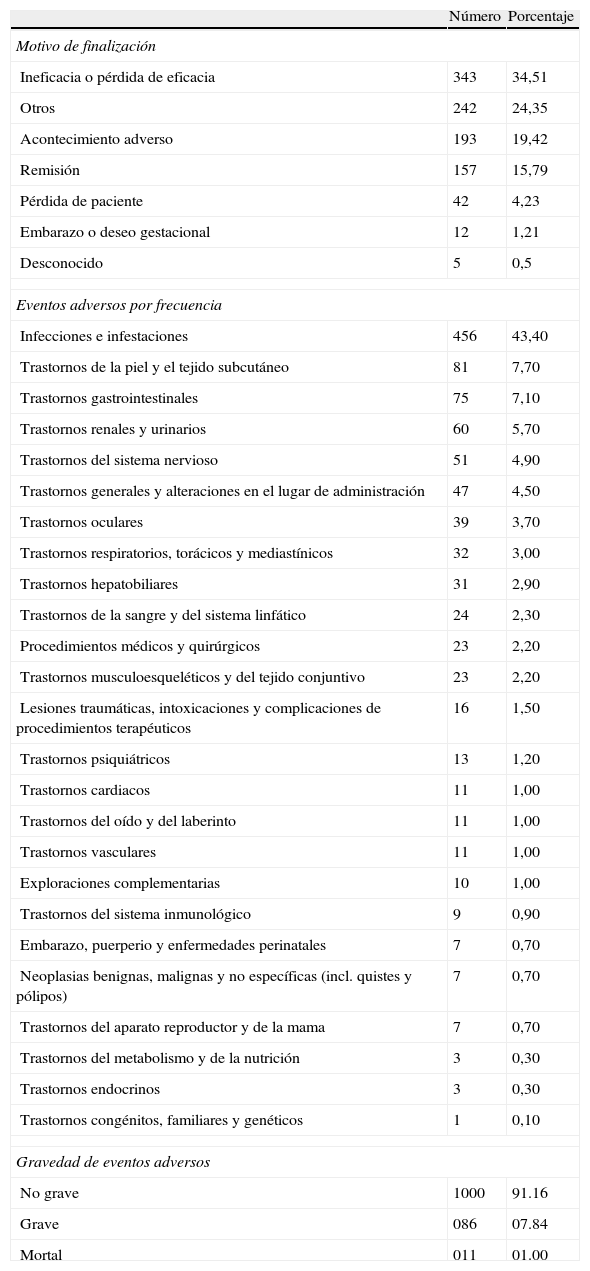
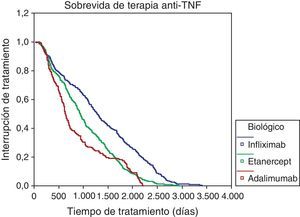
El porcentaje de supervivencia en la terapia biológica de manera global a 12 meses de su inicio fue del 80%, a 24 meses del 61%, a 36 meses del 52% y a 48 meses del 45%. Las causas de descontinuación de anti-TNF-α más frecuentes fueron: falta de eficacia (56%), eventos adversos (5%). La figura 1 muestra las curvas de sobrevida de los 3 anti-TNF-α y en la tabla 3 se presentan las causas de descontinuación de todos los fármacos biológicos, siendo ineficacia o pérdida de la eficacia el 34,51% (n = 343) y eventos adversos el 24,35% (n = 242) las más frecuentes.
Causas de descontinuación de la terapia biológica
| Número | Porcentaje | |
| Motivo de finalización | ||
| Ineficacia o pérdida de eficacia | 343 | 34,51 |
| Otros | 242 | 24,35 |
| Acontecimiento adverso | 193 | 19,42 |
| Remisión | 157 | 15,79 |
| Pérdida de paciente | 42 | 4,23 |
| Embarazo o deseo gestacional | 12 | 1,21 |
| Desconocido | 5 | 0,5 |
| Eventos adversos por frecuencia | ||
| Infecciones e infestaciones | 456 | 43,40 |
| Trastornos de la piel y el tejido subcutáneo | 81 | 7,70 |
| Trastornos gastrointestinales | 75 | 7,10 |
| Trastornos renales y urinarios | 60 | 5,70 |
| Trastornos del sistema nervioso | 51 | 4,90 |
| Trastornos generales y alteraciones en el lugar de administración | 47 | 4,50 |
| Trastornos oculares | 39 | 3,70 |
| Trastornos respiratorios, torácicos y mediastínicos | 32 | 3,00 |
| Trastornos hepatobiliares | 31 | 2,90 |
| Trastornos de la sangre y del sistema linfático | 24 | 2,30 |
| Procedimientos médicos y quirúrgicos | 23 | 2,20 |
| Trastornos musculoesqueléticos y del tejido conjuntivo | 23 | 2,20 |
| Lesiones traumáticas, intoxicaciones y complicaciones de procedimientos terapéuticos | 16 | 1,50 |
| Trastornos psiquiátricos | 13 | 1,20 |
| Trastornos cardiacos | 11 | 1,00 |
| Trastornos del oído y del laberinto | 11 | 1,00 |
| Trastornos vasculares | 11 | 1,00 |
| Exploraciones complementarias | 10 | 1,00 |
| Trastornos del sistema inmunológico | 9 | 0,90 |
| Embarazo, puerperio y enfermedades perinatales | 7 | 0,70 |
| Neoplasias benignas, malignas y no específicas (incl. quistes y pólipos) | 7 | 0,70 |
| Trastornos del aparato reproductor y de la mama | 7 | 0,70 |
| Trastornos del metabolismo y de la nutrición | 3 | 0,30 |
| Trastornos endocrinos | 3 | 0,30 |
| Trastornos congénitos, familiares y genéticos | 1 | 0,10 |
| Gravedad de eventos adversos | ||
| No grave | 1000 | 91.16 |
| Grave | 086 | 07.84 |
| Mortal | 011 | 01.00 |
Las 11 defunciones reportadas en la tabla corresponden a las registradas en el total de pacientes (2.047). En el subgrupo analizado de 1.514 casos se registraron 6 defunciones.
Durante el seguimiento de los pacientes, se registró un total de 1.097 eventos adversos entre los 2.651 tratamientos totales. De acuerdo con la terminología MedDRA, el 91,16% de ellos fueron no graves, el 7,84% fueron graves y el 1,00%, muerte. Los más frecuentes entre todos los tratamientos registrados fueron: infecciones e infestaciones el 43,40%, trastornos gastrointestinales el 7,10%, trastornos de la piel y el tejido subcutáneo el 7,70% y trastornos del sistema nervioso el 4,90%. La lista con la frecuencia de acontecimientos adversos según el tipo de órgano o sistema afectado, así como la frecuencia de acontecimientos adversos fatales, se presenta en la tabla 3.
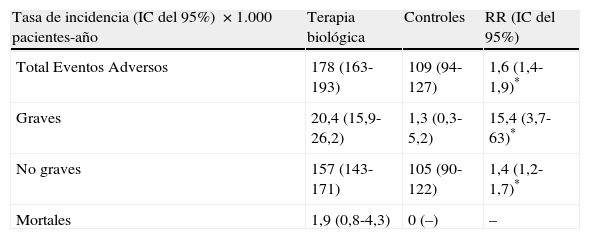
De los 2.047 casos totales, se incluyeron en la segunda parte del análisis 1.514 casos (1,114 con terapias biológicas vs. 400 controles) para calcular la tasa de incidencia y el riesgo relativo de eventos adversos. La tasa para cualquier evento adverso fue de 178/1.000 pacientes-año en el grupo de biológicos vs. 109/1.000 pacientes-año en el grupo control; para los eventos adversos graves fue de 20/1.000 pacientes-año vs. 1.3/1.000 pacientes-año y para los eventos mortales fue de 1.9/1.000 pacientes-año vs. 0/1.000 pacientes-año. La exposición a cualquier tratamiento biológico se asoció a un incremento en el riesgo de presentar eventos adversos de cualquier índole (RR 1.6 [IC del 95%, 1,4-1,9, p < 0,0001]). El riesgo asociado al uso de fármacos biológicos se incrementó notablemente al analizar únicamente los eventos adversos graves (RR 15,4 [IC del 95%, 3,7-63,0; p < 0,0001). Debido a que no se presentó ningún evento adverso mortal en el grupo control no fue posible calcular el RR (tabla 4).
Riesgo relativo de eventos adversos según gravedad
| Tasa de incidencia (IC del 95%) ×1.000 pacientes-año | Terapia biológica | Controles | RR (IC del 95%) |
| Total Eventos Adversos | 178 (163-193) | 109 (94-127) | 1,6 (1,4-1,9)* |
| Graves | 20,4 (15,9-26,2) | 1,3 (0,3-5,2) | 15,4 (3,7-63)* |
| No graves | 157 (143-171) | 105 (90-122) | 1,4 (1,2-1,7)* |
| Mortales | 1,9 (0,8-4,3) | 0 (–) | – |
* < 0.001.
Respecto de los principales eventos adversos de acuerdo con el MedDRA, se observó un incremento en el riesgo para infecciones e infestaciones (RR 2,05; IC del 95%, 1,5-2,7; p < 0,0001); en el 71,96% el germen no fue identificado y se registraron 8 casos de tuberculosis. Los riesgos para otros eventos adversos: trastornos generales y alteraciones en el lugar de administración (RR 5,5; IC del 95%, 1,7-18,0; p < 0,001), trastornos respiratorios, torácicos y de mediastino (RR 4,9; IC del 95%, 1,5-21,0; p < 0,05), trastornos del SNC (RR 3,3; IC del 95%, 1,4-7,9; p < 0,0001) y para procedimientos quirúrgicos (RR 15,4; IC del 95%, 3,7-63,0; p < 0,0001), pero no para el resto de eventos. El único evento se encontró un RR menor en pacientes con biológico en comparación con el grupo control fue para procedimientos quirúrgicos (RR 0,2; IC del 95%, 0,0-0,6; p < 0,01).
Se reportaron 11 defunciones entre el total de pacientes registrados (2047), pero la tasa de mortalidad estandarizada fue calculada con los 1.514 casos, en donde se reportaron 6 defunciones, con un seguimiento total de 3.063 personas/año; durante este (todos habían recibido terapia biológicas vs. 0 en el grupo control), de acuerdo con los datos oficiales emitidos por el Instituto Nacional de Estadística Geografía e Informática (INEGI) respecto de la mortalidad total para la población general, se tenía un estimado de 26 casos de defunciones, con una tasa de mortalidad estandarizada de 0,23 (IC del 95%, 0,0-49) vs. 0,00 (IC del 95%, 0,00-0,24) en el grupo control.
DiscusiónNumerosas publicaciones han reportado los efectos a largo plazo y la seguridad de terapia biológica, en particular los anti-TNF-α8,11,14–16. La mayoría reitera la eficacia de estos y el potencial que tienen para modificar el curso de la enfermedad, lo cual favorece una mejor calidad de vida. Por el otro lado, se reportan resultados de registros que incluyen miles de casos que, si bien indican en términos generales un buen perfil de seguridad, también ponen en evidencia un mayor riesgo de eventos adversos, principalmente infecciosos9,11,18. La mayoría de estos registros se han llevado a cabo en países desarrollados y con población anglosajona; solo recientemente se han publicado los resultados de un estudio brasileño (Biobadabrasil)19 y ahora presentamos nuestros resultados de México.
En este registro multicéntrico observacional en el que se analizaron los datos de 2.047 pacientes mexicanos tratados con fármacos biológicos, se encontró un alto porcentaje de retención en el tratamiento con anti-TNF-α (el 80% en un año y hasta el 45% a los 48 meses). Al comparar las tasas de retención con las reportadas a uno y 3 años por grupos europeos como Italia, el 78,8 y el 70%16, España, el 83 y el 70%17, y Suecia, que a los 20 meses reporta que el 79% persiste con terapia anti-TNF-α también se observa una sobrevida mayor al 75%. El registro brasileño reporta 750 casos tratados con anti-TNF e identifica qué pacientes con AR son los que permanecen más bajo el tratamiento y reportan una tasa de retención global del 60% a 4 años19. También las causas de descontinuación son similares a lo reportado en estas series, que en nuestra población fue del 56% por falta de eficacia y por eventos adversos el 5%.
En cuanto a eventos adversos los resultados al analizar un subgrupo de la muestra total versus el grupo de pacientes con AR tratados sin terapia biológica, se encontró una tasa de eventos adversos de 178 vs. 109/1.000 pacientes-año entre el grupo de biológicos vs. controles y un mayor riesgo de presentar eventos adversos; los más comúnmente registrados fueron infecciones, trastornos gastrointestinales, de la piel, tejido subcutáneo, del sistema nervioso y alteraciones en el sitio de la administración.
Lacaille20 reportó el riesgo relativo de infecciones en una cohorte paciente con AR manejados con FARME no biológicos y con seguimiento de 162.710 personas-año (RR de 0.90; IC del 95%, 0,88-0,93), que se incrementa con el uso de glucocorticoides a 0,92, IC del 95%, 0,85-1,0. En el registro Biobadamex, el RR calculado fue de 2,0 (IC del 95%, 1,5-2,7 [p < 0,0001]), significativamente mayor y de acuerdo con otros registros como Biobadaser21,22, que también han reportado mayores tasas de incidencia de infecciones (114/2.644 pacientes-año entre los pacientes con terapias biológicas versus 63/2.269 pacientes-años del grupo control); sin embargo, estas incidencias no se impactan en desenlaces como mortalidad23, si bien hay en nuestra población un riesgo mayor de presentar eventos infecciosos entre los pacientes que reciben terapia biológica, esta no es mayor a la reportada en series de países desarrollados a pesar de que en nuestro medio existe un riesgo epidemiológico mayor para procesos infecciosos, lo que respalda el perfil de seguridad para utilizar estos medicamentos con nuestros pacientes. En particular, los episodios de tuberculosis no son más frecuentes en nuestro medio, apoyando los reportes españoles que señalan que el control de los potenciales factores de riesgo es fundamental en la limitación de este evento adverso21. Conocedores de la alta prevalencia de tuberculosis en nuestro medio, los especialistas parecen ser cautelosos y apegarse a las recomendaciones para descartar, antes de utilizar un anti-TNF-α, una posible tuberculosis inactiva e inclusive asociar una terapia profiláctica22.
Adebajo y Furst24 sugieren hacer consideraciones especiales en el manejo de biológicos en sociedades con economías emergentes, como sería llevar a cabo registros específicos, interpretación correcta de eventos adversos, establecer adecuadas medidas de desenlace, tomando en cuenta el entorno epidemiológico en cuanto a riesgo de infecciones, así como los costos locales y los diferentes sistemas de salud que determinaran el acceso de la terapia biológica.
Los autores de este reporte identifican ciertas limitaciones de este registro: la primera es la necesidad de ampliarlo, ya que si bien se cuenta con un número suficiente para llevar a cabo un análisis con significación, se requiere incluir un número mayor de casos para contar con representatividad de todas las regiones del país; en este caso, la mayoría de los pacientes son del Instituto Mexicano de Seguro Social, así como de la región central (DF y área conurbana), y también considerar la inclusión de pacientes que no están siendo manejados por reumatólogos. Así, tener una muestra representativa servirá para identificar con mejor precisión el riego de infecciones como tuberculosis que en este análisis no parece ser mayor de lo esperado; otro factor importante es la dificultad para el seguimiento, es importante fomentar la cultura de fármaco-vigilancia en nuestra práctica rutinaria, para generar información importante, así como para incluir medidas de desenlace más concretas y también desde la perspectiva del paciente25, como sería estado de salud y mediciones de productividad laboral, con las que se pueda evaluar la verdadera efectividad de esta costosa terapia. Estas limitaciones pueden estar en parte debidas al diseño de cohorte del registro.
Este es el primer reporte en México que concentra un número suficiente para conocer las características de los pacientes con enfermedades reumáticas tratados con terapia biológica. Biobadamex es ejemplo de algunas de las consideraciones propuestas por Adebajo24 porque es un registro específico en nuestro país, resultado de un esfuerzo interinstitucional coordinado por el Colegio Mexicano de Reumatología y con el que se pretende obtener información fundamental a nivel nacional (de la que se carecía) y que será aplicable a múltiples niveles: desde la atención médica para decisiones clínicas hasta niveles institucionales y sociales para considerar decisiones administrativas y en políticas de salud, inclusive valiosa para la industria farmacéutica y las sociedades de pacientes.
FinanciaciónEl Colegio Mexicano de Reumatología agradece a Bristol-Meyer Squibb, Pfizer, Roche, Schering-Plough (ahora Janssen-Cilag) y UCB, por el financiamiento irrestricto brindado al proyecto, el cual se desarrolló con este apoyo y recursos propios del Colegio.
Conflicto de interesesLos autores de este manuscrito, así como los colaboradores que aparecen en el anexo 1 de coautores, declaran no tener conflicto de intereses.
| Salvador Salinas Saldivar | Guadalupe Aguilar Roca |
| Silvia Sánchez Alonso | Natasha Castro Lizano |
| Aida Galicia López | Angélica Peña Ayala |
| María del Carmen Sahagún Godínez | Ana Guilaisne Benard Medina |
| Jose Eduardo Navarro Zarza | Adolfo García González |
| Everardo Alvarez Hernández | Julio Cesar Casasola Vargas |
| Jesús Espinosa Villalpando | Juan Manuel Miranda Limón |
| Mario Pérez Cristóbal | Yeremi Díaz González |
| Gerardo Bori Segura | Brenda Roxana Vázquez |
| Ricardo Solórzano Acosta | Leonardo Limón Camacho |
| Claudia Irene Meléndez Mercado | Iliana Gabriela Holguín Dorador |
| Gustavo Esteban Lugo Zamudio | Virginia Alvarado Romano |
| Aleni Alieta Paz Viscarra | Ana Marcela Pizaña Serna |
| Carolina Duarte Salazar | María de los Angeles Díaz Ceballos |
| Leobardo Terán Estrada | Jorge Alberto Barragán Garfías |
| Ana Laura Marines Castillo | Mario Alfredo Chavez López |
| Francisco Antonio Rojo Leyva | Iván Francisco Chavira Ruiz |
| Rosa Elda Barbosa Cobos | Ana Sofía Vargas |
| Luis Javier Cruz Alvárez | Zully Castro Colín |
| Claudia Mendoza Pinto | Antonio Rodríguez Aguirre |