Estudiar la frecuencia de toxicidad retiniana y factores de riesgo asociados en una cohorte de pacientes tratados con antipalúdicos de un hospital comarcal.
Material y métodosEstudio retrospectivo de 40 pacientes. Se recogieron: tipo de antipalúdico, dosis diaria y acumulada, enfermedad reumatológica de base, enfermedad concomitante y estudio oftalmológico. Se definió toxicidad retiniana como alteración en 2 de las 4 siguientes pruebas: examen de fondo de ojo, campo visual con patrón macular, tomografía de coherencia óptica de dominio espectral y electrorretinografía de campo completo.
ResultadosLa frecuencia de toxicidad retiniana fue del 13,1% (intervalo de confianza [IC] del 95%, 5-21%), con tendencia a un mayor riesgo en los pacientes en tratamiento con cloroquina (CQ). En estos pacientes con toxicidad retiniana, la dosis media acumulada de CQ fue de 229g y la de hidroxicloroquina (HCQ) de 111g. La dosis media diaria de CQ fue de 250mg y la de HCQ fue de 333mg. Encontramos una asociación positiva entre toxicidad retiniana e hipertensión arterial.
ConclusionesLa frecuencia de toxicidad retiniana, valorada objetivamente mediante técnicas oftalmológicas, fue alta, con una mayor tendencia en pacientes en tratamiento con cloroquina.
To study the frequency of retinal toxicity and associated risk factors in a cohort of patients treated with antimalarials and seen at a tertiary level hospital.
Material and methodsRetrospective study of 40 patients treated with antimalarials, who were referred to ophthalmology for the study of retinal toxicity during 2011. Data collection included type of antimalarial prescribed, daily and cumulative doses, presence of rheumatic disease, corticosteroid use, associated diseases and ophthalmologic examination. Retinal toxicity was confirmed if two of the following tests were altered: fundus examination, visual field with a macular pattern, changes in spectral domain optical coherence tomography and full-field electroretinography.
ResultsToxic retinopathy was detected in 13.1% of patients (95% confidence interval 5-21%) and a trend for a higher risk was observed in case of chloroquine (CQ) treatment. Among the patients with retinopathy, the mean cumulative dose was 229g for CQ and 111g for Hydroxychloroquine (HCQ), and the mean daily dose of CQ was 250mg and 333mg for HCQ. Arterial hypertension had a statistically significant effect on retinopathy development.
ConclusionsToxic retinopathy defined by ophthalmological evaluation was detected in 13.1% of patients. A trend for a higher risk was observed in case of chloroquine treatment.
En 1959 Hobbs informó por primera vez de toxicidad retiniana debido a la utilización a largo plazo de cloroquina (CQ)1. En la actualidad, el sulfato de hidroxicloroquina (HCQ) es el agente antipalúdico más utilizado en el tratamiento de enfermedades autoinmunitarias por su menor incidencia de reacciones adversas, aunque al igual que la CQ puede producir toxicidad ocular por depósito corneal y retiniano. La afectación retiniana produce alteraciones irreversibles de la visión y el paciente puede no percibir su presencia de forma temprana, por lo que se recomiendan revisiones oftalmológicas periódicas.
Debido a la diferencia encontrada en los distintos estudios y a su uso frecuente en Reumatología, realizamos este estudio para analizar la frecuencia de toxicidad retiniana e identificar los factores de riesgo asociados en los pacientes tratados con antipalúdicos en una consulta de Reumatología.
MétodosPacientesSe realizó un estudio retrospectivo de 40 pacientes tratados con antipalúdicos (CQ e HCQ) en la consulta de Reumatología y que fueron remitidos a consulta de Oftalmología durante el año 2011 de manera sistemática tras un año de tratamiento para descartar toxicidad ocular.
Los criterios de inclusión fueron: pacientes mayores de 18 años, tratamiento actual con antipalúdicos por enfermedad reumatológica y con estudio oftalmológico durante el año 2011. Se excluyó a 2 pacientes con afección retiniana previa (uno con drusas duras y otro con seudoagujero macular), por lo que la muestra analizada fue de 38 pacientes.
Todos los pacientes firmaron el consentimiento informado y el estudio se realizó de acuerdo con la Declaración de Helsinki.
Mediciones y recogida de datosLa variable principal fue la toxicidad retiniana definida como daño secundario al fármaco, detectada mediante alteración en al menos 2 de las siguientes pruebas: examen de fondo de ojo, campo visual con patrón macular, tomografía de coherencia óptica de dominio espectral (SD-OCT) y electrorretinografía de campo completo o Full-field (ERG), siguiendo las recomendaciones de la Academia Americana de Oftalmología publicadas en 20112.
A todos los pacientes se les valoró la agudeza visual de ambos ojos y se les realizaron un examen con lámpara de hendidura, un examen de fondo de ojo bajo dilatación y una tomografía de coherencia óptica. A aquellos pacientes con sospecha de toxicidad por antipalúdicos mediante fondo de ojo y/o SD-OCT se les realizó un campo visual usando patrón macular abarcando los 10° centrales y ERG.
Como variables secundarias se consideraron: tipo de antipalúdico, dosis diaria y acumulada de CQ e HCQ, duración del tratamiento y función renal mediante determinación sérica de creatinina.
AnálisisEl análisis de la asociación entre toxicidad retiniana y uso de antipalúdicos se evaluó mediante el test estadístico de la chi al cuadrado para variables cualitativas y la prueba de la t de Student para variables cuantitativas, con un intervalo de confianza (IC) del 95%. El subanálisis de los pacientes con toxicidad retiniana se realizó mediante el test estadístico exacto de Fisher. El análisis estadístico se llevó a cabo con el programa SPSS versión 15.0 (Chicago). Se consideraron estadísticamente significativos valores p < 0,05.
ResultadosLas características sociodemográficas de los pacientes se exponen en la tabla 1. El 81,6% de los pacientes recibían tratamiento con HCQ, dosis media diaria de 254mg y dosis media acumulada ± desviación estándar 251,3 ± 182,2 g. La dosis media diaria de CQ fue de 250mg y la dosis media acumulada fue de 371,5 ± 377,2 g. La duración media del tratamiento 3,17 ± 2,5 años. En todos los casos las cifras de creatinina fueron normales.
Características basales de los pacientes
| Muestra total | Toxicidad retiniana | |
| n | 38 | 5 |
| Edad media (años ± DE) | 53,2 ± 14,1 | 5,0 ± 10,5 |
| Sexo, n (%) | Mujeres, 31 (81,6) | Mujeres, 5 (100) |
| N.° tratamientos con hidroxicloroquina (%) | 31 (81,6) | 2 (40) |
| Dosis diaria media de cloroquina (mg) | 250 | 250 |
| Dosis media acumulada de cloroquina (g) | 371,6 ± 377,2 | 229,9 ± 455,4 |
| Dosis diaria media de hidroxicloroquina (mg) | 254 | 333 |
| Dosis media acumulada de hidroxicloroquina (g) | 251,3 ± 182,2 | 110,0 ± 106,1 |
| Duración de tratamiento (años) | 3,2 ± 2,5 | 3,8 ± 4,4 |
| Enfermedad reumática | ||
| Artritis reumatoide | 16 (41) | 3 (60) |
| LES, n (%) | 13 (33,3) | 2 (40) |
| Artrosis, n (%) | 3 (7,9) | |
| Síndrome de Sjögren, n (%) | 2 (5,1) | |
| EMTC, n (%) | 2 (5,1) | |
| Otros, n (%) | 2 (5,1) | |
| Tratamientos concomitante corticoideo, n (%) | 19 (50) | 3 (60) |
| Hipertensión arterial, n (%) | 11 (28,9) | 4 (80) |
| Diabetes mellitus, n (%) | 5 (13,2) | 0 (0) |
| Afectación hepática/renal, n (%) | 0 (0) | 0 (0) |
| Exploraciones complementarias | ||
| SD-OCT positivo, n (%) | 6 (15,8) | 5 (100) |
| ERG positivo, n (%) | 3 (7,9) | 3(60) |
| FO positivo, n (%) | 5 (13,2) | 2 (40) |
EMTC: enfermedad mixta del tejido conectivo; ERG: electrorretinografía; FO: fondo de ojo; g: gramos; LES: lupus eritematoso sistémico; mg: miligramos; SD-OCT: tomografía de coherencia óptica de dominio espectral.
Las variables cuantitativas se expresan como media ± desviación estándar (DE), y las variables cualitativas, como n (%).
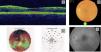
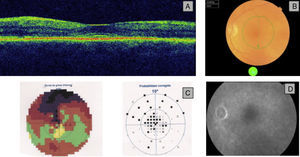
Se detectó toxicidad retiniana en 5 de los pacientes evaluados (13,1%, IC del 95%, 5-21%). Tres estaban en tratamiento con HCQ, con una dosis media diaria de 333mg y acumulada de 111 g, y 2 en tratamiento con CQ, con una dosis media diaria de 250mg y acumulada de 230 g. Cuatro pacientes con toxicidad retiniana tenían antecedente de hipertensión arterial y 3 tomaban corticoides a una dosis equivalente inferior a 10mg de prednisona/día. Los 5 pacientes presentaron alteración de la SD-OCT mientras, que solo en 2 de ellos se observó en el fondo de ojo una imagen típica de maculopatía en ojo de buey (fig. 1). En los otros 3 pacientes se detectaron alteraciones en el campo visual y solo en 2 de estos 3 se hallaron alteraciones en la ERG.
En la SD-OCT encontramos alteración en las capas más internas de la retina a nivel de la línea IS/OS (zona de unión de los segmentos interno y externo de los fotorreceptores) consistente en hiperreflectividad subfoveal, con imagen de doble línea paralela al epitelio pigmentario retiniana. En el campo visual, el defecto observado fue variable en función del grado de afectación, encontrando en la zona central del campo visual una disminución de la sensibilidad en la curva de Bebie y un aumento de defecto medio y varianza perdida. En la ERG se observó una respuesta eléctrica de la retina de baja amplitud bilateralmente.
No se encontró asociación estadísticamente significativa entre toxicidad retiniana y tipo de antipalúdico. Sin embargo, al analizar por separado a los 7 pacientes en tratamiento con CQ se observó que el 42,9% de ellos presentaban una SD-OCT alterada, con una p = 0,06.
Encontramos una relación positiva entre toxicidad retiniana e hipertensión arterial (p < 0,05). No existió asociación entre afectación retiniana y el uso de corticoides, diabetes mellitus, edad y sexo del paciente, enfermedad reumática de base, duración y dosis diaria o acumulada del tratamiento con antipalúdicos.
DiscusiónNuestro estudio mostró una frecuencia de toxicidad retiniana en pacientes en tratamiento con antipalúdicos del 13,1%, con una mayor tendencia en pacientes en tratamiento con CQ. Esta frecuencia fue superior a la encontrada en la mayoría de estudios previos1,3,4 a excepción del estudio de Kobak et al.5. Esto puede deberse tanto a la ausencia de evaluación estandarizada para detectar toxicidad retiniana, a diferencia de nuestro estudio donde se siguió de manera protocolizada las recomendaciones de la Academia Americana de Oftalmología respecto al cribado de los pacientes en tratamiento con antipalúdicos, como a la utilización de nuevos métodos diagnósticos de gran precisión (SD-OCT, ERG), que permiten una detección precoz. Así, se realizaron a todos los pacientes fondo de ojo y SD-OCT, lo que ha podido permitir identificar a un mayor número de pacientes con afectación retiniana. Por otra parte, Kobak et al. reconocen que su población de estudio pudiera presentar una mayor gravedad al proceder de un entorno de investigación clínica, lo que explicaría que la frecuencia de retinopatía sea mayor.
Comparando a los pacientes en función del antipalúdico, se observó que los pacientes en tratamiento con CQ tenían tendencia a presentar un mayor riesgo de toxicidad retiniana, y si el grupo de estudio hubiera sido más amplio es probable que la diferencia hubiera alcanzado la significación.
Entre los factores asociados a toxicidad retiniana por antipalúdicos los más importantes son la duración del tratamiento y dosis diaria, aunque encontramos resultados contradictorios en los diferentes estudios. En nuestro estudio solo encontramos una asociación positiva entre toxicidad retiniana e hipertensión arterial. La inducción de estrés oxidativo y disfunción endotelial cuando existe hipertensión arterial6 podría explicar este hallazgo, pues se ha demostrado que ambos procesos actúan como promotores del daño vascular progresivo y de las complicaciones ateroescleróticas y trombóticas en las paredes vasculares.
En cuanto a las implicaciones clínicas de nuestros hallazgos, a todos los pacientes en los que se detectó toxicidad retiniana se les retiró el tratamiento con antipalúdicos, cambiando este por otro fármaco inmunosupresor según la enfermedad de base. En los 3 casos en los que se detectaron de manera precoz toxicidad retiniana mediante la SD-OCT, sin maculopatía típica en ojo de buey, no se encontraron alteraciones significativas de la agudeza visual que pudieran influir en la calidad de vida de los pacientes.
Nuestro estudio no está exento de limitaciones. En primer lugar, el diseño retrospectivo. Y, en segundo lugar, el tamaño muestral, que pudo condicionar la falta de identificación de factores de riesgo asociados a toxicidad retiniana secundaria a antipalúdicos.
Sin embargo, la evaluación oftalmológica protocolizada lo distingue de los estudios previos. Además, en 3 de los 5 pacientes con toxicidad retiniana la SD-OCT resultó crucial, ya que oftalmológicamente no presentaban alteraciones significativas. Por tanto, alteraciones iniciales en las capas externas de la retina ayudan a la detección precoz de toxicidad retiniana, siendo especialmente útil ya que la SD-OCT está disponible en la mayoría de los hospitales y es altamente sensible y fácil de realizar en la práctica clínica. En pacientes con SD-OCT alterada, el campo visual y la ERG ayudaron a confirmar la toxicidad en estadio precoz.
En resumen, la frecuencia de toxicidad retiniana por antipalúdicos en nuestro estudio fue alta, con tendencia a un riesgo mayor en pacientes en tratamiento con CQ. Encontramos como factor de riesgo asociado la hipertensión arterial, aunque este hallazgo debe confirmarse en posteriores estudios. Consideramos que es fundamental el cribado estandarizado de los pacientes en tratamiento con antipalúdicos para la detección precoz de toxicidad retiniana, aunque se precisa realizar estudios prospectivos de mayor tamaño muestral con las nuevas técnicas oftalmológicas disponibles para confirmar los resultados obtenidos.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflictos de interesesLos autores declaran no tener ningún conflicto de intereses.