Existe una búsqueda urgente de alternativas a los antibióticos para prevenir infecciones, debido al aumento acelerado de la resistencia a los antibióticos. Esto es más grave para los pacientes con infecciones recurrentes que tienen que ser tratados con varios ciclos de antibióticos al año, lo que incrementa el riesgo de resistencia a los antibióticos, que puede ser potencialmente mortal. En los últimos años se ha demostrado que el uso de vacunas profilácticas por vía mucosa para estos pacientes es una alternativa potencialmente beneficiosa y segura para prevenir infecciones. El nuevo conocimiento sobre la inmunidad de las mucosas y la inmunidad entrenada, una forma de memoria de la inmunidad innata que puede mejorar la respuesta a diferentes amenazas por infecciones, ha hecho más fácil expandir su utilización. La aplicación clínica de la inmunidad entrenada de estos fármacos podría explicar sus efectos simultáneos pro-tolerogénicos y potenciadores en diversas células inmunitarias para diferentes infecciones. En esta revisión describimos los mecanismos inmunomoduladores de las vacunas polibacterianas de la mucosa, su conexión con la inmunidad entrenada y su utilidad en la prevención de infecciones recurrentes en pacientes inmunocomprometidos.
An urgent search is currently underway for alternatives to antibiotics to prevent infections, due to the accelerated evolution and increase in antibiotic resistance. This problem is more serious for patients with recurrent infections, since they have to use many cycles of antibiotics per year, so the risk for antibiotic resistance is higher and can be life-threatening. In recent years, the use of prophylactic vaccines via the mucosal route for these patients with recurrent infections has been demonstrated as a potentially beneficial and safe alternative to prevent infections. The new knowledge about mucosal immunity and trained immunity, a form of innate immunity memory that can enhance the response to different infectious threads, has made it easier to extend its use. The application of the new concepts of trained immunity may explain the simultaneous pro-tolerogenic and boosting effect or effects of these drugs on diverse immune cells for different infections. In this review, we describe the immunomodulatory mechanisms of mucosal polybacterial vaccines and their connection with trained immunity and its utility in the prevention of recurrent infections in immunosuppressed patients.
Las resistencias a antibióticos constituyen el principal foco de atención para la salud pública, según datos de la Organización Mundial de la Salud, por lo que la búsqueda de alternativas en la profilaxis frente a infecciones recurrentes es una urgencia1-3. Los antibióticos son la piedra angular de la terapia frente a las enfermedades infecciosas, son efectivos frente a la mayor parte de los patógenos bacterianos, fúngicos y parasitarios, con el problema creciente de las multirresistencias, si bien solo un pequeño número de fármacos son eficaces frente a virus. A modo de ejemplo, a pesar de la importante reducción en la enfermedad respiratoria e invasiva por Streptococcus pneumoniae (neumococo), debido al uso extendido de los antibióticos y la implementación de nuevas vacunas conjugadas parenterales, aún se mantiene como una causa relevante de morbimortalidad en humanos4,5. En este contexto de lo que se ha denominado «era post-antibiótica» hay una clara necesidad de nuevas alternativas en la aproximación terapéutica de las enfermedades infecciosas. Los antibióticos se mantendrán como la principal medida para combatir los microorganismos patógenos, pero los medicamentos alternativos que pueden reemplazarlos o utilizarse como coadyuvantes a los antibióticos pueden contribuir a prevenir estas infecciones.
En condiciones naturales, la mayor parte de las bacterias no viven como células individuales, sino como organismos pseudomulticelulares que llevan a cabo comportamientos comúnmente coordinados a través de señales moleculares intercelulares en un proceso conocido como «Quorum sensing» (QS), que aumenta la capacidad de las bacterias para la adaptación a través de la absorción e incorporación, mediante la recombinación de nuevo material genético, de la comunidad bacteriana que las rodea6. Esta coordinación multicelular de los ataques bacterianos maximiza las posibilidades de establecer una infección y permite la diseminación bacteriana7. Aproximadamente el 65% de los agentes causantes de infecciones humanas forman biopelículas bacterianas (biofilms) que favorecen las infecciones crónicas7. El beneficio principal para las bacterias derivado del hecho de formar estas biopelículas es que están físicamente protegidas y poseen entre 10 y 1.000 veces más resistencia que una bacteria única7. En la actualidad las biopelículas suponen un reto importante que merma la eficacia de los antibióticos.
Un caso particular son los pacientes que padecen infecciones bacterianas recurrentes que necesitan ser tratados con antibióticos de forma casi continua, lo que favorece aún más el riesgo de resistencia a antibióticos. Además, estos pacientes presentan frecuentemente disbiosis secundaria a la toma repetida de antibióticos8, lo que a su vez puede favorecer una sobreinfección fúngica. Especialmente en el contexto de las infecciones recurrentes, las vacunas mucosas polibacterianas podrían representar una buena alternativa a los antibióticos de amplio rango de acción utilizados con fines preventivos. Estas vacunas se emplean como inmunomoduladores para prevenir infecciones en pacientes inmunocompetentes, pero su utilización en pacientes inmunocomprometidos es cada vez mayor.
La infección es una de las principales causas de morbimortalidad en los pacientes con enfermedades autoinmunes sistémicas (EAS). La predisposición a la infección en los pacientes con EAS está asociada a una respuesta anómala del sistema inmune innato y adaptativo subyacente a la propia enfermedad y secundario a las terapias inmunomoduladoras e inmunosupresoras. Los glucocorticoides pueden disminuir la respuesta de la inmunidad innata y adaptativa, favoreciendo la susceptibilidad a infecciones bacterianas por estreptococos, Staphylococcus aureus, bacilos gramnegativos, así como enfermedades producidas por hongos como Candida y Aspergillus spp. Otros tratamientos inmunosupresores pueden dañar la inmunidad adaptativa favoreciendo infecciones producidas por virus (sobre todo herpes virus, como herpes zoster, citomegalovirus o virus Ebstein-Baar), bacterias (Legionella spp., Listeria monocytogenes y Salmonella tiphy), Mycobacterium tuberculosis y hongos (Candida, Aspergillus, Histoplasma capsulatum y Cryptococcus) y Pneumocystis jirovecii. Por otro lado, la afectación las célulasB con disminución de la producción de inmunoglobulinas se asocia a infecciones recurrentes por gérmenes encapsulados (Streptococcus pneumoniae, Haemophilus influenzae, meningococo).
En el registro español de reacciones adversas a las terapias biológicas (BIOBADASER) se ha encontrado una mayor incidencia de infecciones en los pacientes con artritis reumatoide (AR) que reciben anti-TNF9; datos similares se siguen confirmando en diferentes informes, donde la frecuencia de las infecciones y la de las infestaciones suponen el 23,9% de todos los acontecimientos adversos registrados en pacientes con terapia biológica.
Hay varias explicaciones posibles para un mayor riesgo de infección en pacientes con AR. La evidencia reciente sugiere que los pacientes con AR tienen alteraciones inmunológicas que involucran a la mayoría de las célulasT circulantes desde una etapa temprana en el curso de la enfermedad10. Por lo tanto, la capacidad del sistema inmune para responder a nuevos estímulos antigénicos puede verse comprometida. Alternativamente, la terapia con glucocorticoides y otros inmunosupresores también puede predisponer a los pacientes con AR al desarrollo de sepsis11,12. Otros factores que pueden influir en el riesgo de infección en pacientes con AR son factores relacionados con la enfermedad (inmovilidad, cirugía articular), manifestaciones extra-articulares de AR (síndrome de Felty, enfermedad pulmonar reumatoide) y comorbilidades (diabetes mellitus).
Las infecciones se suelen localizar en el tracto respiratorio superior e inferior, la piel y el tracto genitourinario. Habitualmente se deben a Staphylococcus aureus y a gérmenes gramnegativos. De igual manera, se ha comunicado una mayor frecuencia de herpes zoster, y también se han descrito casos de infecciones oportunistas, como listeriosis, aspergilosis diseminada y otras poco frecuentes en España, como histoplasmosis y coccidioidomicosis, aunque su incidencia ha sido baja. Con el resto de agentes biológicos también se ha descrito una mayor incidencia de infecciones.
Por todo ello, se hacen cada vez más necesarias estrategias terapéuticas adyuvantes o alternativas a los antibióticos como es la inmunización de estos pacientes con vacunas para prevenir las infecciones primarias y recurrentes, pues con ello se conseguirá disminuir el uso reiterado de antibióticos, con lo que disminuirá la aparición de resistencias y también la aparición de enfermedades infecciosas severas, con la consiguiente disminución de hospitalizaciones por esta causa.
En esta revisión abordamos los conocimientos más actuales sobre los mecanismos de acción de inmunomoduladores polibacterianos de mucosas, también llamados vacunas antiinfecciosas de mucosas.
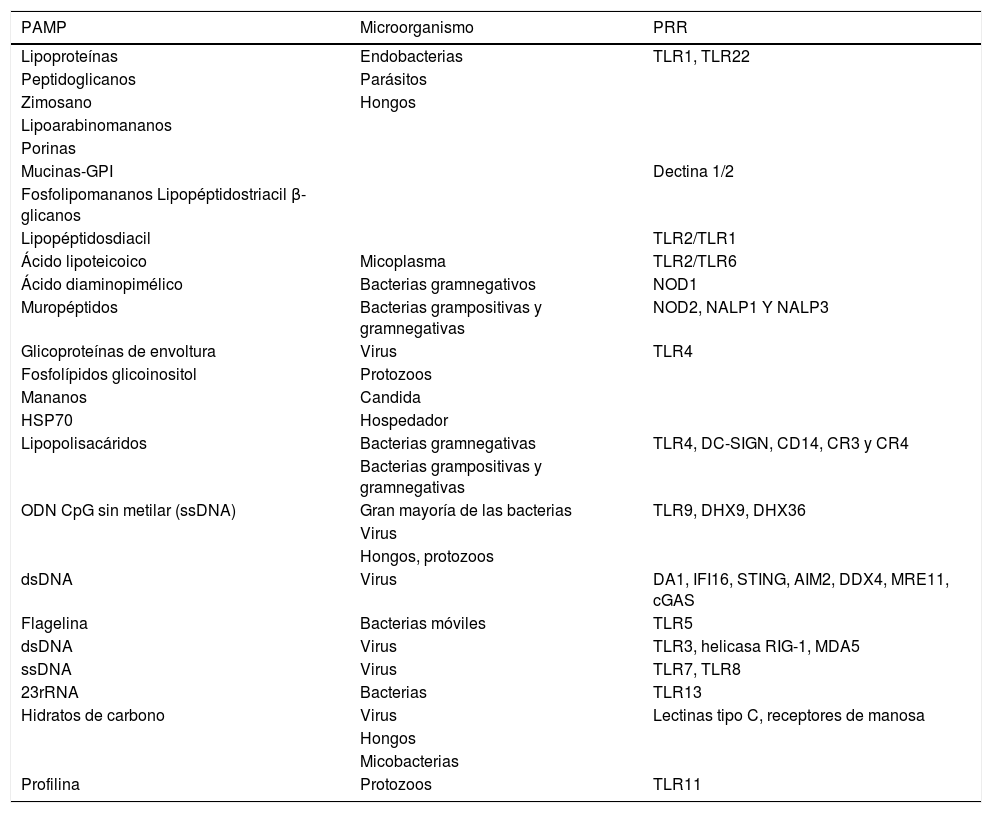
En la frontera: inmunidad de mucosas, nuevo paradigma de la inmunidad entrenadaLas mucosas cubren una superficie muy extensa en nuestro cuerpo, aproximadamente 200 veces mayor que la superficie de la piel13. Las mucosas son la principal vía de entrada de los agentes infecciosos y ambientales. Por ello, las infecciones de mucosas son una de las principales causas de morbimortalidad en el mundo, siendo niños y ancianos los grupos más susceptibles, y no habiendo vacunas efectivas disponibles en la mayoría de los casos. El tejido linfoide asociado a las mucosas (MALT) engloba una red compleja de componentes altamente especializados y compartimentalizados de la inmunidad innata y adaptativa13,14. Incluye el tejido linfoide asociado a la nasofaringe (NALT), a los bronquios (BALT), a la mucosa gastrointestinal (GALT), al tracto urogenital y a las glándulas exocrinas15,16. Las células dendríticas (CD) se activan al reconocer estructuras comunes en los microrganismos patógenos muy conservadas a lo largo de la evolución mediante receptores de reconocimiento de patrones (PRR) (tabla 1). La captación de antígenos por parte de las CD puede realizarse vía directa e indirecta17. Vía indirecta es, por ejemplo, a través de la captación por las célulasM (Microfold), por células caliciformes, por receptores neonatales Fc (FcRn) y tras apoptosis17. Las célulasM son células especializadas que captan antígenos y bacterias entéricas a través de la superficie epitelial para la captura y procesamiento por parte de las CD y macrófagos, que iniciarán la respuesta inmunitaria efectora18. Las CD pueden también capturar directamente antígenos desde el lumen extendiendo sus dendritas18.
Repertorio innato de receptores de reconocimiento de patrones (PRR) que se unen a patrones moleculares asociados a patógenos (PAMP) y a patrones moleculares asociados a daños (DAMP)
| PAMP | Microorganismo | PRR |
|---|---|---|
| Lipoproteínas | Endobacterias | TLR1, TLR22 |
| Peptidoglicanos | Parásitos | |
| Zimosano | Hongos | |
| Lipoarabinomananos | ||
| Porinas | ||
| Mucinas-GPI | Dectina 1/2 | |
| Fosfolipomananos Lipopéptidostriacil β-glicanos | ||
| Lipopéptidosdiacil | TLR2/TLR1 | |
| Ácido lipoteicoico | Micoplasma | TLR2/TLR6 |
| Ácido diaminopimélico | Bacterias gramnegativos | NOD1 |
| Muropéptidos | Bacterias grampositivas y gramnegativas | NOD2, NALP1 Y NALP3 |
| Glicoproteínas de envoltura | Virus | TLR4 |
| Fosfolípidos glicoinositol | Protozoos | |
| Mananos | Candida | |
| HSP70 | Hospedador | |
| Lipopolisacáridos | Bacterias gramnegativas | TLR4, DC-SIGN, CD14, CR3 y CR4 |
| Bacterias grampositivas y gramnegativas | ||
| ODN CpG sin metilar (ssDNA) | Gran mayoría de las bacterias | TLR9, DHX9, DHX36 |
| Virus | ||
| Hongos, protozoos | ||
| dsDNA | Virus | DA1, IFI16, STING, AIM2, DDX4, MRE11, cGAS |
| Flagelina | Bacterias móviles | TLR5 |
| dsDNA | Virus | TLR3, helicasa RIG-1, MDA5 |
| ssDNA | Virus | TLR7, TLR8 |
| 23rRNA | Bacterias | TLR13 |
| Hidratos de carbono | Virus | Lectinas tipo C, receptores de manosa |
| Hongos | ||
| Micobacterias | ||
| Profilina | Protozoos | TLR11 |
Evidencia clínica y epidemiológica extraída de estudios con vacunas convencionales ponía de manifiesto una reducción de la mortalidad infantil en los individuos vacunados frente al sarampión y la tuberculosis en el primer año de vida por causa infecciosa frente a los no vacunados19. Estos resultados no pueden ser explicados por una protección específica a estas enfermedades, sino por una protección de amplio espectro, más propia de la inmunidad innata, en lo que se ha denominado «inmunidad entrenada» (trained immunity)20,21. La inmunidad entrenada se refiere a que hay células —como por ejemplo el monocito/macrófago o las células natural killer (NK), entre otras— capaces de generar una respuesta intensificada ante una segunda infección por el mismo microorganismo y por otro diferente (protección cruzada) e independiente de la respuesta adaptativa (linfocitoT yB), si bien potencia a su vez la respuesta adaptativa22-26. Estudios que datan de 50años ya habían descrito que las infecciones confieren propiedades antibacterianas adquiridas a través de bacterias patógenas específicas y también de otras no relacionadas22. Los mecanismos que median esta inmunidad entrenada incluyen reprogramación epigenética y transcripcional de las células de la inmunidad innata, incluyendo modificaciones en las histonas y en el ADN que pueden favorecer la transcripción de citoquinas proinflamatorias23, una contribución de microARN, junto a cambios metabólicos (fig. 1)27.
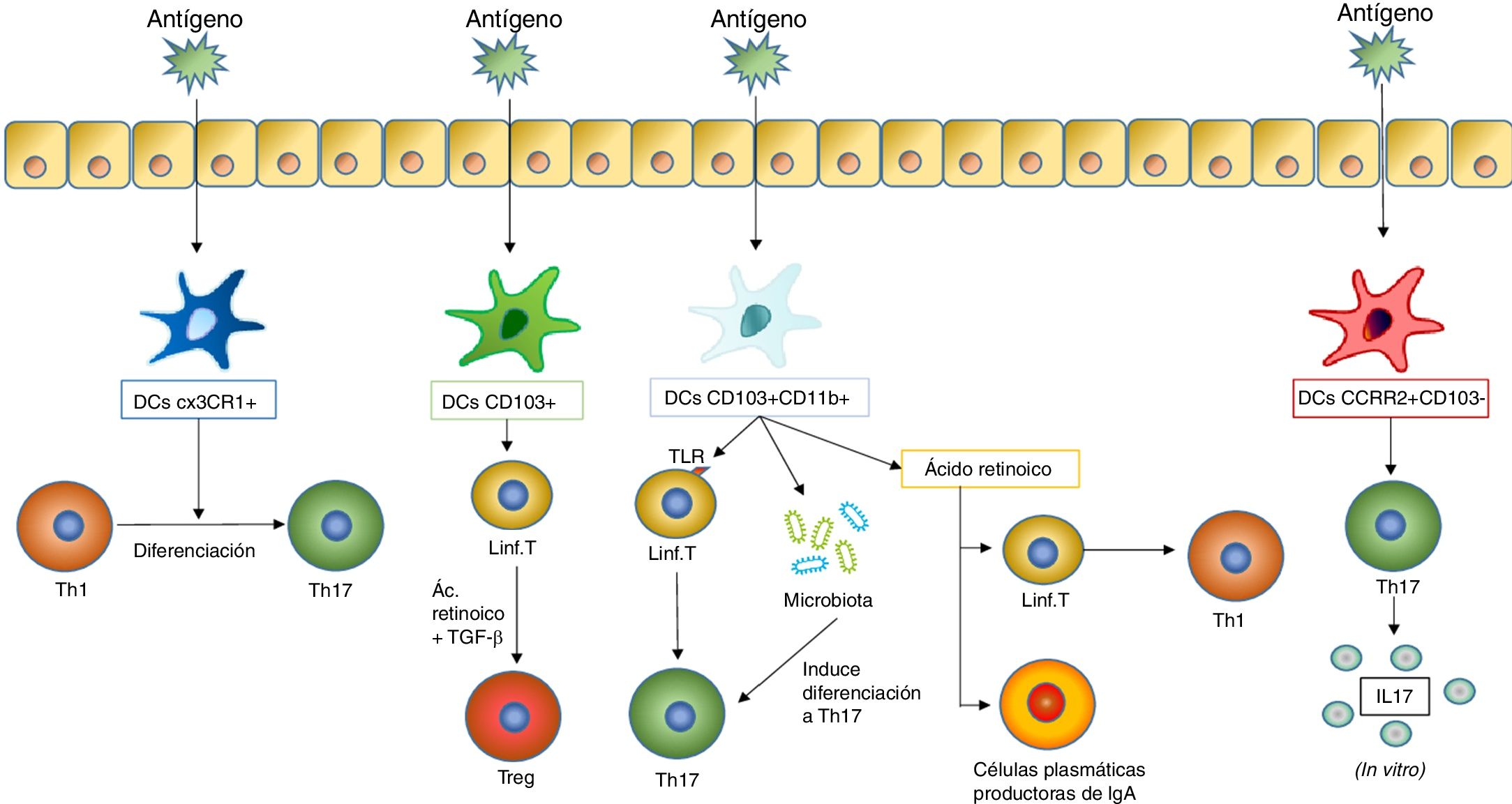
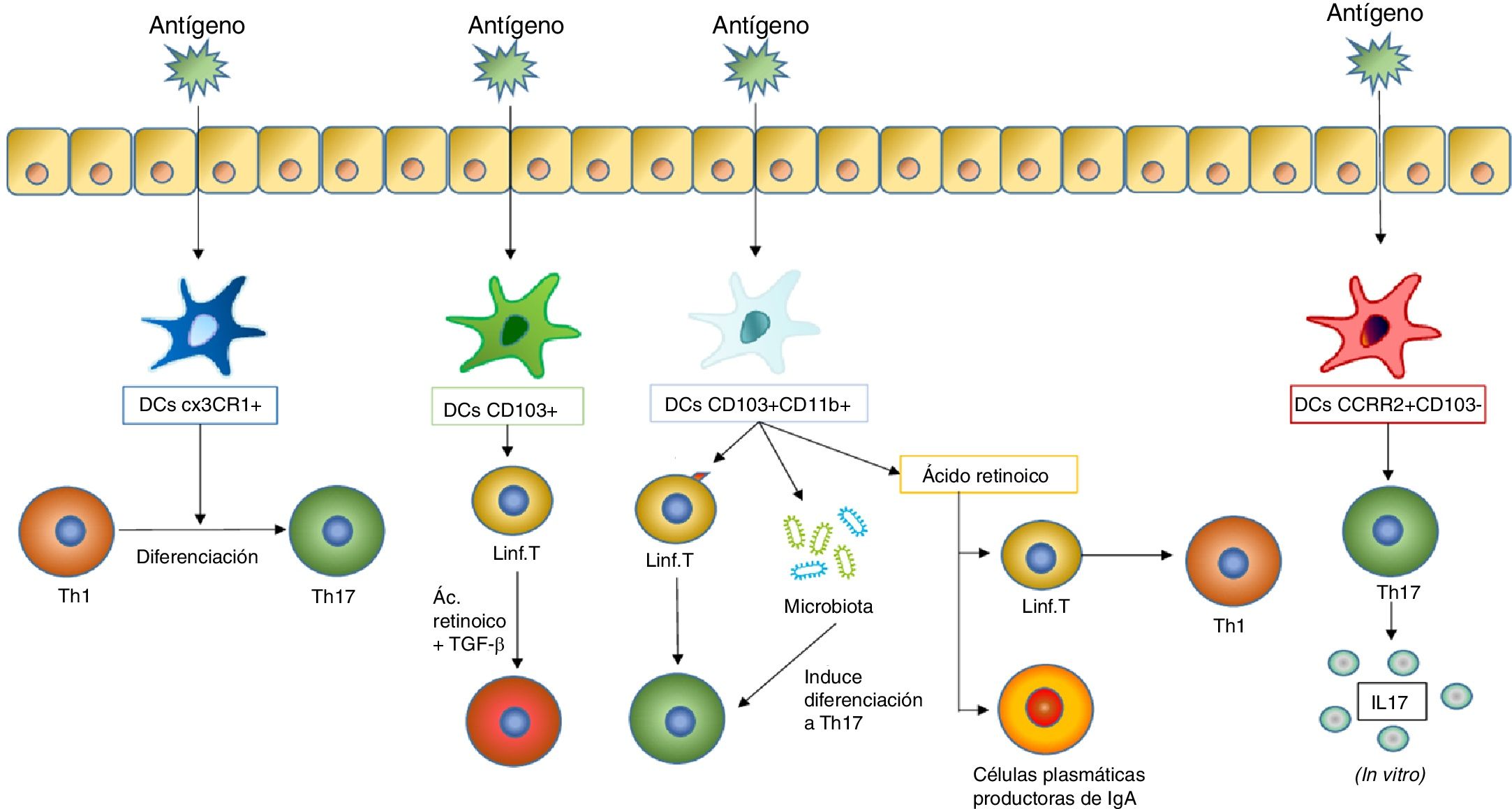
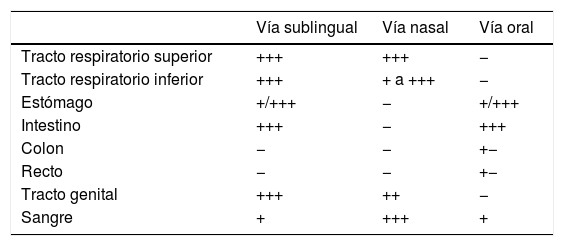
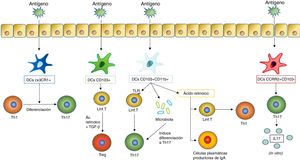
Al ser estimuladas con un antígeno, las células dendríticas inducen diferentes respuestas en los tejidos mucosos. Una de las respuestas más importantes es la diferenciación de los linfocitosT en diferentes subtipos, que depende a su vez de qué tipo de célula dendrítica estimule dicha diferenciación. En la figura se incluyen los subtipos de DC mencionados anteriormente que inducen la diferenciación de linfocitosT en las mucosas (como las DC CX3CR1+, las CD103+ y las CD103+CD11b+) y las que inducen una estimulación de los linfocitosT para que estos produzcan citocinas (acción llevada a cabo por las DC CCR2+CD103− que da lugar a la producción de IL17 por los linfocitosT).
Las vacunas antiinfecciosas de mucosas son combinaciones de bacterias u hongos completos inactivados o bien de lisados bacterianos que estimulan el sistema inmunitario a través de PRR comunes a diversos gérmenes, que según numerosos estudios disminuyen el número de reinfecciones por los mismos patógenos y por otros patógenos que los contenidos en las vacunas (fig. 2). Los mecanismos subyacentes a este beneficio colateral pueden deberse en gran parte a la «inmunidad entrenada» más que a la específica, que también se ha visto que contribuye al efecto protector.
Inmunidad entrenada. Reprogramación epigenética en células de la inmunidad innata al estimular la inmunidad entrenada. Una vez reconocido el patógeno1 por un receptor, los monocitos experimentan una reprogramación epigenética (principalmente a través de metilaciones en el ADN) y cambios metabólicos, de modo que quedan preparados para responder más robustamente a una estimulación secundaria no específica (patógenos 1, 2 y 3).
A diferencia de las vacunas convencionales administradas parenteralmente, las vacunas de mucosas actúan directamente en tejidos específicos donde los patógenos inician o diseminan infecciones. En las superficies mucosas existe un equilibrio inmunológico mantenido por la flora comensal. La inducción de las respuestas innatas podría suponer la activación de las CD, macrófagos, células epiteliales y células NK, mientras que la estimulación de la inmunidad adaptativa supondría la producción de anticuerpos específicos y célulasB yT memoria. Las vacunas mucosas apropiadamente formuladas estimulan los dos componentes del sistema inmunitario, lo que las hace herramientas prometedoras para la prevención y la profilaxis terapéutica de infecciones28-30. Las respuestas de anticuerpos en las mucosas, fundamentalmente IgA secretora, estimulada por estas vacunas, inhiben un paso crítico en la patogénesis infecciosa microbiana, la adhesión del microorganismo a las células epiteliales de la mucosa, confiriendo una mejor protección frente a la colonización e invasión que las vacunas parenterales31. La IgG de las mucosas media la opsonización e internalización de patógenos que han atravesado la barrera epitelial mediante fagocitosis. Esto induce la activación de los fagocitos y la eliminación de los patógenos o la presentación de antígenos derivados de los mismos, favoreciendo la diferenciación de múltiples subtipos de linfocitosT efectores, como los linfocitos Th17, los linfocitosTγδ y los linfocitosT CD8+ citotóxicos (CTL), para la destrucción del patógeno32. Los linfocitosT memoria residentes en los tejidos mucosos (TRM) pueden responder rápidamente a una reinfección local por patógenos, independientemente del reclutamiento de linfocitosT procedentes de la sangre. Cuando las TRM CD8+ son activadas liberan IFN-γ, que amplifica y complementa la activación de la respuesta inmune innata creando un microambiente antivírico en la mucosa. La inducción de los linfocitos TRM es un reto actualmente para las estrategias de vacunación, y puede que las vacunas mucosas sean una ruta eficaz para generar persistentemente linfocitos TRM33.
La administración a través de las mucosas induce tolerancia, lo que supone un beneficio adicional en el tratamiento de las EAS. Las vacunas sublinguales para la inmunoterapia alergénica han sido usadas durante cien años, y estudios recientes sugieren que la inmunoterapia sublingual puede mejorar la inducción de tolerancia sistémica. De acuerdo con el modelo actual de mecanismos inmunes subyacentes, el alérgeno es captado por las CD plasmacitoides tolerogénicas de las amígdalas, que posteriormente emigran a los nódulos linfáticos cervicales e inducen la respuesta de los linfocitosTreg34. Las biopsias del epitelio oral han demostrado que hay una mayor cantidad de célulasTreg en pacientes tratados con inmunoterapia sublingual que en pacientes tratados con placebo35. Este modelo en alergia sería trasladable a lo que ocurre en pacientes con EAS, si bien se necesitan estudios específicos que lo demuestren.
Vacunas antiinfecciosas en enfermedades autoinmunesLas enfermedades autoinmunes son un objetivo principal para el desarrollo de estos fármacos36. La inducción de secreción de sIgA específica tiene múltiples mecanismos regulatorios que también pueden promover baja capacidad de respuesta de los linfocitosT de las mucosas y sistémicos, mediante un efecto modulador de la diferenciación de linfocitosTreg37.
Modelos experimentalesLa administración mucosa intranasal y perlingual de antígenos puede inducir una profunda supresión de la inmunidad celular, como se ha demostrado por la disminución de las reacciones de hipersensibilidad retardada, bajos niveles de proliferación de célulasT y altos niveles de secreción de citoquinas inmunosupresoras34,38,39. Un estudio reciente demostró que la vacunación oral con una vacuna atenuada de Salmonella inducía célulasTreg específicas al antígenoI del factor de colonización (CFA/I) de las fimbrias, mientras que protegía simultáneamente frente a la encefalomielitis autoinmune experimental (EAE), un modelo murino de esclerosis múltiple40. En este estudio, la vacunación oral frente a un antígeno irrelevante inducía célulasTreg que podrían controlar la autoinmunidad y un efecto antiinfeccioso concomitante. Otro estudio en EAE ha mostrado este efecto dual frente a infección bacteriana del tracto respiratorio mediante la producción de la citoquina antiinflamatoria IL-10 que suprimiría la migración de célulasT autorreactivas al sistema nervioso central41. Estudios similares en el modelo experimental de artritis inducido por colágeno en ratones DBA/1 sugieren que la inducción de una inmunidad espectadora (bystander) frente a las bacterias podría controlar potencialmente procesos autoinmunes o inflamatorios36,38. Este efecto inmunomodulador de algunas bacterias podría ser explotado para mejorar un nuevo concepto de las vacunas mucosas bacterianas como una innovación terapéutica para favorecer la tolerancia inmunológica (tolerancia cruzada) y la homeostasis en el contexto de las enfermedades autoinmunes.
Estudios clínicosUn estudio clínico observacional prospectivo evaluó los efectos clínicos e inmunológicos del tratamiento con vacunas sublinguales de combinaciones bacterianas en respuestas antígeno-específicas a bacterias responsables de infecciones del tracto respiratorio42. La inmunización diaria con una preparación sublingual polivalente bacteriana durante un período de 6meses fue estudiada en una cohorte de 17 pacientes con infecciones recurrentes respiratorias (IRR). El número de infecciones respiratorias en pacientes inmunizados disminuyó significativamente comparado con la incidencia el año previo. También se observó una clara disminución en la severidad y duración de los eventos infecciosos respiratorios. Los resultados inmunológicos demostraron un incremento significativo en la frecuencia y la capacidad proliferativa de linfocitosT CD4+ específicos en sangre frente a antígenos bacterianos contenidos en la vacuna, a los 6meses de tratamiento. Además, se evidenció un incremento en la capacidad proliferativa de los linfocitosT CD4+ y CD8+ específicos de antígenos del virus influenza tras 6meses de tratamiento (no contenida en la vacuna), lo que podría sugerir que la preparación bacteriana habría estimulado de forma no específica a los linfocitosT in vivo al virus influenza, que dieron una respuesta más potente. Es interesante el caso de uno de los pacientes descritos en este estudio que había padecido 12 episodios de herpes oral el año previo, y que solo informó 3 episodios tras la inmunización con la preparación bacteriana, sugiriendo un efecto in vivo no específico que potencia la respuesta antivírica (inmunidad entrenada). En otro estudio observacional prospectivo con 669 mujeres con infecciones recurrentes del tracto urinario (RUTI) que compararon la eficacia entre un tratamiento profiláctico con antibióticos (Septrin) y la preparación sublingual bacteriana, el 100% de los pacientes experimentaron una nueva infección en el siguiente año versus menos del 10% en el grupo tratado con la preparación bacteriana. Un hallazgo interesante en este estudio fue que los pacientes que previamente tuvieron infecciones con bacterias no incluidas en la vacuna no desarrollaron reinfecciones, sugiriendo esto una protección horizontal o cruzada (cross-protection) que podría atribuirse a una potencialización de la inmunidad innata entrenada43-45.
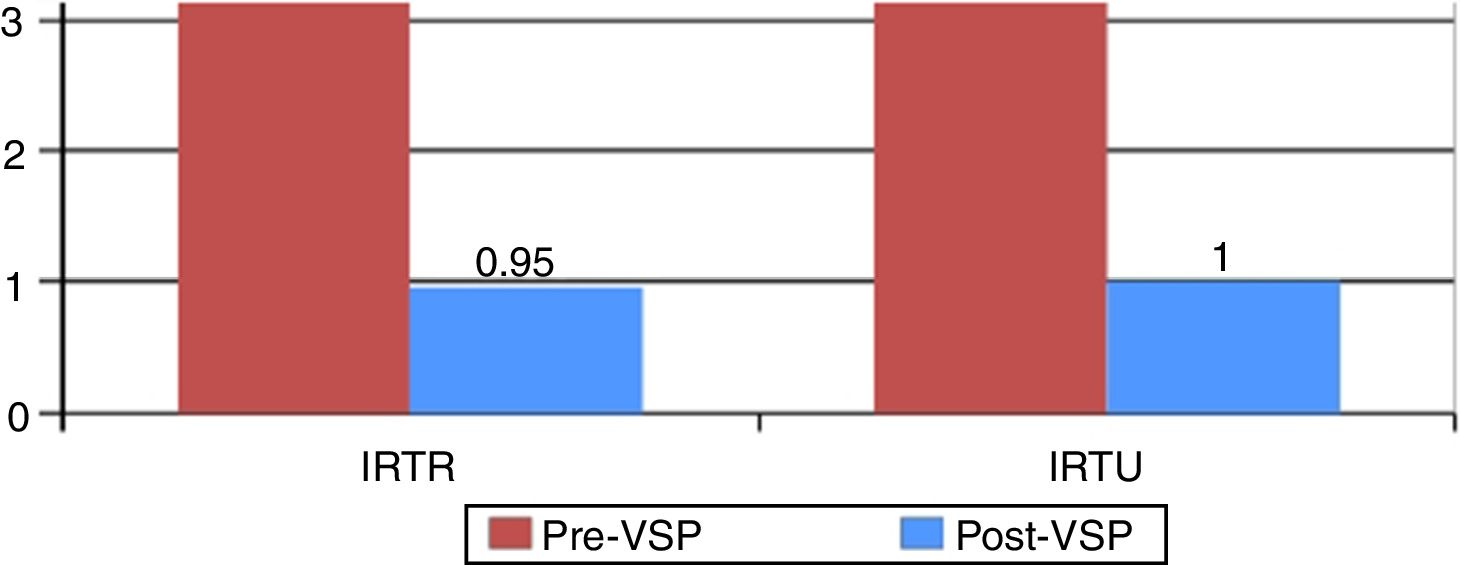
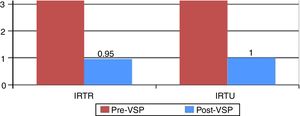
En un estudio observacional prospectivo realizado por nuestro grupo en 50 pacientes con enfermedades inflamatorias (AR [43,18%], lupus eritematoso sistémico [22,72%] y enfermedad mixta del tejido conectivo [6,81%]) que seguían tratamiento con DMARD biológicos y/o no biológicos y glucocorticoides a bajas dosis en la mayoría de ellos, y que presentaban infecciones urinarias y/o respiratorias de repetición, fueron tratados con dos formulaciones sublinguales polibacterianas diferentes dependiendo del tipo de infección (tabla 2). Las vacunas se administraban en ciclos de 3meses al año y se registró la respuesta clínica a los 6meses y al año. La comparación pareada del número de eventos infecciosos en ambos grupos mostró una disminución significativa en la tasa de infecciones urinarias de repetición (RUTI) de 5,57±8,41 frente a 1,0±1,28 (p<0,05) y en la tasa de infecciones respiratorias de repetición (RRTI) de 4,1±1,98 frente a 0,95±1,52 (p<0,05) en el año previo frente al año posterior a la vacuna, así como una disminución significativa en el uso de antibióticos a los 6meses de la vacuna (fig. 3). Seis de 38 pacientes tratados con la vacuna para RUTI que presentaban simultáneamente infecciones respiratorias mejoraron significativamente no solo de su clínica infecciosa urinaria sino también de la respiratoria, sugiriendo una protección cruzada innata46,47.
Las intervenciones terapéuticas con vacunas antiinfecciosas de mucosas poseen diferentes ventajas frente a las vacunas parenterales convencionales: a)llevan a cabo sus efectos directamente en el sitio de infección en la mucosa y pueden prevenir la infección y la colonización por parte de los patógenos; b)la inmunización en la mucosa puede resultar en la secreción de anticuerpos en otras mucosas más distantes y también de forma sistémica10; c)no requieren personal médico para su administración y pueden ser usadas en vacunaciones en masa y campañas de prevención de enfermedades, y d)son indoloras y sencillas de administrar. Por otro lado, y teniendo en cuenta que las bacterias grampositivas estimulan la producción de IL-12 y que las bacterias gramnegativas estimulan la producción de IL-10 por los monocitos, la combinación de bacterias grampositivas y gramnegativas en las vacunas antiinfecciosas de mucosas parece aportar una respuesta inmunológica sinérgica que podría ser mayor dependiendo de la patología involucrada48. Se han observado diferencias en la inducción de respuestas inmunitarias según la vía de administración, siendo la sublingual la más ventajosa (tabla 3). Por último, presentan un gran potencial de desarrollo aprovechando estas características de inmunidad entrenadas, que sería explotable y mejorable mediante herramientas como la vaccinología reversa para el desarrollo de adyuvantes a vacunas convencionales. Sin embargo, a diferencia de las vacunas parenterales, estas vacunas requieren un estímulo repetitivo y la duración del tratamiento activo puede ser larga y requiere la adherencia por parte del paciente.
Comparación de la diseminación anatómica de sIgA según diferentes rutas de inmunización
| Vía sublingual | Vía nasal | Vía oral | |
|---|---|---|---|
| Tracto respiratorio superior | +++ | +++ | − |
| Tracto respiratorio inferior | +++ | + a +++ | − |
| Estómago | +/+++ | − | +/+++ |
| Intestino | +++ | − | +++ |
| Colon | − | − | +− |
| Recto | − | − | +− |
| Tracto genital | +++ | ++ | − |
| Sangre | + | +++ | + |
Fuente: adaptado de Alecsandru et al.42.
En resumen, la intervención terapéutica con preparados polibacterianos de administración mucosa con bacterias completas inactivadas o con lisados bacterianos estimula la inmunidad innata y la adaptativa presentes en la mucosa49 y aporta un beneficio clínico mayor, atribuyéndose su efecto a los siguientes mecanismos: a)las bacterias completas son presentadas al sistema inmune de un modo más natural, maximizando todo su potencial como inmunógenos45,50,51, y b)las bacterias completas estimulan diferentes mecanismos inmunitarios, los cuales ha sido comprobado que son muy importantes para una activación celular completa, como la fagocitosis52. Se requiere un cambio en el diseño de los resultados de estas vacunas, buscando más un efecto de beneficio clínico que el propiamente antígeno-específico.
Las inmunodeficiencias secundarias a terapia inmunosupresora (trasplante de órganos, trastornos reumatológicos, oncología, enfermedades autoinmunes órganoespecíficas), enfermedades metabólicas crónicas (diabetes) o infecciones crónicas (HIV) son situaciones que también conducen a infecciones recurrentes. El uso de vacunas polibacterianas en pacientes que están activamente inmunosuprimidos para preservar un órgano trasplantado, o para mantener bajo control una enfermedad autoinmune, representa un verdadero desafío clínico por el alto riesgo de infecciones y el consiguiente impacto en la morbimortalidad.
ConclusionesEl tratamiento con fármacos polibacterianos o vacunas antiinfecciosas de mucosas, que potencian la inmunidad entrenada innata como principal objetivo en la prevención de infecciones recurrentes, constituye una estrategia terapéutica innovadora y con resultados prometedores. Se requieren nuevos estudios prospectivos y ensayos clínicos aleatorizados para evaluar su eficacia y optimizar las formulaciones actuales. Asimismo, debido a que la finalidad de estos fármacos es una protección de amplio espectro, los objetivos primarios de eficacia deben ser diseñados en relación con la respuesta clínica.
FinanciaciónLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, del sector comercial o de entidades sin ánimo de lucro.
Conflicto de interesesLos autores manifiestan que no tienen ningún conflicto de intereses.