La exposición a la gravedad artificial (GA), a través de la centrifugación humana, constituye la base del tratamiento denominado terapia gravitacional (TG), mediante el cual se produce un estímulo mecánico sobre la pared vascular induciendo la síntesis y liberación de prostaciclina. Se usa desde hace más de cuatro décadas en Uruguay en el tratamiento de enfermedades de base vascular. En la esclerosis sistémica (ES) ha demostrado gran beneficio y excelente perfil de seguridad. Sin embargo, existe un desconocimiento en la comunidad científica acerca de la TG y de sus resultados.
ObjetivoEvaluar la eficacia de la TG en la afección cutánea y vascular, calidad de vida y capacidad funcional y su perfil de seguridad en pacientes con ES.
MetodologíaEstudio descriptivo y retrospectivo de pacientes con ES asistidos en un centro de autoinmunidad de Montevideo, tratados con TG en los últimos 10años.
ResultadosSe incluyeron 50 pacientes: 48 mujeres (96%) y 2 hombres (4%), con una edad media de 62±12 años. El tiempo medio de evolución de la ES al momento de inclusión en el estudio y al iniciar la TG fue de 6,8±3,2 años y de 2,8±3,2 años, respectivamente. Post-TG se observó una mejoría significativa del puntaje modificado de Rodnan (mRSS) (pre-TG 19,2±8,7 vs post-TG 5,4±5,0, p<0,05), que no se relacionó con el tiempo de evolución de la enfermedad al inicio de la TG, extensión cutánea o perfil inmunológico. El grado de mejoría post-TG se correlacionó con un mayor mRSS inicial (R=0,84, p<0,05). Se observó mejoría significativa del número de pacientes con puffy fingers (pre-TG 50% vs post-TG 20% pacientes, p<0,05), pero no en telangiectasias, pitting scars o esclerodactilia. La gravedad del fenómeno de Raynaud disminuyó significativamente, pre-TG: grado 3-4, 43/48 (89,6%) pacientes vs post-TG: grado ≤2, 42/47 (89,4%) pacientes, p<0,05, así como también el dolor vascular medido por EVA (escala 0-10) (pre-TG: 7,6±2,2 vs post-TG: 1,4±1,2, p<0,05). También se registraron casos de curación de úlceras digitales. En cuanto a los resultados reportados por los pacientes, el 97% refirieron mejoría en calidad de vida y el 89,5% mejoría en capacidad para realizar actividades de la vida diaria. No se registraron efectos adversos significativos.
ConclusionesLa TG mejoró el compromiso cutáneo y vascular, la calidad de vida y la capacidad funcional en pacientes con ES con excelente perfil de seguridad. Se necesitan ensayos clínicos controlados y aleatorizados para corroborar estos resultados observacionales.
The exposure to artificial gravity (AG) through human centrifugation is the basis of the treatment called gravity therapy (GT), in which the mechanical stimulation over the vessel wall, induces the synthesis and release of prostacyclin. It has been used for more than four decades in Uruguay in the treatment of different vascular-based pathologies. In patients with systemic sclerosis (SSc) it has shown good benefits and excellent safety profile over the years. However, there is a lack of knowledge in the scientific community about GT and its results.
ObjectiveTo evaluate the effectiveness of GT in cutaneous and vascular involvement, in the quality of life and functional capacity and its safety profile in patients with SSc.
MethodologyIt is a descriptive and retrospective study of patients with SSc assisted in an autoimmunity center in Montevideo, treated with GT in the last 10years.
ResultsFifty patients were included, 48 women (96%) and 2 men (4%) with a mean age of 62±12 years. The mean time of evolution of SSc at the time of inclusion in the study at the beginning of GT was 6.8±3.2 years and 2.8±3.2 years respectively. After GT, a significant improvement in the modified Rodnan skin score (mRSS) was observed (pre-GT 19.2±8.7 vs post-GT 5.4±5.0, P<.05), which was not related to the time of disease progression at the beginning of GT nor to the skin extension or immunological profile. The degree of improvement post-GT was related to a higher initial mRSS (R=0.84, P<.05). Also, a significant improvement was observed in the number of patients with puffy fingers (pre-GT 50% vs post-GT 20% patients, P<.05), but not in telangiectasias, pitting scars or sclerodactyly. The severity of Raynaud's phenomenon significantly decreased (pre-GT: grade 3-4, 43/48 (89.6%) patients vs post-GT: grade ≤2, 42/47 (89.4%) patients, P<.05) as well as the vascular pain measured with VAS (0-10 scale) (pre-GT: 7.6±2.2 vs post-TG: 1.4±1.2, P<.05). The healing of digital ulcers was also recorded. Regarding the results reported by patients, 97% reported improvement in the quality of life and 89.5% improvement in the ability to carry out activities of daily living. No significant adverse effects were recorded.
ConclusionsGT improved cutaneous and vascular involvement, the quality of life and the functional capacity in patients with SSc with an excellent safety profile. Randomized, controlled clinical trials are needed to corroborate these observational results.
La esclerosis sistémica (ES) es una enfermedad autoinmune crónica de etiología desconocida. Desde el punto de vista patogénico, se caracteriza por la desregulación inmunológica, vasculopatía y excesivo depósito de colágeno, lo que determina fibrosis cutánea y afectación multiorgánica1. El daño estructural microvascular es responsable de manifestaciones vasculares como el fenómeno de Raynaud (FR), telangiectasias, afección miocárdica, ectasia vascular antral, hipertensión arterial pulmonar, úlceras digitales (UD) y crisis renal esclerodérmica2. La vasculopatía es secundaria al proceso inmunoinflamatorio, que determina disfunción y daño endotelial2-3. Este se expresa por la disminución de la síntesis y liberación de prostaciclina y de óxido nítrico (ON), provocando vasoespasmo, trombosis in situ y proliferación de la íntima, lo que contribuye a la fibrosis y a la rigidez de la pared vascular con estenosis. Además de la pérdida y obliteración de capilares, hay ausencia de formación de nuevos vasos. En la ES la angiogénesis está gravemente comprometida2-5. Las anormalidades en la microcirculación se pueden detectar precozmente mediante la capilaroscopia periungueal.
La ES deteriora la calidad de vida de los pacientes y determina repercusión socioeconómica personal y sanitaria. No existe actualmente un tratamiento curativo. Este suele ser sintomático, y en algunos casos logra la estabilización del paciente por un período variable de tiempo. Algunos fármacos pueden tener efectos secundarios importantes, lo cual no favorece la adherencia al tratamiento y puede repercutir en la calidad de vida de los pacientes. Por otro lado, algunos tratamientos farmacológicos son de alto costo o no están disponibles en Uruguay (p.ej., análogos de la prostaciclina intravenosos).
La exposición a la gravedad artificial (GA) a través de la centrifugación humana constituye la base del tratamiento denominado terapia gravitacional (TG) y se ha utilizado en Uruguay, durante más de 40años. Se ha aplicado para el tratamiento de patologías vasculares y el FR, pero también en el linfedema, síndrome doloroso regional complejo, y para la rehabilitación física de otras afecciones médicas, con resultados exitosos6-18.
Isasi M.E. e Isasi E.S. han demostrado que el vector friccional de la fuerzas hemodinámicas generadas por la TG, a través de la centrifugación humana, constituye un estímulo mecánico vascular que induce la síntesis y liberación de sustancias vasodilatadoras como la prostaciclina y posiblemente ON6,9,15,18. Además de una vasodilatación sostenida, aumentaría el recambio del endotelio vascular y la circulación colateral7-10. Como el endotelio vascular es sensible al estrés/estimulación mecánica durante la hipergravedad, se ha especulado que las células endoteliales desempeñarían un papel central en los efectos terapéuticos observados6,13,19,20. También el estudio controlado aleatorizado de Mitropoulos et al.21 sugiere que la estimulación mecánica/biofísica tiene el potencial de mejorar la disfunción endotelial microvascular en pacientes con ES. En este sentido, es posible que las fuerzas hemodinámicas generadas por la TG induzcan la síntesis y liberación de otras sustancias biológicamente activas, factores de crecimiento y citoquinas y modulen la expresión génica endotelial, en analogía con los efectos del estrés de cizallamiento sobre el endotelio6.
Desde 1990, la TG se aplica en Uruguay para el tratamiento de la ES y ha demostrado mejorar el FR, la microcirculación, las UD y la esclerosis cutánea11,12,22,23. En los estudios realizados, los pacientes mostraron un aumento en la amplitud de la onda de pulso, reducción del dolor isquémico, de la frecuencia y gravedad de los ataques del FR y se produjo curación de UD, lo que evitó, en casos graves, la amputación digital, el uso de analgésicos opioides y la hospitalización11,12,22,23. También mejoró el color de la piel, la temperatura, la sensibilidad y la movilidad (debido a la reducción del edema en las manos)11-12. La TG ha demostrado mejorar la esclerosis cutánea también en pacientes con morfea24, y se ha descrito mejoría post-TG de los síntomas digestivos, como la apertura bucal, la esofagitis leve y la hipomotilidad esofágica en pacientes con ES25.
Es un tratamiento seguro y bien tolerado, en pacientes de un amplio rango etario, sin efectos secundarios significativos en las condiciones aplicadas. El protocolo de hipergravedad se ajusta (número de sesiones, nivel máximo de g alcanzado) según la tolerancia, la edad y las características clínicas del paciente6. Pueden ocurrir mareos o náuseas transitorios cuando el paciente aún no está acostumbrado al procedimiento, o infrecuentemente vómitos/mareos relacionados con el movimiento de la cabeza durante la centrifugación (efectos de Coriolis)6. El entrenamiento del paciente es importante para una mejor tolerancia y continuidad del tratamiento.
Dada la amplia experiencia existente en Uruguay en TG y su eficacia en la ES, con un excelente perfil de seguridad, disponibilidad y bajo costo, sumado a que se trata de una opción terapéutica poco difundida en la comunidad científica, se realiza este trabajo de investigación, que podría aportar beneficios científicos, sanitarios y económicos futuros.
ObjetivoEvaluar la eficacia de la TG en la afección cutánea y vascular, en la calidad de vida y en la capacidad funcional, y su perfil de seguridad en pacientes con ES.
MetodologíaDiseño del estudioEstudio descriptivo, retrospectivo, de una cohorte de pacientes con ES asistidos en la unidad de enfermedades autoinmunes sistémicas (UEAS) del Hospital Militar, centro de referencia en autoinmunidad de Montevideo, Uruguay.
Pacientes y variablesCriterios de inclusión: pacientes mayores de 18años, con diagnóstico confirmado de ES (criterios ACR/EULAR 2013)26, tratados con TG (mínimo 10 sesiones) durante el período abril 2013-abril 2023.
Criterios de exclusión: no consentimiento en participar, superposición con otras enfermedades autoinmunes sistémicas (EAS). Los datos se obtuvieron de la revisión de la historia clínica de los pacientes. Las variables de eficacia cutánea y vascular, calidad de vida y capacidad funcional se compararon entre sí, antes y después de la TG.
Para evaluación de la eficacia cutánea se registró: el puntaje de Rodnan modificado (mRSS) en 17 áreas27 y su variación pre/post-TG. Se consideró como mRSS inicial (pre-TG) el registrado en la sesión 0 de la TG y mRSS final (post-TG) el correspondiente al mayor número de sesiones con respecto a la sesión0. Se exploró la correlación entre la variación del mRSS pre/post-TG y la extensión cutánea, el perfil inmunológico y los años de evolución de la ES (al iniciar la TG). También se registró presencia/ausencia/mejoría de puffy fingers, esclerodactilia, pitting scars y telangiectasias. Los pacientes sin datos completos de mRSS pre y/o post-TG y con ES sin esclerodermia fueron excluidos del análisis de eficacia cutánea. La extensión cutánea de la ES se clasificó en limitada (Escl), difusa (Escd) o ES sine esclerodermia según criterios de Le Roy28.
Perfil de anticuerpos (AC): determinación de AC antinucleocitoplasmáticos (ANA) por inmunofluorescencia indirecta sobre células Hep-2 (se consideraron positivos títulos mayores a 1/80)29. Con ANA positivos, se determinaron los AC específicos por técnica de ELISA: anti ADN, anticitoplasma de neutrófilos (ANCA), y por inmunoblot: anti- RNP/SM, anti ADN, anti-Smith, anti-ribonucleoproteínas (anti-RNP), anti-Ro 60 (SS-A), anti-Ro 52 (SS-A), anti-La, anti-Jo1 y los específicos para ES, anti-topoisomerasaI (anti-Scl 70) y anti-centrómero. Otros AC específicos para ES30 y los asociados a síndrome de solapamiento con esclerodermia30 no están disponibles en el prestador de salud. Se incluyeron en la categoría «otros AC de interés» a los antifosfolipídicos (anticardiolipina, anti-beta 2-glucoproteína1 por técnica de ELISA y anticoagulante lúpico por técnicas coagulométricas), anti-péptido citrulinados, factor reumatoide y ANCA.
Para la evaluación de la eficacia vascular se consideraron: la gravedad del FR (según escala de Taylor-Pelmear)31, el número de UD, lesiones necróticas y de amputaciones, así como también el dolor de causa vascular, medido por una escala visual analógica (EVA) de 0 a 10 realizada por los pacientes.
Para evaluación de la calidad de vida y de la capacidad funcional se utilizaron las escalas Cochin Hand Function Score (CHFS)32 y la Mouth Handicap in Systemic Sclerosis (MHISS)33 validadas en ES. Para complementar la evaluación de calidad de vida y capacidad funcional, se elaboró un cuestionario, autogestionado y anónimo (cuestionario sobre TG), con resultados reportados por los pacientes (RRP) sobre los beneficios de la TG. También incluyó preguntas sobre tolerancia al tratamiento y adherencia al mismo (Suplementario I).
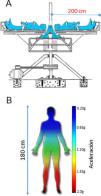
Terapia gravitacionalLa TG fue realizada por especialistas del Centro de Terapia Gravitacional (CTG) de Montevideo. Los pacientes fueron expuestos a perfiles de aceleración/desaceleración (+Gz) (gradiente de niveles g de la cabeza a los pies) de 0 hasta 1,5-2,5g a nivel de los pies (fig. 1) con un inicio rápido hasta el pico de aceleración y una rápida desaceleración posterior. El protocolo de TG fue ajustado según la tolerancia de cada paciente. La duración promedio del protocolo fue de 1hora, 1-3 veces/semana, hasta completar 20 sesiones. En algunos casos se realizó una terapia de mantenimiento (10-20 sesiones al año), según su situación clínica. En todos los pacientes se mantuvo su tratamiento farmacológico habitual.
Dibujo de la centrífuga humana del Centro de Terapia Gravitacional y gradientes+Gz. A)Centrífuga de casi 2 metros de diámetro utilizada para las sesiones de TG en el Centro de Terapia Gravitacional en Montevideo, Uruguay. Máximo 4 pacientes en una sesión. B)Ejemplo de un gradiente de gravedad sobre un paciente de 180cm de altura expuesto a un máximo de 2g a nivel de los pies en un sistema de 2m de diámetro. Adaptado de: Isasi et al., 2022, doi: 10.3389/fphys.2022.952723.
En las variables cuantitativas se realizó la comparación de medias con la prueba t-test, una vez testeadas la homogeneidad de varianza y normalidad de los datos. Se aplicó el test de McNemar para identificar si existen diferencias entre las proporciones de las muestras pareadas. En las variables cualitativas se emplearon distribuciones de frecuencia (número y porcentaje sobre total de pacientes). Se utilizaron los softwares Rstudio (versión 2022.07.2) y R para Windows (versión R-4.2.1).
ResultadosSe incluyeron un total de 50 pacientes. Predominaron las mujeres (96%), la raza blanca (98%), y la edad media de la cohorte fue de 62±12 años. Las características demográficas, el tiempo de evolución de la ES al inicio de la TG y al momento de inclusión en el estudio, la extensión cutánea y el perfil inmunológico de los pacientes se muestran en la tabla 1.
Características demográficas, tiempo de evolución, extensión cutánea y perfil inmunológico de los pacientes con esclerosis sistémica incluidos en el estudio
| Característica | N.° pacientes (%) |
|---|---|
| Total | 50 |
| Género (mujeres/hombres) | 24/1 (96/4) |
| Edad al estudio (años) | 62±12 |
| Raza | |
| Caucásicos | 49 (98) |
| Afrodescendientes | 1 (2) |
| Duración ES a la inclusión en el estudio (años) | 6,8±3,2 |
| Duración ES al inicio de TG (años) | 2,8±3,2 |
| Perfil inmunológico: (n=43) | |
| Grupo ANA positivoa | 10 (20) |
| Grupo anti centrómero positivo | 15 (30) |
| Grupo Scl70 positivo | 11 (22) |
| Grupo ANA negativo | 7 (14) |
| Extensión cutánea (n=49) | |
| Difusa (EScd) | 20 (40) |
| Limitada (EScl) | 26 (52) |
| Sine esclerodermia (sine) | 3 (6) |
Grupo ANA positivo incluye: pacientes ANA positivos, anti centrómero y anti-Scl70 negativos. Grupo ANA negativo incluye: pacientes ANA, anti centrómero y anti-Scl70 negativos. Los pacientes anti-centrómero positivos asociaron: EScl (11), EScd (2), sine (2). Los pacientes Scl70 positivos asociaron: EScl (3), EScd (7), ninguno sine. Pacientes Scl70 y anti-centrómero negativos asociaron: EScl (7), EScd (7), sine (1). Pacientes Scl70 y anti-centrómero positivos asociaron: EScl (2). Excluidos del análisis 8 pacientes por datos incompletos.
Las variables cualitativas están expresadas en número y/o porcentaje, y las cuantitativas, con la media±desviación estándar.
ES: esclerosis sistémica.
No se registraron efectos adversos significativos durante el tratamiento.
Análisis de la eficacia cutáneaPara este análisis se excluyeron 3 pacientes sine esclerodermia y 22 sin datos pre y/o post TG. En total se analizaron 25 pacientes. Post TG se observó una mejoría significativa del mRSS (pre-TG 19,2±8,7 vs post-TG 5,4±5,0 puntos, t-test, p<0,05), reducción promedio mRSS post vs pre-TG: 13,8±5,7 puntos (tabla 2, fig. 2). El 75% de los pacientes mejoraron el mRSS en 11 puntos o más. El tiempo medio para completar 20 sesiones de TG fue de 137,2±99,3 días. La reducción media del mRSS en los pacientes que recibieron 10 sesiones fue de 8,8 puntos vs 13,1 en los que se realizaron 20 sesiones. La reducción del mRSS post-TG fue mayor en los pacientes con mRSS iniciales más altos (R=0,84, p<0,05) (fig. 3). El valor de la variación del mRSS pre/post-TG no tuvo relación significativa con el tiempo de evolución de la ES al inicio de la TG (<1año, 1-4años, >4años), con el perfil inmunológico de los pacientes ni con la extensión cutánea de la ES. En los RRP, 36/38 (95%) de los pacientes que completaron el cuestionario reportaron mejoría a nivel cutáneo, el 87% responden que mejoró bastante o mucho y el 8% que mejoró poco. Por otro lado, se observó una mejoría significativa del número de pacientes con puffy fingers (pre-TG 25/50 [50%] vs post-TG 10/50 [20%], McNemar test, p<0,05), pero no en la frecuencia de pacientes con telangiectasias, pitting scars o esclerodactilia (tabla 3).
Puntaje de Rodnan modificado (mRSS) pre y post terapia gravitacional y su variación
| n | Q25 | media | Q75 | DE | min | máx | |
|---|---|---|---|---|---|---|---|
| Pre-TG | 25 | 15 | 19,2 | 24 | 8,7 | 2 | 37 |
| Post-TG | 25 | 2 | 5,4 | 8 | 5,0 | 0 | 19 |
| Variación | 25 | 11 | 13,8 | 17 | 5,7 | 0 | 23 |
Se observa una disminución significativa del mRSS, pre-TG 19,2±8,7 y post-TG 5,4±5,0 (t-test, p<0,05). La reducción promedio mRSS post vs pre TG fue de 13,8±5,7 puntos.
Valores del puntaje de Rodnan modificado (mRSS) pre y post-terapia gravitacional. Veinticuatro pacientes (96%) mejoraron el mRSS post-TG (los puntos se sitúan por debajo de la línea x=y), excepto un paciente (4%), que no presentó cambios. Además, el 75% de los pacientes mejoraron el mRSS en 11 puntos o más.
Comparación entre el puntaje de Rodnan modificado (mRSS) pretratamiento y su variación. Se observa una correlación significativa entre la magnitud de la reducción del mRSS (post-TG - pre-TG) y el valor inicial pre-TG (R=0,84, p<0,05). La reducción del mRSS fue mayor en los pacientes con mRSS iniciales más altos.
Efectos de la terapia gravitacional en puffy fingers, esclerodactilia, pitting scars y telangiectasias
| Signo clínico | Momento del registro | N.° de pacientes (%) |
|---|---|---|
| Puffy fingers | ATG | 25 (50) |
| DTG | 10 (20) | |
| Esclerodactilia | ATG | 36 (72) |
| DTG | 33 (66) | |
| Pitting scars | ATG | 5 (10) |
| DTG | 2 (4) | |
| Telangiectasias | ATG | 15 (30) |
| DTG | 10 (24) |
Se observa una mejoría significativa del número de pacientes con puffy fingers (pre-TG 50% vs post-TG 20%, McNemar test, p<0,05), pero no en telangiectasias, pitting scars o esclerodactilia.
ATG: antes de terapia gravitacional; DTG: después de terapia gravitacional; n=50 pacientes.
Se observó una disminución significativa en la severidad del FR en gran parte de los pacientes, la mayoría con FR grave al inicio: FR pre-TG grado 3-4, 43/48 (89,6%) pacientes vs post-TG, grado ≤2, 42/47 (89,4%) pacientes. En total, 38/48 (81%) de los pacientes mejoraron el grado de FR, mientras que 9 no registraron cambios. Por lo tanto, la probabilidad de tener FR grave grado 3-4 disminuye post-TG (McNemar test, p<0,05) (tabla 4). Desde la perspectiva del paciente, 32/35 (91%) de los pacientes reportan mejoría del FR, el 74% responden que mejoró bastante o mucho y el 17%, que mejoró poco. Por otro lado, se observó una notoria mejoría en el dolor vascular cuantificado por EVA (pre-TG, 7,6±2,2, post-TG, 1,4±1,2, p<0,05). Los RRP reportan mejoría significativa en el dolor vascular y también en el dolor articular/muscular (tabla 5). Con respecto a las UD, pre-TG, 7 pacientes presentaban 15 dedos con isquemia crítica, post-TG, 5 lograron curación completa de dedos y 2 pacientes curación parcial (1amputación c/u). En total, hubo mejoría de UD en 11 dedos (tabla 4, fig. 4).
Efecto de la terapia gravitacional en el fenómeno de Raynaud, las úlceras digitales y el dolor vascular
| N.° de pacientes (%) | ||
|---|---|---|
| Gravedad del FR | ATG | G 0: 1 (2)G 1: 1 (2)G 2: 3 (6,2)G 3: 35 (72,9)G 4: 8 (16,7) |
| DTG | G 0: 13 (27,7)G 1: 21 (44,7)G 2: 8 (17)G 3: 0G 4: 1 (2,1) | |
| Úlceras digitales | ATG | 7 (14,5) |
| DTG | 0 | |
| Media±DE | ||
| Dolor vascular por EVA | ATG | 7,6±2,2 |
| DTG | 1,4±1,2 |
Las variables cuantitativas se expresan como media±desviación estándar, y las cualitativas, como número (porcentaje).
ATG: antes de terapia gravitacional; DTG: después de terapia gravitacional; EVA: escala visual analógica. 2 pacientes sin datos ATG y 7 pacientes sin datos DTG; FR: fenómeno de Raynaud.
Se observa una disminución significativa en la severidad del FR en la mayoría de los pacientes (la mayoría con FR grave al inicio): pre-TG grado 3-4, 43 (89,6%) de pacientes vs post-TG, 46 (89,4%) grado ≤2, McNemar test, p<0,05), así como del dolor vascular medido por EVA: pre-TG, 7,6±2,2, post-TG, 1,4±1,2, p<0,05).
Resultados reportados por los pacientes en un cuestionario de terapia gravitacional
| Variable | Mejoría (% de pacientes) |
|---|---|
| Calidad de vida | 97 |
| Fenómeno de Raynaud | 89,5 |
| Piel | 95 |
| Capacidad para AVD | 89,5 |
| Estado de ánimo | 65 |
| Trastornos del sueño | 37 |
| Otras variables | % pacientes |
|---|---|
| Dolor vascular (EVA > 4), pre-TG | 65 |
| Dolor vascular (EVA ≤ 4), post-TG | 84a |
| Dolor muscular/articular (EVA > 4), pre-TG | 60 |
| Dolor muscular/articular (EVA ≤ 4), post-TG | 74a |
| Tolerancia a TG «buena» | 100% |
| Adherencia al 100% de las sesiones | 87% |
AVD: actividades de la vida diaria.
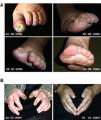
Efecto de la terapia gravitacional en lesiones vasculares digitales de pacientes con esclerosis sistémica. A)Imágenes del efecto de la TG sobre una úlcera digital de un miembro inferior izquierdo al inicio y su evolución con la TG en un paciente con ES. B)Evolución de la necrosis digital en una paciente con enfermedad mixta del tejido conectivo al inicio (izquierda) y post-TG (derecha). Estas imágenes no corresponden a pacientes de este estudio. Adaptado de: Isasi et al., 2022, doi: 10.3389/fphys.2022.952723. Fotos cortesía del Centro de Terapia Gravitacional.
Se registró disminución del CHFS y del MHISS (valor promedio pre TG: 10,1 y 9,9, respectivamente (21 pacientes), y valor promedio post-TG: 7,9 y 8,1, respectivamente (9 pacientes). Los RRP muestran que 34/38 (89%) de los pacientes reportan mejoría en la capacidad para realizar actividades de la vida diaria y 37/38 (97%) de los pacientes reportan mejoría en la calidad de vida. La tabla 5 resume los RRP de 38 pacientes que completaron el cuestionario de TG.
Discusión y conclusionesLa TG mejoró de forma significativa el compromiso cutáneo en pacientes con ES, como ya se había demostrado en los estudios previos de Isasi et al.11,12,23. El beneficio es mayor cuanto más sesiones se realizan, lo que surge de la comparación en la disminución del mRSS según se realicen 10 o 20 sesiones. No obstante, la mejoría cuando aparece es precoz, y ya se observa en las primeras 10 sesiones, como se ha publicado previamente11,12. El tiempo en el que se alcanzaron los resultados (20 sesiones) fue relativamente corto (poco más de 4 meses). Aunque no fue un objetivo de este estudio el seguimiento de los pacientes a largo plazo, el mantenimiento en el tiempo de la mejoría del mRSS post-TG es variable, lo que se evidencia en la revisión de las historias clínicas y según la opinión de expertos del CTG; por lo tanto, la indicación de TG anual de mantenimiento debe individualizarse. Los pacientes con los mRSS iniciales más altos fueron los que presentaron mayor reducción del mRSS post-TG, probablemente por su mayor capacidad de mejoría debido a un compromiso cutáneo más extenso, y a expensas de mejorar las áreas cutáneas con menor compromiso fibrótico. El mRSS inicial y su variación post-TG no estuvieron relacionados con el tiempo de evolución de la ES al inicio de la TG, ni con el perfil inmunológico de los pacientes o la extensión cutánea de la enfermedad. Esto debe interpretarse con cautela, ya que el número de pacientes con mRSS presentados en este estudio es reducido, no existen investigaciones previas completas de pacientes con ES tratados con TG que permitan comparar los resultados de este estudio con otras cohortes, y tampoco se incluyó en este análisis un grupo de pacientes control (sin TG).
Se registró una mejoría significativa del número de pacientes con puffy fingers, siendo la disminución del edema de manos un hecho reportado previamente por Isasi et al.12. Sin embargo, la TG no influyó en la frecuencia de pacientes con esclerodactilia, pitting scars o telangiectasias.
A nivel vascular, la gravedad del FR disminuyó de forma significativa post-TG en la mayoría de los pacientes. Por otro lado, hubo curación de UD, lo que evitó la hospitalización y la eventual amputación digital, así como tampoco fue necesaria la utilización de vasodilatadores como las prostaciclinas intravenosas, no disponibles en Uruguay. Los pacientes mejoraron significativamente el dolor isquémico, lo que disminuyó el uso de analgésicos opiáceos. Estos resultados son similares a los ya reportados previamente11,12. La capacidad funcional medida por CHFS y MHISS mejoró, si bien el número de pacientes que contaban con estos datos fue reducido.
En los RRP, la mayoría de los pacientes informaron mejoría a nivel cutáneo, en el FR, en el dolor isquémico y articular/muscular (mejoría estadísticamente significativa), y surgen otros datos, como la mejoría en el estado de ánimo y trastornos del sueño, reportada en un menor número de pacientes. Todos estos beneficios necesariamente repercuten en la calidad de vida y en la capacidad funcional, y así fue manifestado por la mayoría de los pacientes en el cuestionario TG. En este estudio no se registraron efectos adversos significativos, similar a lo observado en el CTG, incluso con seguimientos de pacientes por más de 20 años. Esto también se ve reflejado en el cuestionario sobre TG, en el cual la totalidad de los pacientes expresaron buena tolerancia al tratamiento y una elevada adherencia al mismo.
Si bien este estudio presenta limitaciones dado su diseño descriptivo y retrospectivo y la ausencia de un grupo control de pacientes con ES, no tratados con TG, los resultados son muy auspiciosos. Tampoco se analizó el efecto del tratamiento farmacológico en los resultados, lo que podrá ser un punto de partida para futuras investigaciones.
Este trabajo de investigación contribuye a la difusión de la TG y sus resultados, que coinciden con los beneficios observados en la práctica clínica diaria y con los relatados por los pacientes. Son necesarios ensayos clínicos controlados y aleatorizados, que comparen los efectos de la TG vs tratamiento farmacológico convencional. Además, es necesaria más investigación básica para desentrañar los mecanismos biológicos y las bases celulares y moleculares de la mejoría clínica, así como para su validación internacional y su uso generalizado.
ConclusionesLa TG mejoró el compromiso cutáneo y vascular, la calidad de vida y la capacidad funcional en pacientes con ES con un excelente perfil de seguridad. Se necesitan ensayos clínicos controlados y aleatorizados para corroborar estos resultados observacionales.
FinanciaciónLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
Contribución de los autoresL.F.S., E.I., M.E.I.: concepción y diseño del trabajo, recolección de datos, análisis e interpretación de datos y resultados, análisis estadístico, redacción del manuscrito, revisión crítica del manuscrito. AP, S.P.: recolección de datos.
Conflicto de interesesL.F.S. es médica e investigadora independiente. E.I. y M.E.I. son socias de ISASI CENTER.SRL (Centro de Terapia Gravitacional). S.P y A.P son médicas del CTG. Los autores declaran la no existencia de conflicto de intereses.