Los pacientes con artritis reumatoide (AR) pueden presentar un número amplio de complicaciones, siendo de especial importancia las de etiología infecciosa. Su elevada incidencia está muy ligada al uso de inmunosupresores.
El espectro de agentes causantes de infecciones oportunistas en pacientes con AR es muy amplio; sin embargo, son relativamente escasos los casos de infección por Leishmania, especialmente en pacientes sin tratamiento con fármacos biológicos.
A large number of complications have been associated with rheumatoid arthritis (RA), those of infectious etiology being of special relevance. Their high incidence is closely linked to the use of immunosuppressive medication.
The spectrum of agents causing opportunistic infections in patients with RA is very broad; however, there are relatively few cases of Leishmania infection, especially in patients not being treated with biological drugs.
La leishmaniasis es una infección protozoaria intracelular causada por la picadura de un díptero. El desarrollo de la enfermedad depende de la virulencia del parásito y de factores de riesgo del huésped, fundamentalmente el estado de su sistema inmunitario. Los pacientes que presentan artritis reumatoide (AR) son tratados de forma crónica con metotrexato y otros inmunosupresores, y presentan por ello mayor riesgo de desarrollar infecciones1. El espectro de infecciones oportunistas en estos pacientes es muy amplio, sin embargo, son raros los casos de leishmaniasis, especialmente en pacientes en tratamiento solo con metotrexato.
Caso clínicoVarón de 84 años, residente de un área del sur de Madrid (perteneciente a un área con elevada población de conejos), con antecedentes personales de hipertensión arterial, diabetes mellitus, dislipidemia, insuficiencia cardiaca con fibrilación auricular, con implantación de marcapasos debido a un bloqueo auriculoventricular de tercer grado, diagnosticado hace 6 años de AR con factor reumatoide positivo, anticuerpos antipéptido cíclico citrulinado positivos, en tratamiento con metotrexato 15mg semanales, con buena respuesta clínica. Ingresa por fiebre, tiritona y escalofríos de una semana de evolución. En la exploración física se objetivan leves crepitantes bibasales. No se observan adenopatías, visceromegalias ni otros datos de focalidad infecciosa. Analíticamente, presenta pancitopenia (hemoglobina de 10,9 g/dl, 2.050 leucocitos con 1.310 neutrófilos/μl y 49.000 plaquetas/μl), proteína C reactiva (PCR) de 104mg/l y velocidad de sedimentación globular de 110mm/h. Inicialmente, se sospechó toxicidad medular por metotrexato, con probable sobreinfección bacteriana.
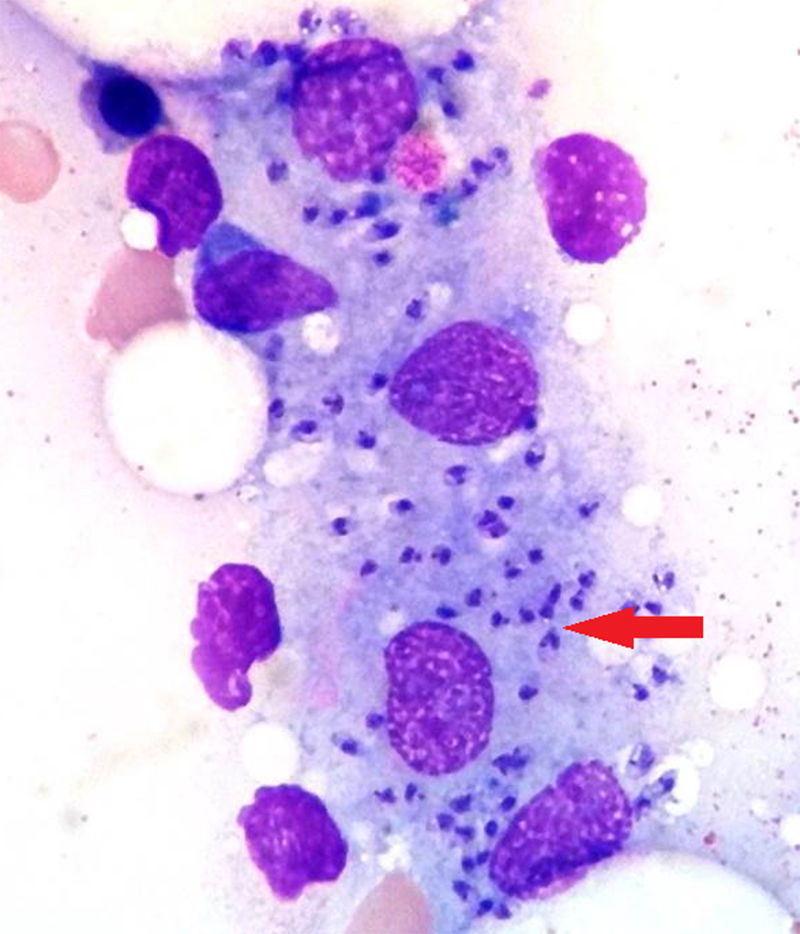
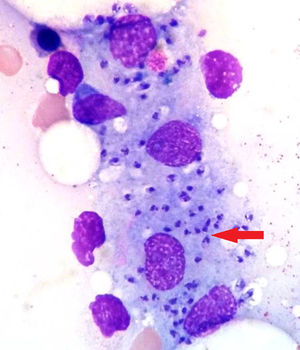
Se suspendió el metotrexato y se solicitaron diversas pruebas microbiológicas (hemocultivos, urocultivo, cultivo de esputo, serologías víricas y bacterianas) y de imagen (tomografía computarizada toraco-abdominal, ecocardiografía transtorácica y transesofágica), siendo todas no diagnósticas para el cuadro actual del paciente. Se inició tratamiento con ácido folínico y antibióticos empíricos de amplio espectro. Ante la persistencia de la fiebre y la pancitopenia, se realizó una biopsia de médula ósea diagnóstica de leishmaniasis visceral (fig. 1). La serología para Leishmania resultó positiva (título de 1/640) y también la reacción en cadena de la polimerasa (PCR) en la biopsia de médula y en sangre periférica. Por el contrario, el cultivo en sangre periférica fue negativo. Se inició tratamiento con anfotericina B liposomal 200mg IV inicialmente cada 4 días hasta alcanzar una dosis acumulada de 2.400mg. Tras finalizar el tratamiento, el paciente presentó recuperación de la pancitopenia, disminución de los títulos de anticuerpos y la PCR en sangre permaneció negativa.
DiscusiónLa leishmaniasis es una zoonosis causada por más de 20 especies de protozoos intracelulares del género Leishmania. La transmisión se produce por la picadura de un díptero hembra infectado (géneros Phlebotomus y Lutzomya). Los mamíferos actúan como reservorios, siendo los más importantes en nuestro medio los perros y los roedores.
La infección puede ser asintomática, cutánea localizada o diseminada (mucocutánea o visceral). Según la Organización Mundial de la Salud, cada año se producen entre 900.000 y 1,3 millones de nuevos casos en todo el mundo; de estos, entre 200.000 y 400.000 presentan la forma visceral. En la cuenca del Mediterráneo la infección se debe a la Leishmania infantum (Leishmania donovani complex), responsable de la forma visceral. Esta se caracteriza por fiebre, pérdida de peso, hepatoesplenomegalia y pancitopenia. El desarrollo de la enfermedad depende de la agresividad del parásito y de los factores de riesgo del huésped, como la inmunodepresión. La activación de la respuesta inmunitaria celular específica de los linfocitos T helper 1 y la producción de citocinas activadoras de macrófagos como interferón gamma, interleucina 12 y factor de necrosis tumoral alfa (TNF-α) desempeñan un papel fundamental en la defensa contra la enfermedad. El metotrexato inhibe la quimiotaxis de los neutrófilos y la proliferación de linfocitos T, disminuyendo la activación de los macrófagos y la respuesta contra el parásito.
El diagnóstico puede realizarse en muestras titulares (piel, bazo, médula ósea o ganglios linfáticos) por visualización directa del parásito, cultivo o cuantificación del DNA por PCR. En sangre periférica se realiza PCR y detección de anticuerpos mediante ELISA o inmunofluorescencia indirecta1.
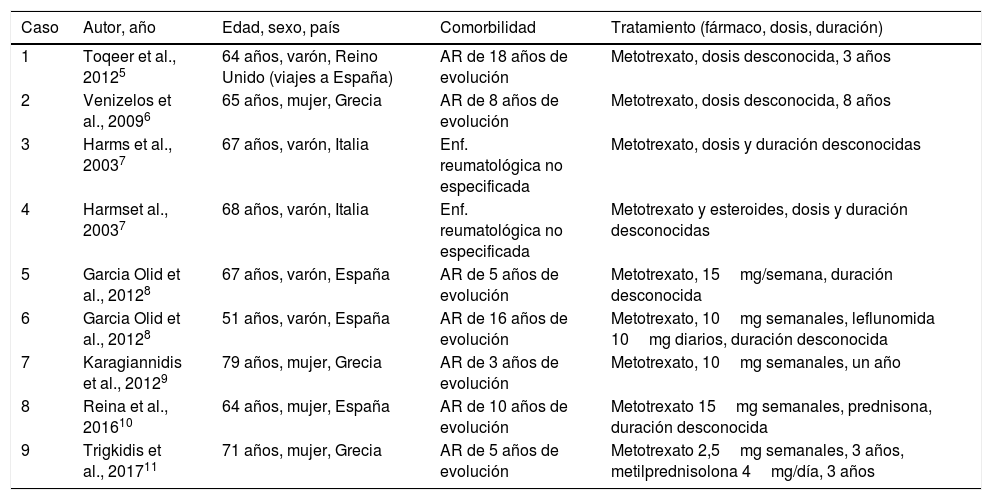
ConclusionesLa AR afecta al 0,5-1% de la población mundial y la mayoría de los pacientes son tratados con metotrexato2. Se han descrito múltiples casos de leishmaniasis visceral en pacientes con AR con terapia biológica, especialmente en tratamiento con anti-TNF, pero tras una revisión de la literatura solo encontramos 9 casos publicados en pacientes tratados únicamente con metotrexato, casi todos del área mediterránea (tabla 1), y dada la escasa casuística, es difícil establecer un subgrupo de pacientes con mayor susceptibilidad para el desarrollo de la infección.
Casos descritos en la literatura de leishmaniasis visceral en pacientes tratados con metotrexato
| Caso | Autor, año | Edad, sexo, país | Comorbilidad | Tratamiento (fármaco, dosis, duración) |
|---|---|---|---|---|
| 1 | Toqeer et al., 20125 | 64 años, varón, Reino Unido (viajes a España) | AR de 18 años de evolución | Metotrexato, dosis desconocida, 3 años |
| 2 | Venizelos et al., 20096 | 65 años, mujer, Grecia | AR de 8 años de evolución | Metotrexato, dosis desconocida, 8 años |
| 3 | Harms et al., 20037 | 67 años, varón, Italia | Enf. reumatológica no especificada | Metotrexato, dosis y duración desconocidas |
| 4 | Harmset al., 20037 | 68 años, varón, Italia | Enf. reumatológica no especificada | Metotrexato y esteroides, dosis y duración desconocidas |
| 5 | Garcia Olid et al., 20128 | 67 años, varón, España | AR de 5 años de evolución | Metotrexato, 15mg/semana, duración desconocida |
| 6 | Garcia Olid et al., 20128 | 51 años, varón, España | AR de 16 años de evolución | Metotrexato, 10mg semanales, leflunomida 10mg diarios, duración desconocida |
| 7 | Karagiannidis et al., 20129 | 79 años, mujer, Grecia | AR de 3 años de evolución | Metotrexato, 10mg semanales, un año |
| 8 | Reina et al., 201610 | 64 años, mujer, España | AR de 10 años de evolución | Metotrexato 15mg semanales, prednisona, duración desconocida |
| 9 | Trigkidis et al., 201711 | 71 años, mujer, Grecia | AR de 5 años de evolución | Metotrexato 2,5mg semanales, 3 años, metilprednisolona 4mg/día, 3 años |
Entre 2009 y 2012 hubo un brote de leishmaniasis en la Comunidad de Madrid, con 446 afectados. De los 160 pacientes con leishmaniasis visceral, 25 estaban en tratamiento inmunosupresor3,4.
En conclusión, la presencia de fiebre y pancitopenia en un paciente con inmunodepresión celular en un área endémica obliga a descartar leishmaniasis. La terapia exclusiva con metotrexato (sin tratamientos biológicos) en la AR puede ser suficiente para aumentar el riesgo de esta infección. La biopsia de médula ósea permite realizar el diagnóstico de leishmaniasis visceral, así como descartar otras causas de pancitopenia1.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Al servicio de Hematología del Hospital Ramón y Cajal, por su colaboración.