El plasma rico en plaquetas (PRP) es una novedosa herramienta terapéutica que ha revolucionado el mundo de la medicina deportiva y la traumatología debido a éxitos terapéuticos mediáticos en deportistas de élite. Sujeto a continuo debate, el PRP se perfila en el espectro de las terapias musculoesqueléticas con múltiples cualidades que potencialmente lo hacen idóneo para su uso en la consulta de reumatología: efectividad, seguridad, fácil manejo y bajo coste. ¿Es el PRP un nuevo producto de la mercadotecnia? o, por el contrario, es una herramienta con fundamento que debe incluirse en el arsenal terapéutico del reumatólogo. En la siguiente revisión se repasarán en detalle su fundamento, preparación y regímenes de administración. Se reflexionará sobre potenciales efectos adversos y, por último, se realizará un análisis crítico de la evidencia científica que avala su posible uso en la consulta de reumatología.
Platelet Rich Plasma (PRP) is a novel therapeutic tool that has revolutionized the world of sports medicine and trauma due to therapeutic success shown in the media. Subject to ongoing debate, the PRP is outlined along a spectrum of musculoskeletal therapies with many qualities that make it ideal for use in the rheumatology: effectiveness, safety, easy handling and low cost. Is PRP a product of marketing? Or, conversely, is an interesting tool to consider in the armamentarium of the rheumatologist. In the following review we will analyze in detail its principles, preparation, and management regimes. We will reflect on potential adverse effects and, finally, there will be a critical analysis of the scientific evidence that supports its potential use in the rheumatology clinic.
El plasma rico en plaquetas (PRP) es una novedosa herramienta terapéutica de naturaleza autóloga que ha surgido con fuerza en los últimos años debido a mediáticos éxitos terapéuticos en deportistas de élite1. Famosos jugadores profesionales de fútbol americano, Tiger Woods o el mismo Rafael Nadal deben, en parte, sus «milagrosas» recuperaciones deportivas al empleo de este enigmático tratamiento bautizado como «fenómeno PRP». El PRP es un tratamiento poco conocido en el ambiente reumatológico pero bastante destacado en los congresos de traumatología y medicina deportiva en los que, a pesar de la controversia que suscita, progresivamente despierta un creciente interés debido a su supuesta eficacia y aparente inocuidad2. Su diana terapéutica comprende eminentemente las tendinopatías y entesopatías crónicas, si bien su abanico de indicaciones está en continua expansión aplicándose con éxito a múltiples dolencias, entre ellas, a la osteoartritis de rodilla. Su bajo coste, su fácil manejo, su utilidad en procesos patológicos esquivos a los tratamientos convencionales y su aparente inocuidad hacen del PRP una seductora alternativa terapéutica a considerar en el arsenal terapéutico del reumatólogo.
En la siguiente revisión se pretende analizar lo que se ha dado en llamar el «fenómeno PRP», para lo cual se repasará en detalle el fundamento para su empleo, la preparación y los regímenes de administración. Igualmente, se someterán a discusión y análisis crítico su perfil de seguridad y la evidencia científica que avala su uso con el fin de someter a consideración su posible utilidad en la consulta de reumatología.
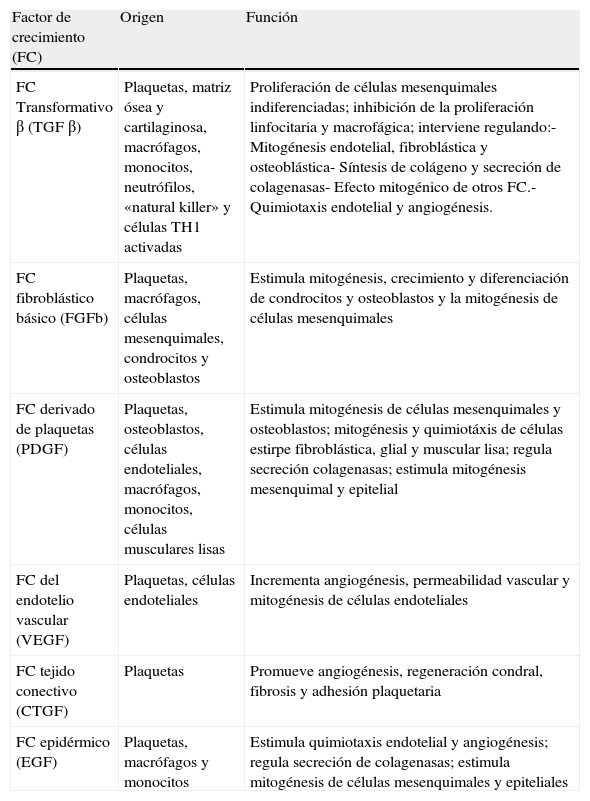
FundamentoEl PRP debe su interés terapéutico al papel instrumental decisivo de las plaquetas en el proceso de curación y reparación de la herida tisular. Este papel reparador no está relacionado con las plaquetas por sí mismas sino, más bien, con los factores de crecimiento (FC) liberados por sus gránulos α, poseedores de múltiples propiedades regeneradoras (tabla 1). La reparación de la herida tisular es un proceso complejo en el que coexisten, secuencial y solapadamente, una gran variedad de funciones celulares como la quimiotaxis, la angiogénesis, la proliferación celular, la formación de matriz extracelular y la «limpieza» macrofágica. Estas funciones forman un complejo entramado en el que clásicamente se distinguen 3 fases relativamente bien diferenciadas: inflamación, proliferación y remodelado3–7. Todos los FC contenidos en el PRP intervienen en alguna de las fases descritas, pero todavía se desconoce con exactitud la totalidad de sus funciones. Se especula con un papel preponderante de algunos de estos4, pero es concebible que el protagonismo individual de cada uno varíe en función del tipo de herida tisular (rotura, inflamación, degeneración, etc.) y del tipo de tejido (tendón, músculo, hueso, etc.).
Factores de crecimiento contenidos en el plasma rico en plaquetas
| Factor de crecimiento (FC) | Origen | Función |
| FC Transformativo β (TGF β) | Plaquetas, matriz ósea y cartilaginosa, macrófagos, monocitos, neutrófilos, «natural killer» y células TH1 activadas | Proliferación de células mesenquimales indiferenciadas; inhibición de la proliferación linfocitaria y macrofágica; interviene regulando:- Mitogénesis endotelial, fibroblástica y osteoblástica- Síntesis de colágeno y secreción de colagenasas- Efecto mitogénico de otros FC.- Quimiotaxis endotelial y angiogénesis. |
| FC fibroblástico básico (FGFb) | Plaquetas, macrófagos, células mesenquimales, condrocitos y osteoblastos | Estimula mitogénesis, crecimiento y diferenciación de condrocitos y osteoblastos y la mitogénesis de células mesenquimales |
| FC derivado de plaquetas (PDGF) | Plaquetas, osteoblastos, células endoteliales, macrófagos, monocitos, células musculares lisas | Estimula mitogénesis de células mesenquimales y osteoblastos; mitogénesis y quimiotáxis de células estirpe fibroblástica, glial y muscular lisa; regula secreción colagenasas; estimula mitogénesis mesenquimal y epitelial |
| FC del endotelio vascular (VEGF) | Plaquetas, células endoteliales | Incrementa angiogénesis, permeabilidad vascular y mitogénesis de células endoteliales |
| FC tejido conectivo (CTGF) | Plaquetas | Promueve angiogénesis, regeneración condral, fibrosis y adhesión plaquetaria |
| FC epidérmico (EGF) | Plaquetas, macrófagos y monocitos | Estimula quimiotaxis endotelial y angiogénesis; regula secreción de colagenasas; estimula mitogénesis de células mesenquimales y epiteliales |
El PRP se define como una fracción del plasma centrifugado que contiene una concentración de plaquetas superior a la de sangre periférica. Algunos autores son más precisos y consideran que la concentración plaquetaria del PRP debe aproximarse a cifras 5 veces superiores a las normales8. En realidad, se trata de una alícuota plasmática procedente de 20-30ml de sangre periférica que se centrifuga a 3.200 revoluciones por minuto durante 15min. El resultado son aproximadamente 2-3ml de plasma enriquecido en plaquetas con concentraciones variables pero, casi siempre, alrededor de 1×106 plaquetas. Opcionalmente, dicha alícuota puede ser activada con trombina o cloruro cálcico según su utilidad terapéutica futura. Cuando el PRP se destina a tratar lesiones de partes blandas, la mayoría de los autores no consideran necesaria la activación previa, debido a que esta se produce in situ al contacto con el colágeno tendinoso o con el propio coágulo de la rotura fibrilar9. Cuando el PRP se utiliza para facilitar osteointegración de implantes o cuando se usa para el tratamiento de la osteoartritis de rodilla suele preferirse cierta activación que, además, le confiere una consistencia gelatinosa que facilita su uso quirúrgico10.
Las dosis y regímenes de administración varían en función de la dolencia a tratar. En el caso de tendinopatías crónicas, la literatura parece consensuar una única administración para epicondilitis, tendinitis aquilea y fascitis plantar9,11,12. Sin embargo, serán 3 consecutivas (una cada 2 semanas) cuando se trate de una tendinopatía rotuliana crónica o «rodilla del saltador»13. Hay algunos autores que utilizan con frecuencia el PRP para el tratamiento del síndrome subacromial, especialmente cuando este es muy crónico o refractario. Sin embargo, no se dispone de información veraz que acredite una pauta de administración concreta. Recientemente se ha comunicado la utilidad del PRP para el tratamiento de la osteoartritis de rodilla. La mayoría de los autores están de acuerdo en que el número idóneo de infiltraciones en estos casos debe ser 3; sin embargo, no existe unanimidad acerca del intervalo de administración, reportando buenos resultados tanto con una periodicidad semanal, como trisemanal14,15.
SeguridadLa naturaleza autóloga del PRP parece ser el argumento principal por el cual la tolerancia a la infiltración es excelente, produciéndose en contadas ocasiones una leve reacción inflamatoria local. Tampoco se han comunicado casos de infección pospunción, dato que quizá pueda relacionarse con el efecto antimicrobiano del PRP sugerido por algunos autores16. Los adeptos al PRP aseguran reiteradamente que este carece de efectos indeseables debido a que se trata de un producto de naturaleza autóloga y, por tanto, «propio». Lo cierto es que estas afirmaciones solo se sustentan en sus propias experiencias, debido a que no se dispone de estudios de seguridad, ni tampoco de información contrastada procedente de ensayos clínicos. Es razonable pensar que la naturaleza autóloga del PRP facilite su tolerancia terapéutica, pero tolerancia no es sinónimo de inocuidad. El efecto terapéutico del PRP se consigue concentrando cantidades ingentes de FC en los tejidos dañados. Ya se ha mencionado que los FC promueven múltiples funciones celulares que, bien moduladas, pueden redundar en una aceleración del proceso reparativo tisular. Pero la reparación tisular no es el único proceso en el que estos factores intervienen decisivamente. El factor de crecimiento del endotelio vascular (VEGF), el factor de crecimiento fibroblástico básico, el factor de crecimiento hepatocitario (HGF) y el factor de crecimiento insulínico son factores de especial relevancia en el crecimiento de ciertos tumores debido a su elevado potencial angiogénico. Algunos FC, incluso, han exhibido un potencial oncogénico propio, capaz de favorecer la expansión clonal de células previamente mutadas o «iniciadas»’ y, también, de favorecer su inmortalización mediante la inhibición del ciclo apoptósico17–19. Estas propiedades de los FC, proclives a la generación y perpetuación de tumores, aunque inquietantes están solo descritas en animales de experimentación, no existiendo evidencias hasta el momento que relacionen el uso terapéutico del PRP en seres humanos con algún tipo de transformación carcinomatosa20.
Recientemente ha podido demostrarse que ciertos FC favorecen la proliferación o activación (in situ y periférica) de progenitores osteogénicos circulantes o «COP cells»21. Estas células indiferenciadas, de reciente descripción, son conocidos progenitores osteocondrales que están definitivamente implicados en la neoformación ósea extraesquelética, como la que ocurre en las osificaciones heterotópicas postartroplastia o en las calcificaciones valvulares22. Parece razonable pensar que, en presencia de un microambiente adecuado en la herida tisular, las concentraciones exageradas de FC contenidas en el PRP puedan favorecer un reclutamiento y activación supranormal de COP cells en el área de la infiltración con capacidad para desarrollar una calcificación u osificación heterotópica en partes blandas o a nivel intrarticular. Hasta la fecha, estas reflexiones no dejan de ser meras especulaciones ya que tampoco se han comunicado complicaciones de este tipo en la literatura.
Evidencias preclínicasTendón y músculoLa mayor parte de las evidencias preclínicas que apoyan el beneficio del PRP en las tendinopatías se fundamentan en su supuesta capacidad para estimular el proceso de reparación tisular. Los cultivos celulares aportan evidencias de que el PRP interviene en las distintas fases del proceso reparativo. En la fase de inflamación, los FC contenidos en el PRP son capaces de movilizar células inflamatorias circulantes hacia la herida tisular23. Igualmente, estimulan los tenoviocitos para secretar colágeno, VEGF y HGF, todos ellos, aceleradores del proceso reparativo24. En la fase proliferativa, el PRP es capaz de estimular la proliferación y división de casi todo tipo de células de estirpe mesenquimal (osteoblastos, fibroblastos, tenoviocitos o condrocitos) y, también, de células madre multipotenciales25,26. En la fase final de remodelado, el PRP facilita la maduración del colágeno recién formado y la apoptosis de las células en exceso27. En su conjunto, todas estas evidencias implican definitivamente al PRP en el proceso reparativo tisular, pero no aclaran si esta participación se traduce directamente en una aceleración del mismo y, menos aún, si favorece una cicatrización más rápida y más eficiente, como proponen algunos autores. Parte de estas incógnitas han podido ser aclaradas gracias a determinados modelos de experimentación animal. En modelos murinos con sección parcial del tendón de Aquiles, el PRP ha demostrado asociarse con una consolidación más rápida del callo tendinoso, la cual también es mecánicamente más eficiente28,29. Parte de este efecto se podría deber a su capacidad para acumular células circulantes proinflamatorias en la herida tendinosa23. En músculo, también algunos modelos han coincidido en observar un beneficio del PRP en el proceso reparativo miofibrilar. En un modelo de rotura-distensión del tibial anterior en ratas, el PRP parece acortar significativamente los tiempos de recuperación en aquellas lesiones que requieren de miogénesis para su recuperación, implicándolo directamente en el proceso de neoformación muscular30. Ninguno de estos trabajos ha podido determinar todavía las propiedades que, individualmente, tiene cada uno de los FC en estos 2 microambientes tan distintos. Tampoco está descrita la respuesta al PRP en modelos animales de tendinopatías inflamatorias31, más en consonancia con la realidad clínica del reumatólogo.
Hueso y articulacionesHistóricamente las primeras aplicaciones terapéuticas del PRP comenzaron en el campo de la cirugía dental y maxilofacial como compactante y sellante de implantes óseos32. Estas propiedades osteointegradoras llamaron la atención de algunos cirujanos ortopédicos que vieron en el PRP un adyuvante idóneo para acortar los tiempos de recuperación de ciertas cirugías33. Este efecto osteoinductor y sellante es todavía hoy objeto de controversia en algunos foros, pero no deja de ser la virtud más consistente y valiosa del PRP para muchos de sus defensores. Lo cierto es que la composición del PRP contiene múltiples factores, la mayoría de los cuales ha demostrado individualmente un potente efecto anabólico óseo. El potencial osteoinductor del factor de crecimiento derivado de plaquetas ha sido contrastado en sobradas ocasiones de tal manera que algunos autores han especulado con su utilización clínica (especialmente la isoforma BB) en la osteoporosis y en la consolidación del callo de fractura34. Una de las propiedades más conocidas del factor de crecimiento epidérmico (EGF) es su capacidad para expandir poblaciones de células madres totipotenciales. Además de expandir estas poblaciones, el EGF también es capaz de diferenciar estas células al linaje osteoblástico, favoreciendo de este modo notablemente la osteogénesis35,36. El factor de crecimiento fibroblástico (FGF) es un clásico y potentísimo estimulador de la diferenciación y de la activación osteoblástica cuyo potencial anabólico óseo se debe, en gran medida, a la activación de la vía Wnt37. En conejos, el FGF se ha utilizado con éxito para el tratamiento de la osteonecrosis de cadera evitando, no sólo el colapso cefálico, sino también el desarrollo de la coxartrosis secundaria38. En seres humanos, el FGF acelera notablemente la formación del callo de fractura acortando el tiempo de descarga de pacientes con osteotomía de tibia39. El factor de crecimiento transformativo β (TGF β) es un FC ampliamente involucrado en el anabolismo óseo y condral40. Sin embargo, la superfamilia del TGF β es un complejo entramado de factores y de receptores que, en virtud de distintas circunstancias, pueden convertir a esta molécula también en un poderoso estimulador osteoclástico determinante, por ejemplo, de la agresividad ósea del mieloma múltiple41 y de ciertas metástasis esqueléticas42.
El conjunto de todas estas evidencias parece indicar que, en virtud de su composición, el PRP reúne cualidades idóneas para desempeñar un potente papel osteoinductor, capaz de acelerar la consolidación de fracturas43 o de osteointegrar rápida y eficientemente distintos tipos de implantes óseos44,45. Sin embargo, la literatura no es unánime en ponderar estas hipotéticas propiedades beneficiosas del PRP46–48. Las concentraciones relativas de cada FC, su activación previa, su pauta de administración, el tipo de lesión o el microambiente sobre el que actúen, parecen factores determinantes para que las cualidades osteoinductoras de los FC se puedan traducir en beneficios clínicos reales del PRP.
El uso del PRP en articulaciones es relativamente reciente y dispone de escasa bibliografía preclínica. En lo relativo a artropatías degenerativas, tan solo existe un único trabajo que analiza el efecto del PRP en osteoartritis de rodilla en conejos. En este estudio, los autores analizaron histológicamente las rodillas de los conejos tratados intrarticularmente con microesferas impregnadas de PRP, observando una disminución de la progresión de la osteoartritis con respecto a controles. Mediante el uso de cultivos celulares complementarios, los autores concluyeron que este efecto se debía a una estimulación del metabolismo de la matriz condral mediante la síntesis de glucosaminoglicanos49. En lo relativo a artropatías inflamatorias, muy recientemente acaba de ser publicado un primer trabajo, de especial interés para los reumatólogos, que analiza el efecto del PRP en un modelo porcino de artritis reumatoide inducida por antígenos. En este estudio, el tratamiento intrarticular de las rodillas artríticas con PRP resultó, histológica e inmunohistoquímicamente, en una significativa atenuación de los cambios inflamatorios propios de la enfermedad, tanto a nivel de cartílago como de sinovial50. Estos resultados contrastan, en cierta medida, con el efecto proinflamatorio recientemente atribuido a las plaquetas en la artritis reumatoide y otras artropatías inflamatorias afines51.
Evidencia clínicaPlasma rico en plaquetas y tendinitis subacromialEl uso del PRP en el síndrome subacromial y todas sus variantes carece, hasta el momento, de estudios que lo evalúen como tratamiento único. La única evidencia disponible hace mención a su uso como adyuvante en la cirugía descompresora y reparadora del manguito de los rotadores. En este tipo de cirugía el PRP mejora los resultados de la cirugía reparadora convencional y acorta los tiempos de recuperación52,53.
Plasma rico en plaquetas y epicondilitisLa epicondilitis es una tendinopatia limitante, con clara tendencia a la cronificación, que tiene una respuesta aleatoria y, muchas veces, parcial a las infiltraciones de glucocorticoides y a la fisioterapia. Algunos autores han investigado la eficacia del PRP en esta dolencia dado el potencial efecto reparador observado en modelos animales. El ensayo pionero que analiza por primera vez el efecto del PRP en la epicondilitis data del año 2006. Se trata de un ensayo piloto, controlado con anestésico local, realizado sobre 19 pacientes con epicondilitis refractaria propuesta para cirugía9. En este estudio, los autores analizaron el efecto de una única infiltración de PRP sobre dolor (Visual Analog Scale de dolor [VAS]) y capacidad funcional (Mayo Elbow Score modificado). A las 8 semanas, los pacientes tratados referían una mejoría del 60% (16% en controles), que a los 2 años acabó siendo del 93%. No se comunicaron efectos adversos. Más recientemente, un estudio abierto con 30 pacientes también analizó el papel del PRP como terapia de rescate en la epicondilitis54. Al igual que en el trabajo anterior, se administró una única dosis de PRP y se evaluó su efecto al año sobre dolor (VAS) y capacidad funcional (American Shoulder & Elbow Surgeons outcome instrument). Se comunicó una mejoría ≥25% del VAS en el 90% de los pacientes infiltrados, sin encontrar tampoco efectos adversos. Las conclusiones de los 2 estudios coinciden en ponderar la utilidad clínica del PRP en este tipo de pacientes con epicondilitis refractaria. Conviene recordar que el diseño de ambos consta de algunos sesgos que limitan el valor de sus conclusiones. La limitación principal estriba en el escaso número de pacientes tratados en ambos casos, a lo que hay que añadir la falta de aleatorización y de enmascaramiento en el ensayo controlado y un diseño retrospectivo en el segundo trabajo. A principios del año 2010 se publicó el primer ensayo clínico de calidad que indicó el camino para extraer conclusiones menos vulnerables acerca del papel del PRP en pacientes con epicondilitis55. Se trataba de un ensayo clínico comparativo, controlado con corticoides, randomizado, doble-ciego, realizado sobre 100 pacientes con epicondilitis crónica que fueron seguidos un año. Se analizó el efecto de una única infiltración de PRP en la mejora del dolor y la capacidad funcional del codo, utilizando como control una infiltración corticoidea. Se consideró el descenso en la VAS o en el Disabilities of the Arm, Shoulder and Hand score (DASH) superior al 25% como medida de respuesta al tratamiento. En el grupo del PRP, se reportó un 73% de respondedores mientras que en el grupo de los que recibieron corticoides solo lo hicieron un 50%. En este trabajo tampoco se comunicó ningún efecto adverso. En funci’on de estos resultados, los autores concluyeron que el PRP superaba significativamente el beneficio clínico obtenido por los corticoides. Sin embargo, el beneficio clínico logrado por los corticoides en este trabajo está directamente condicionado por el hecho de que la totalidad de los pacientes a incluir en el ensayo debían tener acreditada su refractariedad previa a las infiltraciones locales de corticoides. Este sesgo impide, ciertamente, un análisis comparativo veraz, ya que se favorece notablemente al PRP en su comparación con los corticoides. Adicionalmente, los resultados de este trabajo refuerzan el concepto reportado en los 2 anteriores sobre la capacidad analgésica del PRP en el tratamiento de la epicondilitis, sin presentar efectos adversos clínicamente relevantes.
Plasma rico en plaquetas y fascitis plantarLa fascitis plantar representa otro problema común en la consulta de reumatología y, al igual que el resto de las tendinopatías, también tiende a la cronicidad. La única evidencia disponible que analiza el efecto del PRP en la fascitis plantar data de 2004 y tiene el valor de ser el primer trabajo que aplica PRP a algún tipo de tendinopatía. Se trata de una serie de 9 pacientes, seguidos durante un año, con fascitis plantar refractaria a AINE, inmovilización, fisioterapia e infiltración corticoidea que recibieron una única infiltración de PRP guiada por ecografía en los fascículos calcáneos central y medial. Se evaluó la mejoría del dolor y el cambio del patrón ecográfico. Al final del seguimiento 8 de los 9 pacientes quedaron asintomáticos aunque uno de ellos precisó una segunda dosis. El grosor ecográfico a los 3 meses disminuyó (de media) 1,2mm en el fascículo central y 2,3mm en el medial. La evidencia que aporta este trabajo parece merecedora de un estudio más detallado pero no deja de ser anecdótica dado el escaso número de pacientes tratados y los sesgos inherentes a un diseño retrospectivo y abierto.
Plasma rico en plaquetas y osteoartritis de rodillasLa aplicación del PRP al tratamiento de la osteoartritis de rodilla puede considerarse una indicación terapéutica relativamente reciente que focaliza, sin duda, la mayor parte de su investigación clínica actual. Esta nueva indicación ha dado pie a múltiples estudios en los 3 últimos años, tanto controlados como abiertos. Entre los primeros destaca el trabajo de un grupo español pionero en el uso terapéutico del PRP y poseedor de amplia experiencia14. Se trata de un estudio retrospectivo realizado sobre 60 pacientes con osteoartritis de rodillas, seguidos durante 5 semanas. En este estudio se comparó el efecto terapéutico del PRP con el ácido hialurónico de alto peso molecular (AHAPM). Los autores trataron a 30 pacientes con una infiltración semanal (durante 3 semanas) de PRP activado y a un número similar con una dosis única de AHAPM. Se consideró respondedores a aquellos con una disminución del WOMAC dolor ≥40% respecto a basal. Los autores encontraron al final del seguimiento un 33% de respondedores al PRP y un 10% al ácido hialurónico. De alguna manera sorprende un porcentaje tan bajo de respondedores a la viscosuplementación, que tiene documentados en la literatura porcentajes de respuesta muy superiores a los reportados en este ensayo56. Indudablemente, una respuesta tan pobre del grupo control favorece al PRP en el análisis comparativo de los autores. Probablemente, este análisis hubiera sido más veraz y de mayor relevancia clínica de haberse empleado un seguimiento más largo que permitiera al AHAPM desarrollar completamente el potencial analgésico acreditado en sus ensayos de eficacia57. En favor de los resultados de este estudio cabe destacar que por primera vez se especifican las concentraciones relativas de los FC contenidos en el plasma infiltrado; y también que es el único trabajo publicado que explícitamente utiliza un PRP libre de leucocitos, hecho de gran importancia para algunos autores58. Muy recientemente otro nuevo estudio, con un mayor número de pacientes, compara de nuevo el efecto del PRP con el del ácido hialurónico. Se trata de un nuevo ensayo comparativo sobre 150 pacientes con osteoartritis de rodillas, seguidos durante 6 meses. Se establecieron 3 brazos de tratamiento con 50 pacientes cada uno: PRP activado (una infiltración cada 21 días), AHAPM (dosis única) y ácido hialurónico de bajo peso molecular (AHBPM) (dosis única). Se analizó el efecto sobre la escala analógica visual de calidad de vida referente a estado de salud (EQ VAS) y la funcionalidad de la rodilla utilizando el International Knee Documentation Comitee index (IKDC). Al final del seguimiento, los autores reportaron una mejor respuesta de ambos índices en los pacientes tratados con PRP que en los tratados con AHAPM o AHBPM (p<0,005). En todos los grupos, la respuesta fue mejor en los pacientes más jóvenes y en aquellos que tenían una osteoartritis más incipiente. Como en el trabajo anterior, el análisis comparativo no resulta del todo equitativo sesgando, en este caso, claramente la comparación con el AHBPM. La utilización de un tratamiento control a dosis infra terapéuticas, como en este caso el AHBPM59, favorece en la comparación a la intervención que se pretende analizar (PRP). Además de este sesgo, la falta de aleatorización y de enmascaramiento restan credibilidad al análisis que, por otro lado, emplea unas medidas de desenlace poco habituales y de dudosa capacidad discriminativa para la osteoartritis de rodilla ya que el IKDC, por ejemplo, es un índice originariamente concebido para el análisis de inestabilidades ligamentarias de rodilla60.
Algunas series de pacientes con osteoartritis de rodillas, tratados con éxito con PRP, han sido comunicadas también en los últimos años. La serie más numerosa pertenece a un grupo español que incluyó a 261 pacientes tratados con 3 infiltraciones de PRP activado cada 15 días (no se detalla volumen infiltrado), a los que se siguió durante 6 meses61. Evaluaron VAS, WOMAC (dolor, rigidez y clase funcional), Lequesme y SF-36 (basal y a los 6 meses). En sus resultados, los autores comunicaron mejoría de todas las medidas desenlace, con porcentajes (con respecto a basal) que oscilaban entre el 8,4 del SF-36 y el 30,7 en la subescala de dolor del WOMAC. Otra serie, con un seguimiento más largo, incluyó a 100 pacientes con osteoartritis de rodillas tratados y seguidos durante un año15. En este trabajo, que emplea también 3 dosis de PRP activado administradas cada 3 semanas, los autores encontraron una mejora significativa del EQ VAS y el IKDC que, aunque fue más marcada en los primeros 6 meses, se mantuvo al año. Al igual que en otros estudios del mismo grupo, los pacientes con mayor beneficio fueron los jóvenes y los que tenían una artrosis menos evolucionada. Finalmente, cabe hacer mención a un último trabajo que evalúa el efecto del PRP en 14 pacientes con gonartrosis refractaria propuestos para recambio protésico62. Se incluyeron pacientes con osteoartritis de rodillas refractarios al tratamiento conservador (AINE, rehabilitación, acupuntura, férulas correctoras, infiltraciones de corticoides o de ácido hialurónico) que fueron tratados con 3 dosis de PRP activado (una al mes). Se observó el efecto al año sobre el VAS y el Knee Injury & Osteoartrhitis Outcome. Los autores observaron una mejoría lineal del VAS y del Knee Injury &Osteoartrhitis Outcome en el 60% de los pacientes al final del seguimiento. Aunque un 40% de los pacientes no mejoró, ninguno tuvo que ser intervenido quirúrgicamente durante el estudio.
En ninguno de los 5 trabajos anteriormente mencionados se comunicaron efectos adversos significativos, salvo un pequeño dolor local pospunción.
ConclusionesEl PRP es una novedosa herramienta terapéutica que cuenta con argumentos a favor y en contra para su uso en el espectro terapéutico del reumatólogo. Sus defensores ponderan entre sus máximas virtudes su naturaleza autóloga como garantía de inocuidad y de un excelente perfil de seguridad. Sin embargo, en la bibliografía analizada, no hay estudios de seguridad ni ensayos clínicos de calidad que permitan extraer esas conclusiones. Las series de pacientes y trabajos publicados carecen de seguimientos de imagen que aporten información acerca de eventuales efectos adversos locales en las áreas de infiltración. Si bien la tolerancia a la infiltración de PRP es excelente y su seguridad a corto plazo también, su perfil de seguridad a largo plazo es todavía incompleto o, al menos, incierto.
La supuesta eficacia del PRP en las distintas patologías analizadas no ha sido contrastada mediante ensayos clínicos de calidad. Los estudios que avalan su efectividad tienen un nivel de evidencia bajo penalizado por múltiples sesgos, tanto de diseño, como de ejecución. A pesar de ello, los resultados comunicados hasta ahora son unánimes en afirmar que el PRP, si no eficaz, sí es efectivo en el tratamiento de la epicondilitis y la osteoartritis de rodilla. Entre un buen número de especialistas esta evidencia científica puede resultar suficiente para justificar la utilización del PRP. Podrán argumentar que la medicina (hasta hace pocos años) ha progresado y crecido fuera de la ortodoxia de los ensayos clínicos, sostenida por un rigor científico menos exigente que el aquí revisado. No les falta razón. Para otra gran parte de clínicos, esta evidencia resultará insuficiente y no neutralizará el lógico recelo que produce un tratamiento indicado para múltiples patologías que nada tienen en común, amparado por un aura de inocuidad cuyo predicamento trasciende el ámbito estrictamente científico. Quizá sea más apropiado no dejarse seducir por modas ni tampoco detenerse en prejuicios académicos, sustanciando el valor de esta terapia con ensayos clínicos de calidad que no existen hasta la fecha, y parecen imprescindibles para desarrollar adecuadamente el potencial terapéutico del PRP. Estos trabajos permitirán precisar múltiples aspectos importantes sobre su utilidad terapéutica que todavía están confusos como su obtención, procesamiento o activación. Adicionalmente contribuirán a protocolizar las dosis, volúmenes y regímenes de administración más adecuados, a establecer indicaciones; y especialmente a evaluar más rigurosamente su potencial lesivo.
El reumatólogo, como referente en la patología médica del aparato locomotor, debería hacer valer su criterio y dimensionar adecuadamente este novedoso tratamiento en el ámbito reumatológico, al igual que otros especialistas ya lo hacen en el suyo propio.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesEl autor declara no tener ningún conflicto de intereses.