Analizar la experiencia española en un estudio internacional para evaluar tocilizumab en pacientes con artritis reumatoide (AR) con respuesta insuficiente al tratamiento con fármacos antirreumáticos modificadores de la enfermedad convencionales (FAME) o anti-TNF en condiciones cercanas a la práctica clínica habitual.
Material y métodosSubanálisis de 170 pacientes con AR que participaron en España en un ensayo clínico, internacional abierto de fase iiib, que presentaban una respuesta inadecuada al tratamiento con FAME o anti-TNF. Los pacientes recibieron 8mg/kg de tocilizumab cada 4 semanas en combinación con FAME o en monoterapia durante un periodo de 20 semanas. Se evaluaron la seguridad y la eficacia de tocilizumab distinguiendo entre pacientes con fallo a FAME o anti-TNF y, dentro de estos, entre los que habían hecho o no periodo de lavado del anti-TNF.
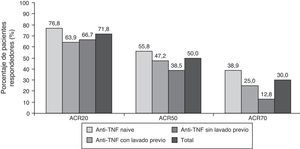
ResultadosLos acontecimientos adversos más frecuentes fueron infecciones (25%) y elevación de colesterol total (38%) y transaminasas (15%). Cinco pacientes abandonaron el estudio por un acontecimiento adverso. El 71/50/30% de los pacientes cumplía criterios de respuesta ACR 20/50/70 a los 6 meses del inicio del tratamiento con tocilizumab. Los pacientes naïve para anti-TNF presentaron una mayor respuesta ACR20: el 76% frente a un 64% en el grupo anti-TNF con lavado previo y el 66% en el grupo anti-TNF sin lavado previo.
ConclusionesSe confirma el perfil de seguridad de tocilizumab en pacientes con AR y fallo a FAME o anti-TNF. Tocilizumab es más eficaz en pacientes que no responden de forma satisfactoria al tratamiento con FAME convencionales que con anti-TNF.
To analyze the Spanish experience in an international study which evaluated tocilizumab in patients with rheumatoid arthritis (RA) and an inadequate response to conventional disease-modifying antirheumatic drugs (DMARDs) or tumor necrosis factor inhibitors (TNFis) in a clinical practice setting.
Material and methodsSubanalysis of 170 patients with RA from Spain who participated in a phase IIIb, open-label, international clinical trial. Patients presented inadequate response to DMARDs or TNFis. They received 8mg/kg of tocilizumab every 4 weeks in combination with a DMARD or as monotherapy during 20 weeks. Safety and efficacy of tocilizumab were analyzed. Special emphasis was placed on differences between failure to a DMARD or to a TNFi and the need to switch to tocilizumab with or without a washout period in patients who had previously received TNFi.
ResultsThe most common adverse events were infections (25%), increased total cholesterol (38%) and transaminases (15%). Five patients discontinued the study due to an adverse event. After six months of tocilizumab treatment, 71/50/30% of patients had ACR 20/50/70 responses, respectively. A higher proportion of TNFi-naive patients presented an ACR20 response: 76% compared to 64% in the TNFi group with previous washout and 66% in the TNFi group without previous washout.
ConclusionsSafety results were consistent with previous results in patients with RA and an inadequate response to DMARDs or TNFis. Tocilizumab is more effective in patients who did not respond to conventional DMARDs than in patients who did not respond to TNFis.
La artritis reumatoide (AR) es una de las enfermedades inflamatorias crónicas más comunes en los países occidentales. La prevalencia estimada de esta afección en España se sitúa en el 0,5%1. El tratamiento farmacológico de la AR se centra en la disminución de la actividad inflamatoria y en evitar la progresión de la lesión articular y sus consecuencias. El consenso de expertos de la Sociedad Española de Reumatología sobre manejo de la AR sitúa como objetivo terapéutico la remisión completa de la enfermedad y, en el caso de pacientes con AR de larga evolución, la baja actividad de la misma2.
Los fármacos antirreumáticos modificadores de la enfermedad (FAME) constituyen el tratamiento de elección tan pronto como se confirme el diagnóstico de AR2. Entre los distintos FAME, el perfil de eficacia y seguridad de metotrexato justifica que sea el tratamiento inicial recomendado, salvo contraindicación2,3. Como segundo escalón terapéutico en los pacientes con respuesta insuficiente, intolerancia o toxicidad a los FAME convencionales, se recomienda el tratamiento con agentes biológicos, siendo los antagonistas del factor de necrosis tumoral (anti-TNF) los más frecuentemente utilizados2. Sin embargo, entre el 30 y el 40% de los pacientes presentan una respuesta insatisfactoria a los anti-TNF, lo que ha conducido a la búsqueda de nuevos tratamientos para esta enfermedad4–7.
Entre las nuevas opciones terapéuticas se encuentra tocilizumab, un anticuerpo monoclonal que se une a los receptores de la interleucina 6 solubles y unidos a membranas inhibiendo la actividad proinflamatoria mediada por esta interleucina8. Diferentes ensayos clínicos han demostrado la eficacia y el buen perfil de seguridad de tocilizumab en distintas poblaciones de pacientes con AR, como es el caso de pacientes con respuesta inadecuada a FAME convencionales o a anti-TNF9–12. A pesar de los buenos resultados observados, siguen existiendo cuestiones abiertas sobre el uso de tocilizumab en la práctica clínica habitual, tales como su utilización en pacientes menos seleccionados que los incluidos en los ensayos clínicos o la necesidad de realizar un periodo de lavado previo de los anti-TNF antes de iniciar el tratamiento con este anticuerpo.
El propósito del presente estudio internacional fue evaluar la seguridad y la eficacia de tocilizumab en un perfil de pacientes con AR más próximos a la práctica clínica habitual, incluyendo más comorbilidades, tratamientos con combinación de FAME o ausencia de periodo de lavado de anti-TNF13. La alta participación española en el mismo nos indujo a realizar este subanálisis con la idea de analizar de forma específica el comportamiento de la muestra de pacientes españoles.
Pacientes y métodosEl ensayo clínico, abierto, fase iiib ACT-SURE; incluyó a pacientes de 25 países diferentes13. En el presente trabajo se describen los resultados obtenidos en el grupo de pacientes incluidos en España. El estudio fue realizado en 28 centros españoles. El estudio se realizó de acuerdo con los principios éticos de la Declaración de Helsinki y fue aprobado por el Comité Ético de Investigación Clínica de referencia. Todos los pacientes proporcionaron su consentimiento informado antes de la realización de cualquiera de los procedimientos específicos del estudio.
Se incluyó a pacientes de ambos sexos, mayores de 18 años, con actividad de la AR moderada o alta (Disease Activity Score [DAS] 28>3,2) de 6 o más meses de duración, que habían sido tratados con FAME convencionales o anti-TNF o ambos tipos de agentes a dosis estables durante un periodo superior a 8 semanas. Los pacientes que estuviesen recibiendo glucocorticoides debían haber recibido dosis estables ≤ 10mg/de prednisona o equivalente. Se excluyó del estudio a aquellos pacientes que habían sido tratados previamente con abatacept, rituximab o anakinra. Tras su inclusión en el estudio, los pacientes recibieron 8mg/kg de tocilizumab mediante infusión por vía intravenosa cada 4 semanas durante un periodo de 20 semanas (6 infusiones en total). Los pacientes podían recibir tocilizumab en monoterapia o en combinación con FAME, a criterio del investigador.
La seguridad se evaluó en la población de pacientes que había recibido como mínimo una dosis de tocilizumab y que dispusiera como mínimo de una evaluación posbasal de seguridad. Con el propósito de evaluar la necesidad de realizar un periodo de lavado de los anti-TNF antes de iniciar el tratamiento con este anticuerpo, se planificó un análisis de subgrupos una vez cerrada la base de datos. Se consideraron 3 grupos de pacientes: pacientes que no habían recibido tratamiento previo con anti-TNF (anti-TNF naïve), pacientes en los que se había interrumpido el tratamiento con anti-TNF como mínimo 2 meses antes de la primera infusión de tocilizumab (anti-TNF con lavado previo) y un tercer grupo formado por pacientes que estaban en tratamiento con anti-TNF y en los que se inició el tratamiento con tocilizumab sin realizar un lavado previo (anti-TNF sin lavado previo).
Se midieron los parámetros de eficacia que forman parte de la respuesta del American College of Rheumatology (ACR) y DAS28 en cada una de las visitas del estudio y a las 4 semanas de la última infusión de tocilizumab. La eficacia del tratamiento con tocilizumab se evaluó como el porcentaje de pacientes que cumplían los criterios de respuesta ACR20/50/70 y el porcentaje de pacientes que cumplían los criterios de remisión y baja actividad de la enfermedad basados en el DAS28 (DAS28 < 2,6 y DAS28 ≤ 3,2, respectivamente) a los 6 meses del inicio del tratamiento con tocilizumab. Los distintos parámetros evaluados permitieron el cálculo posterior de los índices compuestos Simplified Disease Activity Index (SDAI) y Clinical Disease Activity Index (CDAI). Adicionalmente, se estimó el porcentaje de pacientes que cumplían con los criterios de respuesta buena o moderada de la European League Against Rheumatism (EULAR) a los 6 meses de la primera infusión de tocilizumab. La discapacidad asociada a la enfermedad se evaluó mediante el cuestionario Health Assessment QuestionnaireDisability Index (HAQ-DI). La seguridad del tratamiento con tocilizumab se evaluó mediante la monitorización de los acontecimientos adversos y el análisis de parámetros hematológicos y bioquímicos en cada una de las visitas del estudio. Se consideraron como reacciones infusionales los acontecimientos adversos ocurridos durante las 24 h siguientes a la infusión de tocilizumab. La intensidad de los acontecimientos adversos y su relación con la medicación de estudio fue evaluada por los investigadores.
La eficacia del tratamiento con tocilizumab se evaluó en la población por intención de tratar, que estuvo constituida por aquellos pacientes que habían recibido una dosis o más de tocilizumab. Los pacientes que discontinuaron de forma prematura el estudio se consideraron como no respondedores en el análisis de la eficacia en base a los criterios ACR. El análisis de las otras variables de eficacia se realizó sobre el número de pacientes con datos disponibles en cada una de las visitas. Se realizaron estadísticas descriptivas para todas las variables obtenidas: media ± desviación estándar (DE) para las variables continuas y frecuencias para las variables categóricas.
ResultadosCaracterísticas demográficas y disposiciónDel total de 1.681 pacientes incluidos en el estudio internacional ACT-SURE, 170 pacientes pertenecían a los centros españoles participantes. La distribución de pacientes entre los 3 grupos fue similar a la del estudio global: 95 anti-TNF naïve, 36 anti-TNF con lavado previo y 39 anti-TNF sin lavado previo. Las características clínicas y demográficas basales para el total de pacientes y en los diferentes grupos considerados en función del tratamiento previo con anti-TNF se presentan en la tabla 1. La mayoría de los pacientes incluidos en el estudio recibió tocilizumab junto a otro FAME; únicamente 19 (11,2%) pacientes recibieron tocilizumab en monoterapia, cifra parecida a la del estudio global (14%). El 1,8% de los pacientes recibió tocilizumab en combinación con 2 FAME, cifra sensiblemente inferior a la del estudio global (19%). El metotrexato era el FAME más utilizado (62,9%), a una dosis media±DE de 15,9 (5,0) mg/semana. El 15,3% de los pacientes recibió leflunomida a una dosis media de 19,6±2,0mg/día. Un 72,4% recibía corticoides concomitantes. Los pacientes tenían una alta actividad basal (DAS28 6,1) y un tiempo de evolución de la AR cercano a 10 años, datos similares a los del estudio global.
Características clínicas y demográficas basales
| Anti-TNF naïve (N=95) | Anti-TNF con lavado previo (N=36) | Anti-TNF sin lavado previo (N=39) | Total (N=170) | |
| Edad (años), media±DE | 54,2±12,2 | 52,1±12,2 | 51,9±10,8 | 53,2±11,9 |
| Sexo (mujeres), n (%) | 84 (88,4) | 31 (86,1) | 37 (94,9) | 152 (89,4) |
| Duración de la AR (años), media ± DE | 8,8±8,2 | 9,9±5,9 | 11,6±7,8 | 9,7±7,7 |
| Número de FAME concomitantes, n (%) | ||||
| 0 | 9 (9,5) | 3 (8,3) | 7 (17,9) | 19 (11,2) |
| 1 | 84 (88,4) | 32 (88,9) | 32 (82,1) | 148 (87,1) |
| 2 | 2 (2,1) | 1 (2,8) | – | 3 (1,8) |
| Pacientes en tratamiento con leflunomida, n (%) | 10 (10,5) | 8 (22,2) | 8 (20,5) | 26 (15,3) |
| Pacientes en tratamiento con metotrexato, n (%) | 63 (66,3) | 23 (63,9) | 21 (53,8) | 107 (62,9) |
| Pacientes en tratamiento con corticoides, n (%) | 59 (62,1) | 34 (94,4) | 30 (76,9) | 123 (72,4) |
| PCR (mg/dl), media±DE | 1,3±1,9 | 2,2±2,6 | 2,2±3,1 | 1,7±2,4 |
| VSG (mm/h), media±DE | 42,1±24,4 | 48,6±30,2 | 49,3±27,8 | 45,1±26,6 |
| NAD, media±DE | 19,5±13,7 | 19,2±16,2 | 22,2±14,7 | 20,1±14,5 |
| NAT, media±DE | 11,0±9,4 | 11,0±8,5 | 14,1±11,3 | 11,7±9,7 |
| DAS28, media±DE | 6,0±1,2 | 6,1±1,1 | 6,3±1,1 | 6,1±1,1 |
| SDAI, media±DE | 33,9±15,0) | 36,3±15,7 | 38,6±14,7 | 35,5±15,1 |
| CDAI, media±DE | 32,6±14,2 | 34,1±15,1 | 36,4±14,4 | 33,8±14,4 |
AR: artritis reumatoide; CDAI: Clinical Disease Activity Index; DAS28: Disease Activity Score basado en 28 articulaciones; DE: desviación estándar; FAME: fármacos antirreumáticos modificadores de la enfermedad; NAD: número de articulaciones dolorosas; NAT: número de articulaciones tumefactas; PCR: proteína C reactiva; SDAI: Simplified Disease Activity Index; VSG: velocidad de sedimentación globular.
El 88,8% (n=151) de los pacientes completaron los 6 meses del estudio, de forma similar a los del estudio global. Los motivos de discontinuación del estudio fueron retirada del consentimiento informado en 5 pacientes, acontecimiento adverso en 5 pacientes, respuesta inadecuada al tratamiento en 3 pacientes, decisión del investigador en 2 pacientes, violación de algún criterio de selección en 2 pacientes y pérdida de seguimiento en 2 pacientes.
SeguridadLos principales resultados de seguridad del estudio se presentan en la tabla 2. En total, se registraron acontecimientos adversos en 118 pacientes. Los que habían sido tratados previamente con anti-TNF, y en los se había realizado un lavado previo, presentaron una aparente menor incidencia numérica de acontecimientos adversos, a diferencia del estudio global, en el que no se detectaron diferencias de seguridad en función de hacer o no lavado de anti-TNF. Las infecciones fueron uno de los acontecimientos adversos más frecuentes; el 25,9% de los pacientes presentó como mínimo una infección durante el estudio. Un único paciente presentó una infección del tracto respiratorio superior que fue considerada como un acontecimiento adverso grave (1,1 por 100 pacientes-año), frente a un 5,1 por 100 pacientes-año en el estudio global. Un 15,3% de los pacientes presentó reacciones infusionales, entendiendo por tales cualquier acontecimiento adverso ocurrido durante o en las 24 h siguientes a la infusión; esta cifra fue numéricamente más baja en el grupo de pacientes con lavado previo de anti-TNF (8,3%). No se registró ningún caso de muerte durante el estudio. Los acontecimientos adversos no infecciosos que originaron retirada del estudio fueron: fractura de húmero, queratitis ulcerativa, cáncer de laringe y fallo respiratorio.
Resultados de seguridad
| Pacientes | Anti-TNF naïve (N=95) | Anti-TNF con lavado previo (N=36) | Anti-TNF sin lavado pevio (N=39) | Total (N=170) |
| AA, n (%) | 69 (72,6) | 21 (58,3) | 28 (71,8) | 118 (69,4) |
| AAG, n (%) | 5 (5,3) | 2 (5,6) | 1 (2,6) | 8 (4,7) |
| Infecciones, n (%) | 28 (29,5) | 6 (16,7) | 10 (25,6) | 44 (25,9) |
| Infecciones graves, n (%) | 1 (1,1) | 0 (0,0) | 0 (0,0) | 1 (0,6) |
| Reacciones infusionales, n (%) | 17 (17,9) | 3 (8,3) | 6 (15,4) | 26 (15,3) |
| Elevación ALT a>1,5×LSN, n (%) | 19 (20,0) | 3 (8,3) | 6 (15.3) | 28 (16.4) |
| Elevación colesterol total de valores normales a>200mg/dl, n (%) | 40 (42,1) | 13 (36,1) | 12 (30,8) | 65 (38,2) |
| Recuento neutrófilos<1500/mm3, n (%) | 16 (16,8) | 4 (11,1) | 5 (12.8) | 25 (14.7) |
AA: acontecimientos adversos; AAG: acontecimientos adversos graves; ALT: alanina aminotransferasa; LSN: límite superior de normalidad.
El 14,7% de los pacientes desarrolló neutropenia durante el tratamiento con tocilizumab; en ningún caso el recuento de neutrófilos fue inferior a 500/mm3. El 16,4% de los pacientes presentó elevación de los niveles de alanina aminostransferasa (ALT), siendo esta elevación algo más frecuente en la población naïve anti-TNF; solo el 1,7% de los pacientes presentó elevación de ALT entre 3 y 5 veces el límite superior de normalidad, no detectándose ningún caso de elevaciones superiores a esta cifra. En un 38,2% de pacientes se observaron elevaciones del colesterol total.
EficaciaLos datos de eficacia estuvieron en línea con los del estudio global. El 71,8% (n=122), el 50% (n=85) y el 30% (n=51) de los pacientes cumplían los criterios de respuesta ACR20, ACR50 y ACR70 a los 6 meses del inicio del tratamiento con tocilizumab, respectivamente (fig. 1). Es destacable el alto porcentaje de pacientes que alcanzan respuesta ACR20 después de recibir la primera infusión de tocilizumab (44,7%). Este porcentaje se incrementó progresivamente hasta la semana 16, manteniéndose más o menos constante hasta la visita de los 6 meses (datos no mostrados). La respuesta ACR20 a los 6 meses en el grupo naïve para anti-TNF fue superior a la de los otros dos grupos (76,8% vs. 63,9% en el grupo anti-TNF con lavado previo y 66,7% en el grupo anti-TNF sin lavado previo), de acuerdo con lo observado en otros estudios con tocilizumab9,12.
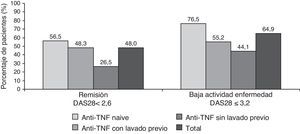
El 48 y el 64,9% de los pacientes presentaban remisión clínica y baja actividad de la enfermedad, respectivamente, según el índice DAS28 a los 6 meses de tratamiento (fig. 2). Estas respuestas también fueron mayores en los pacientes naïve para el anti-TNF (76,5% vs. 55,2% en el grupo anti-TNF con lavado previo y 44,1% en el grupo anti-TNF sin lavado previo).
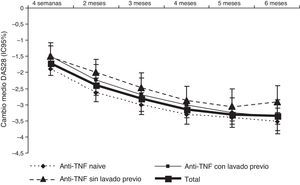
La actividad DAS28 disminuyó progresivamente a lo largo del tratamiento con tocilizumab (fig. 3). El valor medio del DAS28 a los 6 meses de tratamiento era 2,7±1,3, lo que supone una mejoría media de 3,4±1,5 puntos en el conjunto de pacientes.
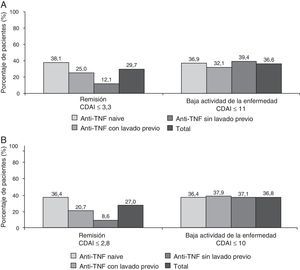
En la figura 4 se representa el porcentaje de pacientes en remisión clínica o baja actividad de la enfermedad a los 6 meses de tratamiento, según los criterios SDAI y CDAI. Como puede observarse, las respuestas a estos 2 índices (cuya única diferencia reside en que el CDAI no incluye ningún reactante de fase aguda) fueron muy similares en los diferentes subgrupos de pacientes. En cuanto a la respuesta EULAR, el 84,1% de los pacientes presentaba respuesta buena o moderada a los 6 meses (el 86,3% de los pacientes anti-TNF naïve, el 80,5% del grupo anti-TNF con lavado previo y el 82,1% del grupo anti-TNF sin lavado previo). Adicionalmente, la mayoría de los pacientes (75,5%) presentó una mejora clínicamente significativa en el cuestionario de discapacidad HAQ-DI (reducción de 0,22 o más puntos) (datos no mostrados).
En este estudio se incluyó a pacientes tratados con tocilizumab, tanto en monoterapia como combinado con FAME. Las respuestas ACR20, 50 y 70 no mostraron diferencias relevantes entre ambos grupos de tratamiento (datos no mostrados)
DiscusiónEl valor añadido del estudio ACT-SURE reside en su diseño, con un perfil de pacientes de AR más próximo a la práctica clínica habitual, incluyendo poblaciones con comorbilidades más amplias, pacientes con diferente refractariedad a tratamientos (fallo a FAME y a anti-TNF) y que podían recibir tocilizumab tanto en monoterapia como en combinación con diferentes FAME a dosis cercanas a las máximas utilizadas, incluso combinaciones de estos. Además, se estudiaba la conveniencia o no de realizar un periodo de lavado de anti-TNF antes de iniciar tocilizumab.
Este diseño tiene especial importancia a la hora de analizar los datos de seguridad. Los resultados globales del ACT-SURE han confirmado el perfil de seguridad de tocilizumab observado en estudios anteriores9–12. La incidencia de acontecimientos adversos en el subgrupo de pacientes incluidos en España es similar al reportado en el estudio global13. Los principales efectos adversos detectados fueron infecciones y alteraciones de parámetros analíticos. Sin embargo, se observan algunas diferencias entre ambos análisis. Es destacable que en la subpoblación española solo hubo un caso de infección grave entre los 170 pacientes incluidos (1,1 por 100 pacientes-año), frente a una tasa de 5,1 por 100 pacientes-año en el estudio global. Otro dato distinto de seguridad en el análisis de nuestra población es el hecho de que las reacciones infusionales, las infecciones y las elevaciones de transaminasas ocurrieron menos frecuentemente en los pacientes con lavado de anti-TNF que en el resto.
Se desconocen las razones de estas discrepancias. En principio, no parece achacable a diferencias en el perfil de pacientes, dado que la distribución entre los 3 subgrupos, el tiempo de evolución de la AR o la actividad basal fueron similares en los 2 análisis. La menor frecuencia de pacientes tratados con la combinación de tocilizumab y 2 o más FAME en nuestra población podría ser un dato diferenciador, aunque desconocemos si este fue un factor asociado a mayor tasa de infecciones graves en el análisis global13. El hecho de que el número de pacientes en el subgrupo español con lavado de anti-TNF sea solo de 36 (21%) hace probable que se trate solo de una variación aleatoria. Esto es importante, dado que el análisis global sugiere que no es necesario realizar un lavado del anti-TNF antes de iniciar tratamiento con tocilizumab, lo que tiene importantes consecuencias prácticas.
En cuanto a la eficacia, nuestros datos confirman el resultado general de tocilizumab, con un efecto rápido y consistente tanto en pacientes naïve a anti-TNF como con respuesta inadecuada a estos fármacos. Como era de esperar, la respuesta es mejor en el primer grupo de pacientes que en el segundo. Esto coincide con los resultados observados previamente con tocilizumab9-12. Las pequeñas diferencias de eficacia de tocilizumab tras realizar lavado o no del anti-TNF están probablemente en relación con el número limitado de pacientes, junto con diferencias basales en la actividad y la duración de la enfermedad. Los pacientes en los que no se realizó un lavado previo presentaban una AR algo más severa y de una duración superior que los pacientes en los que sí se realizó este lavado. En el análisis global de los datos, no se habían observado diferencias de eficacia entre estos grupos13.
El mayor porcentaje de pacientes respondedores según el índice DAS28 en comparación con la aplicación de los índices SDAI y CDAI puede explicarse por el efecto significativo de tocilizumab sobre los reactantes de fase aguda y el peso que la velocidad de sedimentación globular tiene en la fórmula del DAS28. Sin embargo, el hecho de que las respuestas SDAI y CDAI (2 índices que se diferencian solo en que CDAI no incluye el reactante de fase aguda) sean similares demuestra que la eficacia de tocilizumab no se debe principalmente a su efecto sobre reactantes.
Resulta interesante el hecho de que la eficacia de tocilizumab en monoterapia en este análisis sea similar a la de su uso combinado con FAME. Si bien el hecho de que los pacientes no fueran aleatorizados en función de este parámetro limita la significación de este dato, otros resultados apoyan esta idea14, lo que convierte a tocilizumab en una buena opción para pacientes intolerantes o con contraindicación a FAME. Además, un estudio reciente ha demostrado la superioridad de tocilizumab frente a adalimumab en monoterapia15.
Las principales limitaciones de este análisis residen en el número de pacientes y en la duración del seguimiento de 6 meses. Aunque el análisis de periodos más largos de tratamiento es fundamental al evaluar la seguridad de un fármaco, nuestros resultados coinciden con otros estudios de mayor duración16. Por el contrario, el perfil de pacientes menos seleccionado y, por lo tanto, más próximos a la práctica clínica real, aporta gran valor a estos datos.
En conclusión, los resultados del presente estudio permiten confirmar el perfil de seguridad de tocilizumab en pacientes con AR y fallo a FAME o anti-TNF. Tocilizumab parece ser más efectivo en pacientes que no responden de forma satisfactoria al tratamiento con FAME convencionales que con anti-TNF.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesRoche Farma ha sido el promotor del estudio ACT SURE. J.M. Álvaro-Gracia ha recibido ayudas para investigación u honorarios por asesorías o ponencias de Abbott, Aventis, Bristol Myers Squibb, Janssen-Cilag, MSD, Pfizer, Roche, Tigenix y UCB; F.J. Blanco ha recibido ayudas para investigación u honorarios de Absciex, Abbott, Ardea Bioscience, Bioiberica, Bristol Myers Squibb, Celgene, Celltrion, Lilly, Merck, Novartis, Novo Nordisk, Pfizer, Roche, Sanofi Aventis, Tigenix y UCB; A. Fernández-Nebro ha recibido ayudas para investigación u honorarios por ponencias de Abbott, MSD, Pfizer y Roche; A. García-López ha recibido ayudas para investigación u honorarios de Abbott, Amgen, Bristol Myers Squibb, MSD, Roche y UCB; F.J. Navarro ha recibido ayudas para investigación u honorarios de Abbott, Celltrion, Roche y UCB; S. Bustabad ha recibido ayudas para investigación y honorarios de Roche, MSD, UCB, Abbott y Bristol Myers Squibb; Y. Armendáriz es empleada del Departamento Médico de Roche, y J.A. Román-Ivorra ha recibido ayudas para investigación u honorarios de Abbott, Actelion, Amgen, Bristol Myers Squibb, MSD, Pfizer, Roche y UCB.
Los autores del manuscrito desean agradecer la participación de los investigadores en el estudio ACT SURE, así como el soporte proporcionado por Marta Muñoz Tudurí, de la Unidad de Medical Writing de TFS Develop España.
Luis Álvarez Vega Jose
Jose María Álvaro-Gracia
Luis Arboleya Rodríguez
Joaquín Belzunegui Otano
Francisco Blanco García
M. del Sagrario Bustabad Reyes
Javier Calvo Catalá
Cesar Díaz Torne
Antonio Domingo Gómez Centeno
Alejandro Escudero Contreras
Luis Fernández Domínguez
Antonio Fernández Nebro
Ángel García Aparicio
Sergio García Pérez
Alicia García Testal
Jose García Torón
Eduardo Girona Quesada
Manuel Guzmán Ubeda
Isabel Ibero Díaz
Francisco Javier Manero Ruiz
Carlos Marras Fernandez-Cid
Sara Marsal Barril
Francisco Javier Navarro Blasco
Francisco Javier Narváez García
Lucia Pantoja Zarza
María Trinidad Pérez Sandoval
Javier del Pino Montes
Carmen Paula Ramos Núñez
Elena Riera Alonso
Manuel Riesco Díaz
Jose Ramón Rodríguez Cros
Jose Manuel Rodríguez Heredia
Carlos Rodríguez Lozano
José Andrés Román Ivorra
Rosa Rosello Pardo
Jose Javier Salaberri Maestrojuan
Raimon Sanmarti Sala
Manuel Utrilla Utrilla
Tomás Ramón Vázquez Rodríguez
Paloma Vela Casasempere
Los nombres de los investigadores españoles participantes en el estudio ACT SURE están relacionados en el anexo 1.