Las miopatías necrosantes autoinmunes (NAM) son unas entidades raras y emergentes de las miopatías inflamatorias idiopáticas (MII).
Su presencia se ha asociado a conectivopatías, infecciones virales, neoplasias, anticuerpos frente a la partícula de reconocimiento de la señal (anti-SRP) y a anticuerpos frente a la proteína 3-hidroxi-3-metilglutaril-coenzima A reductasa (HMG-CR) (asociada al empleo o no de estatinas).
Las NAM asociadas al anti-SRP presentan unas características clínicas y anatomopatológicas que las diferencian del resto de las MII, resultando en un peor pronóstico. Hasta el momento han sido muy pocos los casos publicados tratados con rituximab y con diferente respuesta clínica.
Presentamos el caso de una mujer de 30 años con NAM asociada al anti-SRP refractaria a tratamiento convencional inmunosupresor y que ha sido controlada a largo plazo con la combinación de rituximab, metotrexato y corticoides.
Necrotizing autoimmune myopathy (NAM) is a rare and emerging entity of idiopathic inflammatory myopathy (IIM).
They have been associated with connective tissue disorders, viral infections, malignancy, anti-signal recognition particle (SRP) and anti-3-hydroxy-3-methylglutaryl-coenzyme A reductase protein (with or without the use of statins).
Anti-SRP associated NAM has different clinical and histological characteristics that differentiate them from other IIM, resulting in a poor prognosis. Very few cases treated with rituximab have been published, with varying clinical response.
Here we describe a case of anti-SRP associated NAM refractory to conventional immunosuppressants and its successful long-term management with the combination of rituximab, corticosteroids and methotrexate.
Las miopatías necrosantes autoinmunes (NAM) suelen presentarse como una miopatía con elevación marcada de la creatinquinasa (CK), hallazgos histopatológicos característicos (presencia de fibras musculares necróticas y regenerativas, práctica ausencia de infiltrados inflamatorios) y mala respuesta al tratamiento convencional.
Los anticuerpos frente la partícula de reconocimiento de la señal (anti-SRP) se describieron por primera vez en 19861 y posteriormente se describieron en pacientes diagnosticados de miopatías inflamatorias (MII) con un curso más severo. Los anticuerpos anti-SRP se dirigen frente a una subunidad de 54kD de unas proteínas ribonucleares con actividad GTP-asa implicadas en el transporte de nuevas proteínas al retículo endoplasmático2–4.
Rituximab es un anticuerpo monoclonal quimérico dirigido frente al CD20 cuyo empleo es habitual en otras conectivopatías5. Existen series de casos publicados de NAM tratados con rituximab, con diferentes respuestas clínicas6–10.
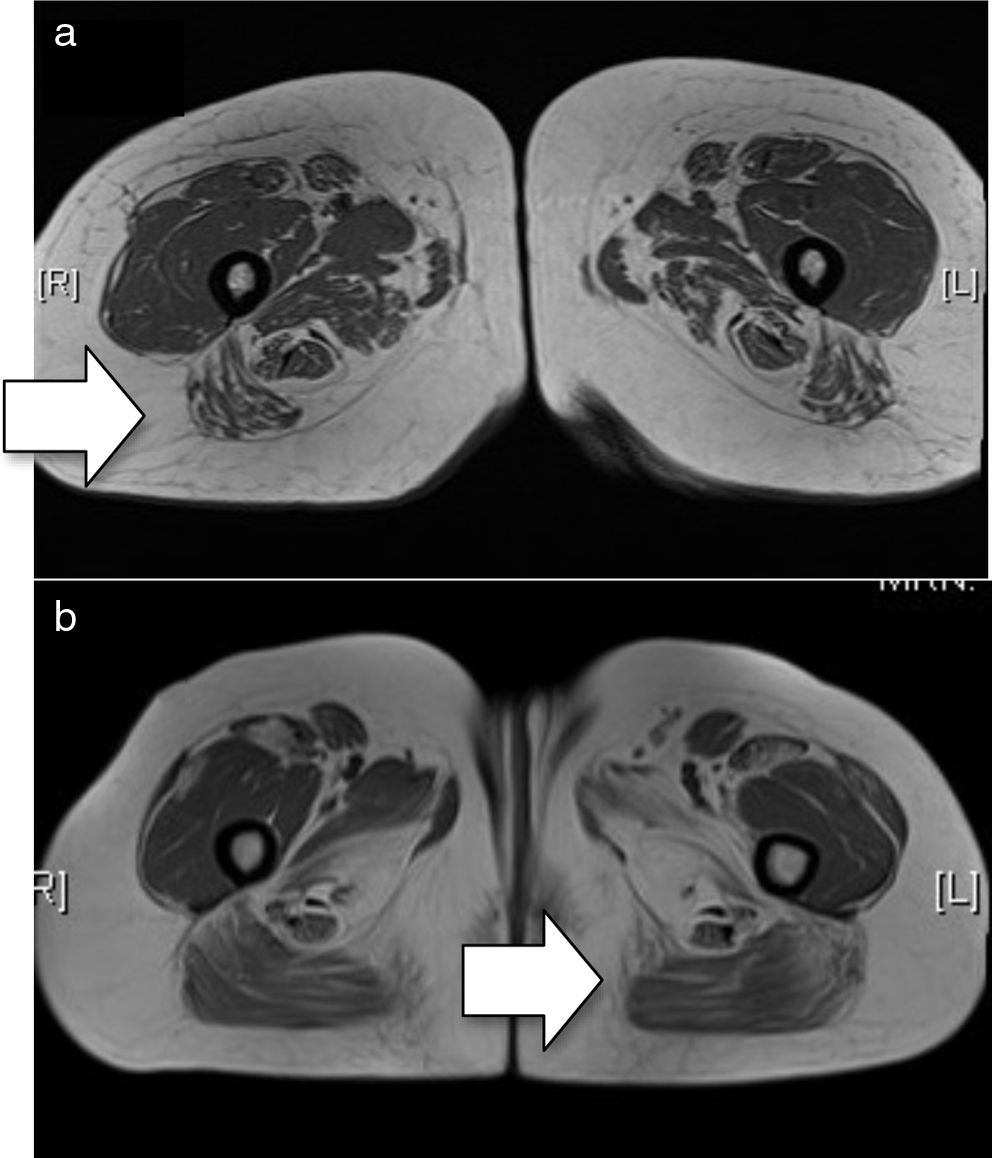
Caso clínicoMujer de 30 años diagnosticada de NAM en función de la presencia de miopatía proximal, disfagia a líquidos y disfonía de 2 meses de evolución, elevación de enzimas musculares (CK 5.922UI/l, aldolasa 84UI/l), electromiograma con patrón miopático, signos en la resonancia magnética de edema intramuscular en cinturas escapulares y pelvianas (fig. 1a) y hallazgos anatomo-patológicos de miopatía necrosante que había presentado fallo terapéutico a tratamiento convencional (corticoides, inmunoglobulinas, azatioprina).
a) RM basal (secuencia T1). Se aprecia mínimo edema en extremo distal de ambos sartorios y en grácilis. Afectación de ambos compartimentos, en el compartimento anterior más afectados los vastos laterales y medios y en compartimento posterior, identificándose de manera general una mayor afectación posterior (flecha); b) RM posterior al tratamiento con rituximab (secuencia T1). Se aprecia una afectación bilateral y simétrica de ambos compartimentos objetivando atrofia muscular con depósitos de la grasa de forma difusa, en el compartimento anterior más afectados los vastos laterales y medios y en compartimento posterior los isquiotibiales, con predominio de la afectación en el compartimento posterior (flecha).
Ante los hallazgos histológicos se solicitaron anticuerpos anti-SRP que resultaron positivos (técnica IFI 1:1.280). Se inicia tratamiento con metotrexato (hasta 30mg/semana). A los 3 meses mejoró clínicamente, excepto a nivel de la musculatura del psoas-ilíaco (4/5). Con la reducción progresiva de corticoides se produce un deterioro clínico y analítico. Por lo cual se inicia tratamiento concomitante con rituximab (2 dosis de un gramo). Cinco meses más tarde había mejorado. A los 6 meses se pauta un nuevo ciclo de rituximab para mantenimiento de la respuesta terapéutica.
Una resonancia magnética muscular a los 2 años muestra ausencia de signos de actividad inflamatoria (fig. 1b).
Al disminuir el metotrexato por debajo de 22,5mg/semana comienza nuevamente con afectación clínica y analítica, por lo que se aumentó la dosis consiguiendo nuevamente control clínico (excepto debilidad en musculatura del psoas-iliaco) en el último año.
DiscusiónPara nuestro conocimiento se han publicado menos de 30 casos de NAM anti-SRP tratadas con rituximab6–10. Pinal-Fernandez et al.7 describen 17 pacientes tratados con rituximab, siendo aparentemente efectivo en 13 de ellos. La duración del efecto biológico del rituximab era variable (desde 6-9 meses hasta más de 2 años). En nuestra paciente no se ha administrado en más ocasiones desde mediados de 2012.
También se han publicado 2 casos refractarios que mejoraron con la combinación de corticoides, plasmaféresis y rituximab8, así como otros 2 casos refractarios tratados con rituximab con buenos resultados9.
Sin embargo, una serie británica10 de 2 pacientes tratados con rituximab presentaron una pobre respuesta clínica.
En nuestro caso se administraron 2 ciclos de rituximab, produciéndose una exacerbación al reducir la dosis del metotrexato con buen control posterior aumentado la dosis del mismo. Los valores de CK de la paciente fueron más bajos de lo publicado en otras series, y quizás sea este uno de los motivos por los que se consiguió un buen resultado terapéutico. Asimismo nos llama la atención los hallazgos de imagen, en donde se aprecia una mayor afectación del compartimento posterior del muslo cuando clínicamente no ha presentado afectación del mismo.
ConclusiónLas NAM se deben sospechar en pacientes con hallazgos atípicos de MII, tanto histopatológicos (presencia de fibras musculares necróticas, práctica ausencia de infiltrados inflamatorios) como clínicos (pobre respuesta a inmunosupresores).
Rituximab podría ser una buena opción terapéutica para aquellos casos en los que fracasa el tratamiento estándar.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.